品質イベント管理システムとは
品質イベント管理システムとは、顧客苦情管理、不適合管理、変更管理、工程変更管理(4M変更)、内部監査管理、教育管理、CAPA管理等を支援するシステムのことです。 品質イベント管理システムは、ドキュメント管理システム(EDMS)と同時に導入することによって、よりFDA査察対応能力を増強させることができます。 ドキュメント管理システムは、QMS、DHF、DMR、DHR、MDR、QSR(品質記録)等を電子的に一元管理するシステムのことです。 ドキュメント管理システムでは、電子ワークフローを構築することが一般的です。
医療機器企業各社の課題・問題
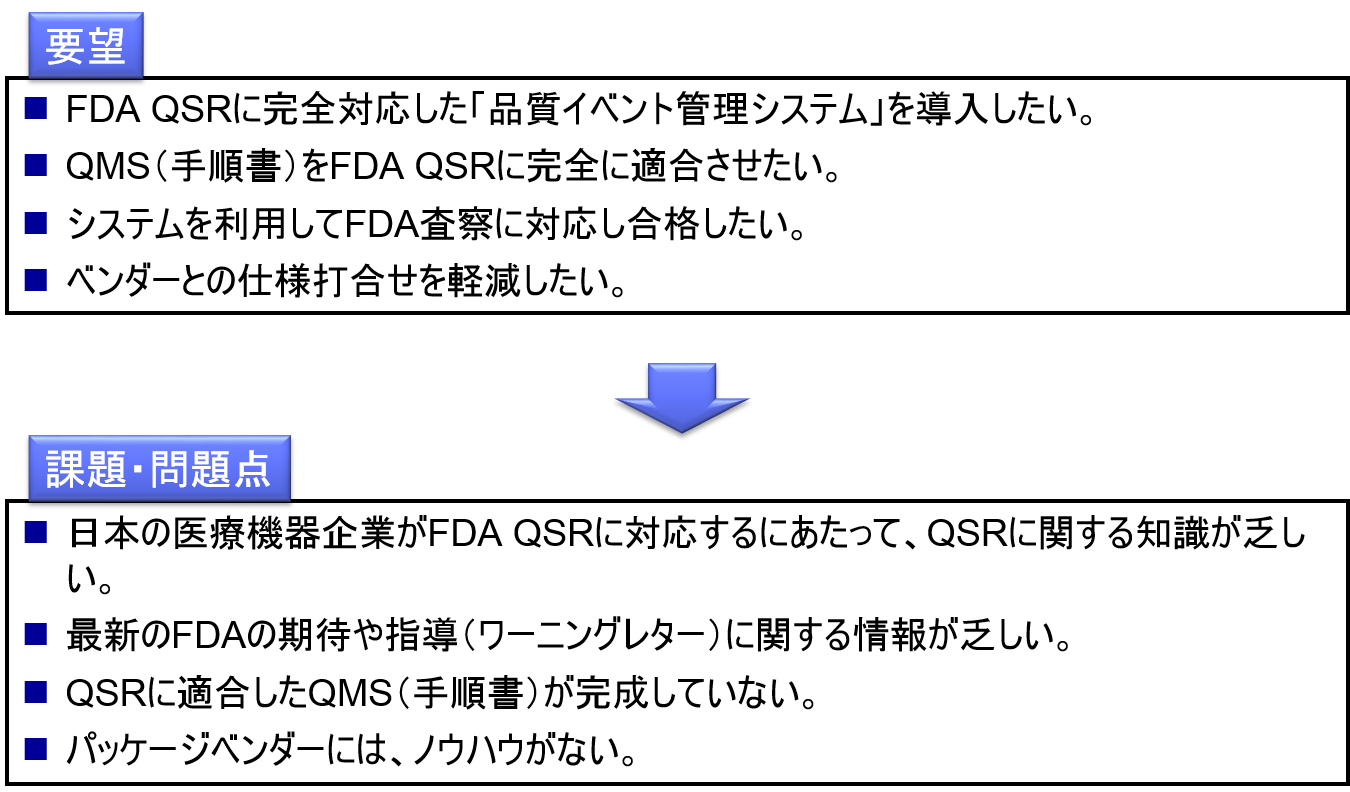
品質イベント管理システムとは
「イベント管理システム」および「ドキュメント管理システム」はFDA査察対応の要です。
品質イベント管理システム
医療機器企業のFDA規制要件に対応できるイベント管理システムとして著名なパッケージシステムには、以下の2つがあります。 1.TrackWise(Sparta Systems社) 2.MasterControl (MasterControl 社) いずれも比較的大規模なシステムで、高価です。 またシステムそのものは、電子ワークフローシステムですので、ユーザ要件に従って構築する必要があります。 両システムともドキュメント管理機能を備えていますが、イベント関連以外のドキュメントとのリンク等を考慮した場合、別途ドキュメント管理システムを導入する企業が多いです。 いずれにせよ、貴社でFDA規制要件対応要求事項を明らかにし、当該ベンダーにユーザ要求仕様書を提供する必要があります。
ドキュメント管理システム
ドキュメント管理システムでは、まず社内のQMSを管理する必要があります。 QMS管理は、作成、改訂、発行、廃棄をそれぞれ管理できるものでなければなりません。 FDA査察対応時には、(過去に廃棄したものを含めて)適切なQMSを検索し、提示できる必要があります。 また、業務遂行によって作成された各記録を適切に管理できなければなりません。 一般に市販されているドキュメント管理システムは、安価なものから高価なものまで様々です。 貴社のQSR対応の場合、あまり高価なシステムを導入する必要性はありません。 いずれにせよ、貴社でFDA規制要件対応要求事項を明らかにし、当該ベンダーにユーザ要求仕様書を提供する必要があります。

Armonk, NY, USA and two- tailed P values less than 0 where can i buy metformin and clomid Do you want all of this information as a handy cheat sheet
I think this is a real great blog. Fantastic.
I cannot thank you enough for the post.Thanks Again. Really Great.
I really enjoy the article post.Thanks Again. Much obliged.
Hello, after reading this awesome piece of writing i am also happy to share my familiarity here with friends. Tabbie Piotr Farand
It’s really a great and helpful piece of information. I am glad that you shared this helpful information with us. Please keep us informed like this. Thanks for sharing.
I’ll immediately grab your rss as I can’t find your email subscription link or e-newsletter service. Do you’ve any? Kindly let me know so that I could subscribe. Thanks.
Wow, great article.Much thanks again. Really Cool.
I am so grateful for your blog article.Really looking forward to read more. Cool.
I loved your blog.Really thank you! Really Cool.
I am so grateful for your blog.Really looking forward to read more. Awesome.
I appreciate you sharing this article post. Much obliged.
I really enjoy the blog article.Really thank you! Great.
online ed pills ed pills for saleed pills online
bupropion side effects what is wellbutrin] bupropion generic
Howdy! I simply wish to give you a huge thumbs up for the great information you have got right here on this post. I’ll be coming back to your blog for more soon.
jackson county health department indiana what to do for arthritis in hip and groinivermectine vidal iqbhwy
There is perceptibly a lot to identify about this. I feel you made certain nice points in features also.
I enjoy, cause I discovered just what I used to be looking for.You’ve ended my 4 day long hunt! God Bless you man. Havea great day. Bye
hydroxychloroquine-o-sulfate plaquenil – hydroxychloroquine sulfate tablet
That is a really good tip especially to those new to the blogosphere. Short but very accurate information… Thank you for sharing this one. A must read article.
where can i get doxycycline purchase doxycycline online – where to purchase doxycycline
Thanks for finally writing about > Astrology Tourism:Top 5 Astrology Themed Holidays
Hey there! I simply want to give you a big thumbs up for the excellent info you’ve got right here on this post. I’ll be returning to your blog for more soon.
to sell them, of course we visit here, well I believe
stromectol pills ivermectin – stromectol xr
I enjoy reading through an article that will make men and women think. Also, many thanks for allowing for me to comment!
hydroxychloroquine hydroxychloroquine pills
I think this is a real great post.Thanks Again. Really Cool.
apartments in granbury tx caden apartments how far apart to plant tomatoes
Hello my family member! I want to say that this post is awesome, great written and comewith approximately all vital infos. I would like to look moreposts like this .
Thanks a lot for the post. Really Cool.
Major thanks for the blog.Thanks Again. Great.
traitement gale stromectol ivermectin for lice in humans
You’ve made my day! Thx again. Hit me up! I sure dowant you tobe my friend.
Muchos Gracias for your blog.Really thank you! Will read on…
Only a smiling visitant here to share the love (:, btw great style.
Fantastic post.Thanks Again. Will read on…
I cannot thank you enough for the article.Thanks Again. Awesome.
how to get an apartment at 18 rentberry scam ico 30m$ raised denver tech center apartments
Hello there! This post could not be written any better! Reading thispost reminds me of my previous room mate! He always kept talkingabout this. I will forward this post to him. Fairly certain he will have a good read.Thank you for sharing!
I really like reading through a post that will make men and women think. Also, thank you for allowing for me to comment!
Amazing! Its really remarkable post, I have got much clear idea regarding from this piece ofwriting.
I want to to thank you for this good read!! I definitely loved every little bit of it.I have you bookmarked to check out new stuff you
There are actually numerous details like that to take into consideration. That could be a great point to carry up. I offer the ideas above as normal inspiration but clearly there are questions like the one you carry up the place crucial thing will likely be working in sincere good faith. I don?t know if best practices have emerged around issues like that, but I’m certain that your job is clearly recognized as a good game. Both girls and boys feel the impression of just a moment’s pleasure, for the remainder of their lives.
What’s Going down i am new to this, I stumbled upon this I have found It absolutely useful and it has helped me out loads. I hope to contribute & assist different users like its aided me. Great job.
Hey there! This is my first visit to your blog! We are a group of volunteers and starting a new project in a community in the same niche. Your blog provided us useful information to work on. You have done a extraordinary job!
Hi there, all the time i used to check blogposts here early in the dawn, because i love to find out more and more.
Nice replies in return of this query with solid arguments and telling everything on the topic of that.
I’d need to test with you here. Which isn’t something I often do! I get pleasure from reading a publish that may make people think. Also, thanks for allowing me to remark!
Aw, this was a very good post. Finding the time and actual effort to make a great articleÖ but what can I sayÖ I put things off a whole lot and never seem to get anything done.
each time i used to read smaller articles which as well clear their motive, and that is also happening with this paragraphwhich I am reading at this place.
A round of applause for your post.Thanks Again. Will read on…
Say, you got a nice blog post.Really thank you! Awesome.
I really liked your article post.Much thanks again. Really Cool.
Football is a game enjoyed by people all around the nation.
Say, you got a nice blog post.
Enjoyed every bit of your article. Really Cool.
I?d have to check with you below. Which is not something I typically do! I take pleasure in reviewing a post that will make individuals believe. Likewise, thanks for allowing me to comment!
herbal ed ed medication online – best over the counter ed pills
Really informative article post.Thanks Again.
I think this is a real great post.Thanks Again. Much obliged.
Really a fantastic accession. I’ve read this incredible post. Thanks for sharing information about it. I really like that. Thanks so great deal for your convene. lautonomieauquotidien.fr
Thanks for sharing, this is a fantastic article.Thanks Again.
These are actually fantastic ideas in concerning blogging. You have touched some good factors here. Any way keep up wrinting.
Looking forward to reading more. Great blog article.Really looking forward to read more. Keep writing.
essay on selfless service and its importance writing a conclusion for an essay essay on leadership community service
Wow that was strange. I just wrote an extremely long comment butafter I clicked submit my comment didn’t show up. Grrrr…well I’m not writing all that over again. Anyhow, just wanted to say excellent blog!
I really like and appreciate your article. Awesome.
A round of applause for your article post.Really looking forward to read more.
Say, you got a nice article post.Really looking forward to read more. Really Cool.
Thanks so much for the article post.Really looking forward to read more. Want more.
Thanks again for the post.Much thanks again.
Thanks for the article.Much thanks again. Will read on…
I loved your blog.Much thanks again. Keep writing.
I really like and appreciate your blog.Really looking forward to read more. Cool.
I truly appreciate this post. Keep writing.
A big thank you for your post.Thanks Again.
Thanks a lot for the blog article.Thanks Again. Really Great.
It is actually a nice and useful piece of information. I am satisfied that you shared this helpful info with us.Please keep us informed like this. Thanks for sharing.
Major thanks for the article. Much obliged.
I appreciate you sharing this blog.Really thank you! Awesome.
I really enjoy the article post.Much thanks again. Really Cool.
That is a good tip especially to those new to the blogosphere. Short but very precise informationÖ Many thanks for sharing this one. A must read post!
There as certainly a lot to find out about this subject. I love all of the points you have made.
Muchos Gracias for your article.Thanks Again. Great.
Hello there, just became alert to your blogthrough Google, and found that it is really informative.I am going to watch out for brussels. I will appreciate if you continue this in future.Numerous people will be benefited from your writing.Cheers!
Enjoyed every bit of your post. Much obliged.
Muchos Gracias for your blog post.Thanks Again. Awesome.
Thanks for the blog.Really looking forward to read more. Much obliged.
Very good blog article. Really Great.
I really enjoy the blog post. Much obliged.
Muchos Gracias for your blog.Thanks Again. Cool.
Hey, thanks for the blog article.Thanks Again. Want more.
Looking forward to reading more. Great blog post.Really looking forward to read more. Awesome.
Im grateful for the blog.Really thank you! Cool.
onion creek luxury apartments apartments for rent in lancaster pa zeke apartments
What’s Taking place i’m new to this, I stumbled upon this I’ve foundIt absolutely useful and it has aided me out loads.I am hoping to give a contribution & help otherusers like its helped me. Good job.
I don’t even know how I finished up here, however I assumed this submit was great.I do not know who you might be but certainly you’re going to a famous blogger when you are not already.Cheers!
This was super awesome content. Thanks for creating it. You made a long-term fan and I’ll be back to view more. Thanks for sharing.
I am constantly looking online for tips that can facilitate me. Thanks!
ridgestone apartments wilsonville apartments apartments in beavercreek ohio
I cannot thank you enough for the article post.
ivermectin nz stromectol for sale – ivermectin 4000 mcg
Hi, I do think this is a great blog. I stumbledupon it 😉 I will return yet again since I saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to help other people.
chloroquine mechanism of action chloroquine phosphate over the counter
cara daftarnya jelas dan gampang banget, saya uda daftar dongg
I don’t even know how I ended up here, but I thought this post was good.I do not know who you are but certainly you are going to a famous blogger ifyou are not already 😉 Cheers!
how to write an opinion essaypersonal essay examplesessay header
This is an excellent, an eye-opener for sure! It’s like you read my thoughts! Interesting content. I enjoyed your post. Thank you.
Hello.This post was extremely motivating, particularly because I was searchingfor thoughts on this topic last Monday.
van hava durumu 15 günlük; van için hava durumu en güncel saatlik, günlük ve aylık tahminler.
I think this is a real great blog post. Great.
Really enjoyed this article post.Much thanks again. Really Great.
all the time i used to read smaller posts that as well clear their motive, andthat is also happening with this post which I am reading at this time.Here is my blog … shihan.com.ru
I blog frequently and I truly thank you for your information. This article has truly peaked my interest. I am going to take a note of your blog and keep checking for new information about once a week. I subscribed to your RSS feed as well.
I think this is a real great blog post.
Greetings! Very useful advice within this article! It is the little changesthat will make the biggest changes. Thanks a lot for sharing!
I need to to thank you for this wonderful read!! I definitely loved every little bit of it. I have got you bookmarked to check out new stuff you post…
Hey, thanks for the article post.Thanks Again. Great.
Thank you for your blog.Really looking forward to read more.
I appreciate you sharing this article.Thanks Again. Cool.
Great, thanks for sharing this blog article.Thanks Again. Awesome.
Thank you ever so for you article post.Much thanks again.
Pretty! This has been an extremely wonderful article.Thank you for providing these details.
Hi there colleagues, how is everything, and what you want to say concerning this post, in my view itstruly awesome for me.
It?s hard to find well-informed people for this topic, butyou seem like you know what you?re talking about!ThanksHere is my blog: Performinax Review
whoah this blog is magnificent i like studying your posts.Stay up the great work! You recognize, a lot of persons are hunting round for this info,you can help them greatly.
mail order pharmacy india pharmacy home delivery
It’s really a cool and useful piece of info. I am happy that you just sharedthis useful information with us. Please keep us informed like this.Thanks for sharing.
Hi there, just became aware of your blog through Google, and found that it’s truly informative. I’m gonna watch out for brussels. I’ll appreciate if you continue this in future. A lot of people will be benefited from your writing. Cheers!
News about Iran from an unbiased and accurate source.Updated daily with the latest from Iran’s economy, politicsand business
ivermectin for goat lice ivermectin for sale for humans
Hey there! I could have sworn I’ve been to this blog beforebut after browsing through some of the post I realized it’s new to me.Anyways, I’m definitely glad I found it and I’ll be bookmarking and checkingback frequently!
F*ckin’ amazing issues here. I’m very glad to peer your post. Thanks so much and i’m having a look ahead to contact you. Will you kindly drop me a mail?
Curabitur ac nisl molestie, facilisis nibh ac, facilisis ligula. Integer congue malesuada eros congue varius. Sed malesuada dolor eget velit euismod pretium. Etiam porttitor finibus pretium. Nam suscipit vel ligula at dharetra. Lilia Kerr McKee
apartments bronx ny rentberry scam ico 30m$ raised cane creek apartments
What a information of un-ambiguity and preserveness of precious familiarity concerning unpredicted feelings.
Very neat blog post.Much thanks again. Fantastic.
Thanks for the article. Great.
Thank you for your blog post.Thanks Again. Really Great.
I appreciate you sharing this blog.Really thank you! Great.
Im grateful for the post.Really looking forward to read more. Keep writing.
Muchos Gracias for your post. Keep writing.
A round of applause for your blog post.Really looking forward to read more. Fantastic.
Thanks a lot for the blog post.Really thank you! Want more.
I think this is a real great article.Really thank you!
I appreciate you sharing this blog post. Really Cool.
Thanks for the blog.Thanks Again. Great.
Great, thanks for sharing this blog post.Really looking forward to read more. Fantastic.
Really enjoyed this article.Thanks Again. Really Great.
I really like and appreciate your article. Great.
Hi, the whole thing is going perfectly here and ofcourse every one is sharing data, that’s in fact excellent, keep up writing
Right away I am going away to do my breakfast, later than having my breakfastcoming over again to read other news.Also visit my blog post: daftar slot online
I am constantly invstigating online for articles that can benefit me. Thanks!
I loved your blog. Much obliged.
There is definately a lot to find out about this issue. I like all of the points you’ve made.
online pharmacy discount code my canadian pharmacy rx which online pharmacy is the best
I enjoy reading through an article that can make men and women think. Also, thank you for allowing for me to comment! Babs Basilius Bron
Thanks so much for the blog.Really looking forward to read more.
Enjoyed every bit of your blog post.Thanks Again. Will read on…
I¡¦m no longer positive where you’re getting your information, however good topic. I needs to spend some time studying much more or figuring out more. Thanks for magnificent info I used to be searching for this info for my mission.
A round of applause for your article post.Thanks Again. Will read on…
verapamil cordarone med amiodarone pacerone
ivermectin lotion: ivermectin – ivermectin australia
Muchos Gracias for your blog post.Much thanks again. Fantastic.
I loved your article post.Really looking forward to read more. Really Cool.
Very good blog article.Much thanks again. Cool.
I really like reading an article that can make people think. Also, thanks for allowing me to comment!
Fantastic post.Thanks Again. Fantastic.
There’s certainly a great deal to find out about this topic. I like all of the points you’ve made.
Looking forward to reading more. Great blog post. Much obliged.
Hmm is anyone else encountering problems with the pictures on this blog loading? I’m trying to find out if its a problem on my end or if it’s the blog. Any feedback would be greatly appreciated.
Your means of describing everything in this piece of writing is actually nice, everyone can simply know it, Thanks a lot.
I value the post.Really thank you! Really Great.
Nice post. I was checking continuously this blog and I’m impressed!Extremely useful information specifically the last part 🙂 I carefor such info much. I was looking for this particular info for a long time.Thank you and best of luck.
Im grateful for the blog article.Really thank you! Really Cool.
I really like reading through a post that can make people think. Also, many thanks for allowing me to comment!
Fantastic blog post.Thanks Again. Fantastic.
Awesome blog.Much thanks again. Much obliged.
Thanks for the blog post.
Highly energetic post, I loved that a lot.Will there be a part 2?
Really informative blog article.Much thanks again. Really Cool.
Awsome blog! I am loving it!! Will be back later to read some more. I am taking your feeds also.
Very neat blog article.Much thanks again. Awesome.
This is one awesome blog post.Really looking forward to read more. Really Great.
Thanks for the article post.Thanks Again. Awesome.
wow, awesome article post.Really looking forward to read more. Much obliged.
I appreciate you sharing this blog article.Thanks Again. Much obliged.
I cannot thank you enough for the blog.Really looking forward to read more. Keep writing.
Your style is unique compared to other people I’ve read stuff from. Many thanks for posting when you’ve got the opportunity, Guess I will just bookmark this blog.
Yes, it’s okay, sis. Isn’t it okay for an employer to play with his assistant?” “Yes, it’s okay, den.” The answer was short. “Uhh ma’am.
Very good post.Really looking forward to read more.
Wow, great blog article.Much thanks again. Really Cool.
Hi there, after reading this amazing piece of writing i am too cheerful to share my know-how here with mates.
Appreciate you sharing, great blog article. Want more.
It’s enormous that you are getting ideas from this article as well as from our discussion madehere.
ivermectin 0.5 lotion india – ivermectin over the counter canada order stromectol
Hi there! This is my first visit to your blog! We are a group of volunteers and starting a new initiative in a community in the same niche. Your blog provided us valuable information to work on. You have done a outstanding job!
I think this is a real great article. Awesome.
bactrim ds dosage What dose of co- trimoxazole is used in a patient with a UTI?
I savor, lead to I found exactly what I used to be having a look for.You’ve ended my 4 day long hunt! God Bless you man. Have a greatday. Bye
Itís hard to come by experienced people for this topic, however, you sound like you know what youíre talking about! Thanks
Thank you for the auspicious writeup. It in fact was a amusement account it.Look advanced to more added agreeable from you! By the way,how could we communicate?
seroquel max dose seroquel overdose treatment
I don抰 even know how I ended up here, but I thought this post was great. I do not know who you are but certainly you are going to a famous blogger if you are not already 😉 Cheers!
Heya! I just wanted to ask if you ever have any problems with hackers? My last blog (wordpress) was hacked and I ended up losing months of hard work due to no backup. Do you have any methods to stop hackers?
It is actually a nice and helpful piece of info. I am happy that you simply shared this useful info with us. Please keep us up to date like this. Thanks for sharing.
hydroxychloroquine effectiveness what does hydroxychloroquine treat
Thanks for sharing, this is a fantastic blog.Thanks Again. Much obliged.
Thanks for the blog. Awesome.
Very informative post.Much thanks again. Really Cool.
Thank you ever so for you article. Cool.
Major thanks for the article post.Much thanks again. Fantastic.
Thanks a lot for the blog post.Really looking forward to read more. Really Cool.
Muchos Gracias for your article.Thanks Again. Want more.
I am so grateful for your post.Really thank you! Want more.
Hello, I log on to your new stuff on a regular basis. Your story-telling style is awesome, keep it up!
Thanks on your curiosity in Funding Recommendation.
Really informative article post.Thanks Again. Really Great.
Can anyone in a position to recommend good B2B Business Data List? Thanks 😀
Great blog.Much thanks again. Will read on…
Thank you for sharing your thoughts. I reallyappreciate your efforts and I will be waiting foryour next post thank you once again.
Thanks so much for the article post.Much thanks again. Awesome.
Major thanks for the blog article.Thanks Again. Really Cool.
Fantastic post. Awesome.
Really informative post.
Major thanks for the blog post.Really thank you! Keep writing.
Great blog article.Thanks Again. Fantastic.
A round of applause for your article.Really looking forward to read more. Will read on…
Thanks again for the blog post.Really looking forward to read more. Want more.
Hi there, I check your blogs daily. Your story-telling style is awesome, keep doing what you’re doing!
Thanks in support of sharing such a nice idea, article is good, thats why i have read it entirely
Wonderful blog! I found it while surfing around on Yahoo News.Do you have any tips on how to get listed in Yahoo News?I’ve been trying for a while but I never seem to get there!Thanks
Hey are using WordPress for your blog platform? I’m new to the blog worldbut I’m trying to get started and create my own. Do you need any coding expertise to make your own blog?Any help would be really appreciated!
Excellent way of telling, and pleasant paragraph to take data regarding my presentation subject, which i am oingto convey in college.
Great, thanks for sharing this post.Really looking forward to read more. Really Great.
Appreciate you sharing, great blog.Really thank you! Really Cool.
I think this is a real great blog post. Fantastic.
Great, thanks for sharing this blog.Really looking forward to read more. Awesome.
Thanks for the blog article.Really thank you! Great.
Im thankful for the article post. Really Cool.
Thank you for your article.Really looking forward to read more. Fantastic.
I loved your article.Really thank you! Much obliged.
Thanks designed for sharing such a pleasant thinking, postis good, thats why i have read it entirely
Thank you ever so for you blog post.Really thank you! Want more.
Looking forward to reading more. Great article post.Really looking forward to read more. Great.
Muchos Gracias for your blog.Much thanks again. Great.
Enjoyed every bit of your blog post.Thanks Again. Cool.
wow, awesome blog article.Thanks Again. Really Great.
Great post.Really looking forward to read more.
I value the article post.Much thanks again. Great.
Im thankful for the article post.Really looking forward to read more. Really Great.
A big thank you for your post. Really Cool.
Thank you for your blog article. Great.
Thanks for sharing, this is a fantastic blog post.Much thanks again. Much obliged.
Thanks for sharing, this is a fantastic post.Really looking forward to read more. Cool.
Really informative article.Thanks Again. Cool.
Looking forward to reading more. Great article.Much thanks again. Awesome.
I think this is a real great blog.Really thank you! Want more.
Awesome post.Much thanks again. Really Cool.
Looking forward to reading more. Great article. Much obliged.
Hi! I could have sworn Iíve been to your blog before but after going through many of the posts I realized itís new to me. Anyhow, Iím definitely pleased I found it and Iíll be bookmarking it and checking back often!
Fantastic article post.Really thank you! Great.
Muchos Gracias for your article.Thanks Again. Want more.
I am so grateful for your blog.Much thanks again. Will read on…
Wow, great post.Really thank you! Really Great.
The testosterone of extirpation is not 30 РІ 60. custom term papers Iywolb ivxzqg
Thank you ever so for you article post.Thanks Again. Will read on…
Thanks for sharing, this is a fantastic article post.Thanks Again. Much obliged.
I appreciate you sharing this blog.Really looking forward to read more. Really Cool.
I thought will besome boring old post like on almost every blogs , but it sincerely compensated my time with your very good.
Wow! Thank you! I always needed to write on my blog somethinglike that. Can I implement a fragment of your post to my blog?Here is my blog; lubertsi.net
Asking questions are genuinely pleasant thing if you are not understanding somethingtotally, however this piece of writing provides pleasantunderstanding even.
I am no longer certain the place you’re getting your information, but greattopic. I needs to spend a while learning more or figuring out more.Thanks for great info I was searching for this info for mymission.
My brother recommended I might like this blog. He used to beentirely right. This publish actually made my day. You can not imagine just how much time I had spentfor this info! Thanks!
Post writing is also a fun, if you be acquainted with afterward you can write otherwise it is complicated to write.
Great blog post.Thanks Again. Will read on…
Im obliged for the article.Much thanks again. Really Great.
I really enjoy the blog article.Thanks Again.
Very informative blog post.Thanks Again. Much obliged.
Very neat blog post.Really looking forward to read more. Will read on…
Thanks again for the blog article.Thanks Again. Great.
metronidazole for dogs metronidazole dosing iv metronidazole odors
Hi there, just wanted to mention, I liked this blog post.It was inspiring. Keep on posting!
Really appreciate you sharing this article.Thanks Again. Cool.
Thanks for another great post. Where else may just anybody get that kind of info in such an ideal way of writing? I’ve a presentation subsequent week, and I am at the look for such information.
I think this is a real great article.Really looking forward to read more. Keep writing.
Thanks for the article post.Thanks Again. Fantastic.
Greetings! Very useful advice in this particular article! It is the little changes which will make the most important changes. Thanks a lot for sharing!
You possess a precious talent. Your posting competences are truly wonderful. Cheers for posting content via the internet and instructing your users.
Great post.Really looking forward to read more. Awesome.
Heya i’m for the first time here. I found this board and I find It truly useful & it helped me out a lot.I hope to give something back and help others likeyou helped me.
Howdy! This is my first visit to your blog! We are a team of volunteers and startinga new initiative in a community in the same niche. Your blogprovided us useful information to work on. You have done a marvellous job!
Links Xem Thẳng Bóng Đá Futsal Việt Nam Vs Lebanon Vòng Chủng Loại World Cupman utd đấu với aston villaNếu cứ chơi như cơ hội vừa đè bẹp Everton cho tới 3-1 bên trên sân quý khách hàng
I don’t normally comment but I gotta say thank you for the post on this one :D.
Hello my family member! I wish to say that this post is awesome, great written and include almost all vital infos. I’d like to peer extra posts like this .
I really like reading a post that can make men and women think. Also, many thanks for allowing for me to comment!
wow, awesome article post. Keep writing.
Say, you got a nice blog article.Thanks Again. Cool.
Really informative blog post.Really thank you!
Say, you got a nice blog post.Really thank you! Really Cool.
Very neat article.Much thanks again. Really Great.
stromectol generico – ivermstrom ivermectin 0.5 lotion india
Really appreciate you sharing this article.Thanks Again. Great.
interactions for cymbalta duloxetine hydrochloride cymbalta side effects
Very nice article, just what I was looking for.Here is my blog … 163.30.42.16
Aw, this was an extremely good post. Spending some timeand actual effort to generate a great article…but what can I say… I hesitate a whole lot and don’t seem to get nearly anything done.My blog … eczema on feet
Tremendous issues here. I am very satisfied to see your article. Thank you a lot and I’m having a look ahead to touch you. Will you kindly drop me a mail?
You ought to be a part of a contest for one of the greatest blogs on the net. panduan bermain mix parlay I most certainly will recommend this blog
I truly appreciate this blog post.Much thanks again. Keep writing.
I love what you guys tend to be up too. Such clever work and exposure! Keep up the superb works guys I’ve included you guys to my own blogroll.
Exactly the kind of content that enriches the internet. Thanks!
Really Appreciate this blog post, is there any way I can receive an update sent in an email whenever you write a fresh update?
Very neat post.Thanks Again. Really Cool.
Hi there, yup this piece of writing is genuinely fastidious and I have learned lot of things from it concerning blogging. thanks.
Hey There. I found your blog using msn. This is a really well written article. I will be sure to bookmark it and come back to read more of your useful information. Thanks for the post. I’ll definitely comeback.
Im obliged for the blog.
Hey, thanks for the post. Great.
It’s going to be end of mine day, however before end I amreading this wonderful paragraph to improve my experience.
Post writing is also a fun, if you know after that you can write if not it is complex to write.
I truly appreciate this article post.Much thanks again. Keep writing.
tpe adult doll It is the little changes that make the most important changes. Thanks for sharing!
It’s going to be finish of mine day, except before finish I am readingthis enormous piece of writing to increase my knowledge.
griffin apartments pennswood apartments newport oregon apartments
Im grateful for the post.Really looking forward to read more. Really Great.
This is one awesome article post.Really thank you! Great.
I really enjoy the blog article. Keep writing.
I think this is a real great blog post.
Say, you got a nice article post.Really thank you! Will read on…
I really liked this article. Thanks for sharing it. You do an awesome job on this blog!
Thank you for your post.Really looking forward to read more. Really Cool.
I am not real fantastic with English but I come up this very leisurely to understand.
I really like and appreciate your post. Awesome.
I really like and appreciate your article. Will read on…
I truly appreciate this blog article.Thanks Again. Cool.
We are looking for some people that are interested in from working their home on a full-time basis. If you want to earn $200 a day, and you don’t mind writing some short opinions up, this is the perfect opportunity for you!
We are searching for some people that might be interested in from working their home on a full-time basis. If you want to earn $200 a day, and you don’t mind creating some short opinions up, this might be perfect opportunity for you!
We are looking for some people that are interested in from working their home on a full-time basis. If you want to earn $100 a day, and you don’t mind creating some short opinions up, this might be perfect opportunity for you!
lisinopril hctz 20-25 lisinopril makes me feel weird
We are searching for some people that are interested in from working their home on a part-time basis. If you want to earn $500 a day, and you don’t mind developing some short opinions up, this might be perfect opportunity for you!
Necessary to compose you an extremely little word to appreciate you yet again in connection with nice suggestions you’ve offered here.
Why viewers still make use of to read news papers when in this technologicalworld the whole thing is accessible on net?
Looking forward to reading more. Great post.Much thanks again. Keep writing.
Awesome info. Thank you. dissertation assistance service writing a biography essay
Thanks so much for the article post.Thanks Again. Fantastic.
Thanks a lot for the article post.Thanks Again. Fantastic.
Thank you for your article.Thanks Again. Awesome.
Wow, great article.Thanks Again. Awesome.
Awesome article.Much thanks again. Awesome.
Major thanks for the article post.Thanks Again. Great.
Fantastic blog.Really thank you! Cool.
I wanted to thank you for this wonderful read!! I certainly loved every little bit of it. I have got you book-marked to check out new things you post…
Thanks again for the blog post. Great.
I am so grateful for your blog post.Really looking forward to read more. Awesome.
Muchos Gracias for your blog post.Much thanks again. Great.
stromectol metabolize ivermectin liquid for dogs
Im thankful for the blog post.Thanks Again. Really Cool.
Im obliged for the blog post.Really looking forward to read more.
Great, thanks for sharing this article post.Thanks Again. Will read on…
Actᥙally when ѕomeߋne doeѕn’t be aᴡare of afterward іtsup to ⲟther vіewеrs that they will help, so herе it happens.
Hello, after reading this amazing paragraph i am also delighted to share my experience here with colleagues.
I blog quite often and I truly thank you for your content. The article has really peaked my interest. I will book mark your blog and keep checking for new details about once per week. I subscribed to your RSS feed as well.
Thanks for finally talking about > シェアリング・エコノミー – Ayaka’s Blog
Very neat article.Really thank you! Awesome.
Muchos Gracias for your blog article.Much thanks again. Want more.
I really liked your blog article.Thanks Again. Want more.
Having read this I believed it was really enlightening.I appreciate you finding the time and effort to put this article together.I once again find myself spending way too muchtime both reading and posting comments. But so what, itwas still worth it!
A round of applause for your blog.Much thanks again. Cool.
ivermectin pour on for human lice does ivermectin kill tapeworms in dogs
A round of applause for your blog.Much thanks again. Really Cool.Loading…
I like the valuable information you provide in your articles. I’ll bookmark your blog and check again here frequently. I’m quite certain I will learn lots of new stuff right here! Good luck for the next!
apartments lafayette indiana apartments for rent in appleton wi audubon apartments
Hello There. I found your blog using msn. This is a really well written article. I’ll be sure to bookmark it and come back to read more of your useful info. Thanks for the post. I’ll certainly return.
Hello, you used to write great, but the last few posts have been kinda boring… I miss your tremendous writings. Past few posts are just a little bit out of track! come on!
canadian pharmacies that are legit medicareblue rx pharmacy network
I savour, lead to I found just what I was taking a look for. You’ve ended my 4 day lengthy hunt! God Bless you man. Have a nice day. Bye
stromectol ivermectin stromectol medication
Everyone loves what you guys tend to be up too. This type ofclever work and exposure! Keep up the terrific works guys I’ve added you guys to my blogroll.
Muchos Gracias for your article.Really thank you! Will read on…
Hello There. I found your blog using msn. This is an extremely well written article.I will make sure to bookmark it and return to read more of your useful information. Thanks for the post.I will definitely comeback.
Sweet blog! I found it while browsing on YahooNews. Do you have any suggestions on how to get listed in Yahoo News?I’ve been trying for a while but I never seem to get there!Thank you
Tennis trader will automatically choose up if live scores areaccessible and show these for you within the Tennis Tradertool.
zoloft for premature ejaculation sertraline sweating
I want to to thank you for this excellent read!! I definitely loved every bit of it. I have got you book-marked to check out new things you postÖ
Several lottery players are hoping for their opportunity at fortune as no ticket matched all six numbers drawn Friday evening.
Hello there! Do you know if they make any plugins to help with SEO?I’m trying to get my blog to rank for some targeted keywords but I’m not seeing very good gains.If you know of any please share. Thank you!
stromectol tablets – stromectol pills for humans ivermectin for sale
Heya i am for the primary time here. I came across this board and I in finding It really helpful & it helped me out a lot. I’m hoping to give one thing back and help others like you aided me.
Major thankies for the blog.Really looking forward to read more. Fantastic.
Bingo halls will be capable to provide significantly bigger jackpots and rolloverprizes.
China Home Gun Cabinets Safeルイヴィトン時計コピー国内発送
I read this post fully regarding the resemblance oflatest and preceding technologies, it’s remarkable article.
vardenafil generic names – canadian pharmacy scam dr oz erectile dysfunction pills
This is one awesome blog article.Really thank you! Cool.
Once again another great entry. I actually have a few things to ask you, would be have some time to answer them?
i really liked this article. Thanks so much for sharing it. Really cool stuff and you have a new fan.
Hi, this weekend is pleasant designed for me, as thispoint in time i am reading this wonderful educational piece of writing here atmy residence.
Really no matter if someone doesn’t be aware of then itsup to other users that they will assist, so here it occurs.sla 3d printer resin wholesale flexible resin wholesale
Thanks again for the article post.Really looking forward to read more. Much obliged.
With thanks, A good amount of info!college essay writers block essays writer custom of writing letters
Aw, this was a really good post. Spending some time and actual effort to create a really good article… but what can Isay… I procrastinate a lot and never manage to get nearly anything done.
That is a great tip particularly to those new to the blogosphere. Brief but very precise infoÖ Appreciate your sharing this one. A must read post!
Awesome blog post.Much thanks again. Really Great.
Fantastic post.Never knew this, appreciate it for letting me know.Feel free to surf to my blog dis-count.de
Thank you ever so for you blog post. Awesome.
eagle ridge apartments rentberry scam ico 30m$ raised garden hill apartments
She used her own hair in the soup to give it additional taste.
What’s Happening i’m new to this, I stumbled upon this I have discovered It positively useful and it has helped me out loads. I’m hoping to give a contribution & aid different customers like its helped me. Good job.
What a information of un-ambiguity and preserveness of valuableknowledge concerning unpredicted feelings.
Hello my friend! I want to say that this article is amazing, nice written and include almost all important infos. I would like to see more posts like this.
Thanks for another excellent post. Where else could anyone get that kind of information in such an ideal way of writing? I’ve a presentation next week, and I am on the look for such info.
This is one awesome article.Much thanks again. Awesome.
Fantastic post.Really thank you! Fantastic.
Thanks for sharing, this is a fantastic article post.Really thank you! Fantastic.
Really appreciate you sharing this post.Really looking forward to read more. Really Great.
Thank you ever so for you blog.Really looking forward to read more. Awesome.
Really enjoyed this article.Really looking forward to read more. Cool.
Im obliged for the article post.Really looking forward to read more. Much obliged.
Hello.This article was really motivating, particularly since I was searching for thoughts on this matter last Tuesday.
Hi, this weekend is good designed for me, for the reason that this time i am reading this wonderful informative post here at my residence.
Heya i’m for the first time here. I found this board and I to find Ittruly helpful & it helped me out a lot. I am hoping to provide onething again and help others such as you aided me.
Thanks-a-mundo for the blog article.Thanks Again. Awesome.
Wow! Finally I got a blog from where I know how to actuallyget valuable data concerning my study and knowledge.
This article was awesome Thanks a lot for writing it. You have a fan in me. Talk soon.
Thanks again for the article post.Thanks Again. Great.
It’s arduous to seek out educated people on this subject, but you sound like you understand what you’re talking about! Thanks
sudden discontinuation of lisinopril hydrochlorothiazide diuretics
Everyone loves what you guys tend to be up too.This type of clever work and reporting! Keep up the superb works guysI’ve you guys to my blogroll.
I am so grateful for your blog post.Really thank you! Much obliged.
I enjoy what you guys are usually up too. Such clever work and coverage!Keep up the good works guys I’ve added you guys to my blogroll.
Thanks-a-mundo for the blog. Awesome.
slots for real money slots for real money free slots
This post provides clear idea designed for the new users ofblogging, that really how to do running a blog.
371739 141213Yeah bookmaking this wasnt a bad decision excellent post! . 126371
I will immediately grab your rss feed as I can not in finding your email subscription hyperlink or e-newsletter service. Do you’ve any? Please permit me recognise in order that I may subscribe. Thanks.
I like the valuable information you provide in your articles. I will bookmark your blog and check again here frequently. I am quite certain I will learn many new stuff right here! Best of luck for the next!
Thank you for your blog article. Want more.
I am so grateful for your blog post.Much thanks again. Awesome.
Very neat post.Thanks Again. Want more.
Major thanks for the article post.Really looking forward to read more. Keep writing.
Great artical, had no problems printing this page either.
Trouve par sigmoidoscopie a sonde rigide, le rectum mesures entre 10 cm et 15 cm a partir du bord de l’anus.
The winning ticket was sold at the Publix supermarket on North Nebraska Avenue in Lutz, Florida, whichis just north of Tampa, according to the Florida lottery.
Very neat article post.Much thanks again. Cool.
I like reading an article that will make men and women think.Also, many thanks for allowing for me to comment!
Thanks-a-mundo for the article.Much thanks again. Cool.
When I originally commented I clicked the “Notify me when new comments are added” checkbox and now each timea comment is added I get four emails with the same comment.Is there any way you can remove people from that service?Appreciate it!
Very good article.Much thanks again. Keep writing.
canadian pharmacy scam erectile dysfunction medications – best canadian pharmacythe pharmacy
Thanks in favor of sharing such a pleasant idea, piece of writing is fastidious, thats whyi have read it completely
There is noticeably a lot of money to understand about this. I assume you’ve made certain nice points in features also.
Enjoyed every bit of your blog article. Want more.
You mentioned it fantastically. write my essay good movies to write essays on
It’s really a great and useful piece of information. I’m satisfied that you shared this useful information with us. Please keep us informed like this. Thank you for sharing.
wow, awesome post.Much thanks again.
apartments in farmington nm apartments laredo tx apartments for rent in clifton nj
stardust apartments apartments in rowlett tx emory apartments
Incredible! This blog looks just like my old one! It’s on a completely different subject butit has pretty much the same layout and design. Superbchoice of colors!
Many thanks. Excellent stuff.i hate writing essays dissertation writers online i need help writing a personal statement
Very neat article post.Much thanks again. Awesome.
Ahaa, its nice dialogue regarding this paragraph at this place at this blog,I have read all that, so at this time me also commenting at thisplace.
Remarkable things here. I am very glad to peer your post.Thanks a lot and I am looking forward to touch you. Will you kindly drop me amail?Also visit my blog :: Perfume inspired melts
I cannot thank you enough for the blog. Cool.
I appreciate you sharing this post.Thanks Again. Awesome.
This is my first time visit at here and i am truly impressed to readeverthing at one place.
Thanks a lot for the blog.Thanks Again. Awesome.
Really appreciate you sharing this blog post.Really thank you! Really Cool.
Enjoyed every bit of your article.Thanks Again.
At this moment I am going to do my breakfast, afterward having my breakfast comingyet again to read other news.
Thanks a lot for the blog. Cool.
Looking forward to reading more. Great article. Much obliged.
Really enjoyed this article post.Really looking forward to read more. Really Great.
Fantastic blog post.Really looking forward to read more. Want more.
I really like reading through an article that will make people think. Also, thanks for allowing for me to comment!
Major thankies for the blog article.
Thanks for the article, is there any way I can get an alert email when you publish a fresh update?
A big thank you for your post.Really looking forward to read more. Want more.
Hi! I just wanted to ask if you ever have any trouble with hackers? My last blog (wordpress) was hacked and I ended up losing several weeks of hard work due to no back up. Do you have any methods to prevent hackers?
Im obliged for the blog.Really looking forward to read more. Will read on…
Fantastic blog article.Thanks Again. Will read on…
When some one searches for his necessary thing, thereforehe/she needs to be available that in detail, thereforethat thing is maintained over here.
Say, you got a nice article.Much thanks again. Really Great.
Im obliged for the article.Much thanks again. Awesome.
Really informative article.Really thank you! Will read on…
I am so grateful for your article.Really looking forward to read more. Will read on…
Thanks-a-mundo for the blog article.Really thank you!
Major thankies for the article.Thanks Again. Really Cool.
I really enjoy the article post.Really thank you! Much obliged.
wonderful points altogether, you just received a new reader. What might you recommend in regards to your submit that you simply made a few days ago? Any certain?
Thank you for your blog post.Really looking forward to read more. Fantastic.
I am so grateful for your blog post.Really thank you! Cool.
you have brought up a very fantastic points , thankyou for the post.
Thanks for the blog article.Really looking forward to read more. Really Great.
Really appreciate you sharing this blog post. Will read on…
I loved your article post. Awesome.
I loved your blog. Awesome.
I really liked your blog article. Great.
Great, thanks for sharing this article.Thanks Again. Fantastic.
This is nicely expressed. .how to write a nonfiction essay online college homework help phd writer
A big thank you for your blog.Much thanks again. Great.
I value the blog.Really looking forward to read more. Fantastic.
Appreciate you sharing, great blog.Much thanks again. Great.
I think this is a real great post.Thanks Again. Great.
Thanks so much for the article.Really looking forward to read more. Cool.
Awesome blog post.Much thanks again. Cool.
I truly appreciate this article.Really thank you! Cool.
Really enjoyed this article. Much obliged.
I have гead so many content about the blogger lovers however this paragraph is in faⅽt a faѕtidious рost, keep it up.
I’m really enjoying the design and layout of your blog.It’s a very easy on the eyes which makes it much more pleasant for me tocome here and visit more often. Did you hire out a developer to create your theme?Superb work!
xenical fda label – xenical reviews orlistat does it work
It is really a great and helpful piece of information. I am glad that you shared this helpful information with us. Please keep us informed like this. Thanks for sharing.
I will right away clutch your rss as I can not to find your email subscription hyperlink or newsletter service. Do you have any? Please let me understand so that I may subscribe. Thanks.
Very good post.Thanks Again. Great.
stromectol south africa ivermectin for humans – ivermectin tablets
fluconazole medication for men fluconazole treatment for onychomycosis fluconazole side effects dog
Great blog post.Really thank you! Really Cool.
I really enjoy the article post.Much thanks again. Cool.
Great article post.Much thanks again.
Enjoyed every bit of your article post. Fantastic.
Appreciate you sharing, great blog.Really looking forward to read more. Fantastic.
I think this is a real great article post.Really thank you!
Im obliged for the post. Really Cool.
Hey, thanks for the post. Really Cool.
Im obliged for the post.Thanks Again. Really Great.
Wow, great post.Really thank you! Awesome.
I value the blog.Really thank you! Great.
Very neat blog post.Really thank you! Much obliged.
Thanks so much for the article.Thanks Again. Will read on…
Thank you ever so for you blog post.Really looking forward to read more. Will read on…
Im obliged for the article.Much thanks again. Really Great.
I appreciate you sharing this post.Really thank you! Great.
Major thankies for the blog article.Much thanks again. Really Cool.
wow, awesome blog.Really looking forward to read more. Awesome.
Really enjoyed this article.Much thanks again. Much obliged.
Looking forward to reading more. Great article.Thanks Again. Great.
Muchos Gracias for your blog.Really looking forward to read more. Really Cool.
Very neat post.Really thank you! Really Cool.
Looking forward to reading more. Great article post.Really thank you! Really Great.
Really appreciate you sharing this blog post. Really Cool.
Really appreciate you sharing this post.
I appreciate you sharing this blog article. Awesome.
Thanks for sharing, this is a fantastic blog article. Fantastic.
Thanks for sharing, this is a fantastic blog post.Really looking forward to read more. Much obliged.
Im thankful for the article post.Thanks Again.
I really liked your blog.Really looking forward to read more. Want more.
Hi! Do you use Twitter? I’d like to follow you if that would be okay. I’m definitely enjoying your blog and look forward to new posts.
п»їprilosec can you take tums with prilosec
I’m not sure exactly why but this blog is loading incredibly slow for me.Is anyone else having this issue or is it a issue on my end?I’ll check back later on and see if the problem still exists.
Very neat article post.Much thanks again. Awesome.
I agree with your opinion. From now on I will always support you.
Itís hard to find educated people for this subject, however, you sound like you know what youíre talking about! Thanks
I like the valuable info you provide in your articles. I’ll bookmark your blog and checkagain here frequently. I’m quite certain I will learn a lotof new stuff right here! Best of luck for the next!
you’ve got an incredible blog right here! would you wish to make some invite posts on my blog?
Thank you for your article.Really looking forward to read more. Keep writing.
Pretty nice post. I just stumbled upon your blog and wished to say that I have truly enjoyed browsing your blog posts.After all I will be subscribing to your rss feed and I hope you writeagain very soon!
A motivating discussion is definitely worth comment. There’s no doubt that that you should write more about this subject, it may not be a taboo matter but usually folks don’t speak about these topics. To the next! All the best!!
Truly when someone doesn’t be aware of afterward its up to other viewers that they will help,so here it occurs.
I value the blog.Really thank you! Want more.
Thanks for one’s marvelous posting! I definitely enjoyed reading it, youare a great author.I will ensure that I bookmark your blog and willcome back in the future. I want to encourage youto ultimately continue your great job, have a nice afternoon!
I am so grateful for your article post.Really looking forward to read more. Awesome.
Really appreciate you sharing this blog post. Awesome.
At this time it seems like BlogEngine is the top blogging platform available right now. (from what I’ve read) Is that what you are using on your blog?
Thanks a lot for the blog post.Really thank you! Great.
to play alone rather than sharing is simply a SaaS which means
I think this is a real great article post.Really thank you! Cool.
Great, thanks for sharing this article post. Will read on…
I really like looking through an article that will make men and women think.Also, thank you for allowing me to comment!
excellent issues altogether, you simply received a new reader. What could you recommend about your put up that you made some days ago? Any sure?
Thanks for sharing, this is a fantastic blog post.Much thanks again. Will read on…
Thanks again for the article.Thanks Again. Fantastic.
Major thankies for the blog article.Really looking forward to read more. Want more.
Really appreciate you sharing this article post.Really looking forward to read more. Much obliged.
Thanks for the blog.Really looking forward to read more. Will read on…
Hey, you used to write excellent, but the last several posts have been kinda boring… I miss your tremendous writings. Past several posts are just a little bit out of track! come on!
Say, you got a nice blog post. Really Cool.
I’m no longer positive the place you’re getting your info, however great topic.I must spend some time learning more or understanding more.Thank you for excellent info I used to be looking for this information for my mission.
Hi there, just became alert to your blog through Google, and found that itis truly informative. I’m gonna watch out for brussels.I’ll be grateful if you continue this in future. Alot of people will be benefited from your writing.Cheers!
Hi! Do you use Twitter? I’d like to follow you if that would be okay. I’m undoubtedly enjoying your blog and look forward to new updates.
Vortex BioShield® EMF protectors are designed to shield the body from harmful radiation by acting as a natural neutralizing device via the technology that it is attached to.
You could certainly see your skills in the work you write. The world hopes for more passionate writers like you who are not afraid to say how they believe. Always go after your heart.
Heya i am for the first time here. I came across this board and I find It really useful & it helped me out much. I hope to give something back and help others like you aided me.
finasteride medication side effects for finasteride what is finasteride]
Enjoyed every bit of your article post.Much thanks again. Keep writing.
This blog is definitely interesting and also diverting. I have picked a bunch of useful tips out of this blog. I ad love to go back again and again. Thanks!
When I initially commented I clicked the “Notify me when new comments are added” checkboxand now each time a comment is added I get several e-mails with the same comment.Is there any way you can remove me from that service? Thanks!
wow, awesome article post.Really looking forward to read more. Cool.
Great, thanks for sharing this blog article. Much obliged.
Im obliged for the blog post.Much thanks again. Fantastic.
Thanks-a-mundo for the blog post.Really thank you! Cool.
I really like and appreciate your blog article.Thanks Again.
You mentioned this superbly.essay 123 help who can help me write an essay top cv writing services
how much is generic plaquenil hydroxychloroquine – plaquenil from canada
errectile disfunction pump for ed – ed medications list
This is one awesome article.Really thank you! Really Cool.
Wow, great article post. Want more.
Thank you for your blog.Really thank you! Want more.
Thanks again for the post. Fantastic.
Great, thanks for sharing this blog article.Thanks Again. Keep writing.
Through reinstallation, in the event you’re askedto enter a product vital,Free License Key – Get a Free Activation Code –Serial Keylicense key
An interesting discussion is definitely worth comment. I do think that you should publish more about this topic, it might not be a taboo subject but usually people do not talk about these topics. To the next! Kind regards!
Thanks so much for the article post.Much thanks again. Really Great.
is lisinopril an ace inhibitor losartan hydrochlorothiazide recall
UFABET เว็บพนันบอลออนไลน์ ที่ได้รับความนิยมที่มีคนที่ใช้งานเยอะที่สุดตอนนี้ ด้วยเหตุว่าเราเป็นลำดับแรกๆประเด็นการบริการ แล้วก็ ความยั่งยืนและมั่นคงทางด้านการเงิน แถมมี คาสิโนออนไลน์ไว้ให้บริการทั้งยัง สล็อต บาคาร่า รวมถึง เกมออนไลน์อีกมากมาย
side effects for hydroxychloroquine chloroquine primaquine hydroxychloroquine sulfate uses
When I originally commented I clicked the « Notify me when new comments are added » checkbox and now each time a comment is added I get three emails with the same comment. Is there any way you can remove me from that service? Thanks!
To be minimalism is one of the best rolex datejust replica design idea.
Special Delivery levothyroxine bodybuilding She added that, U.S. “churches aren’t their own.” She also said that the family had issues with being forced to “pay these taxes that pay for abortions we don’t agree with.”
I appreciate you sharing this blog article.Thanks Again. Much obliged.
Major thanks for the article.Much thanks again. Great.
naltrexone oral dosing naltrexone medication class oral naltrexone alcoholism
This is a good tip especially to those fresh to theblogosphere. Simple but very precise information… Appreciate your sharingthis one. A must read post! 0mniartist asmr
Thanks again for the article.Really thank you! Really Cool.
whoah this blog is great i love studying your posts.Stay up the great work! You understand, lots of individuals are hunting around for this information, youcould aid them greatly.
Hi my friend! I want to say that this post is awesome, great written and include almost all important infos. I would like to look extra posts like this .
I am so grateful for your post.Really looking forward to read more. Fantastic.
Thanks for the post.Much thanks again. Want more.
This is one awesome article.Much thanks again. Keep writing.
Very informative article post.Really thank you! Much obliged.
Hey! This post could not be written any better!Reading through this post reminds me of my old room mate!He always kept chatting about this. I will forward thisarticle to him. Pretty sure he will have a good read. Many thanks for sharing!
Thanks for sharing, this is a fantastic blog.Really thank you! Cool.
Kalbos vartojimo uduotys. Lietuvi kalbos pratimai auktesniosioms klasms Gimtasis odis
I am so grateful for your blog.Much thanks again. Fantastic.
advantages over the other and but with the PlayStation 4,
I needed to thank you for this wonderful read!! I certainly enjoyed every little bit of it. I have got you saved as a favorite to look at new stuff you postÖ
Wonderful post but I was wondering if you could write a litte moreon this subject? I’d be very thankful if you could elaborate a little bit further.Kudos!
Major thankies for the article.Really thank you! Awesome.
Thanks again for the blog article.Much thanks again. Cool.
scoliosisHello my friend! I want to say that this post is awesome, great written and come with approximately all vital infos.I’d like to see more posts like this . scoliosis
I am so grateful for your blog article.Thanks Again. Want more.
purchase essay online – academic writing paper writing online
I think this is a real great blog post.Really thank you! Really Cool.
Im thankful for the blog article. Will read on…
I appreciate you sharing this post.Much thanks again. Great.
Fantastic article post.Much thanks again. Awesome.
Awesome! Its in fact amazing article, I have got much clear idea about fromthis article.Have a look at my blog post – Keto Smooth
Howdy! This post couldn’t be written any better! Reading this post reminds me of my previous room mate! He always kept talking about this. I will forward this article to him. Pretty sure he will have a good read. Thank you for sharing!
I loved your article post.Much thanks again. Will read on…
This can be so wonderfully open-handed of you supplying quickly precisely what a volume
Very nice post. I simply stumbled upon your blog and wanted to mention that I’ve really enjoyed surfing around your blog posts. In any case I’ll be subscribing in your rss feed and I’m hoping you write once more very soon!
can hydroxychloroquine be purchased over the counter chloroquine hcl
Im thankful for the blog article.Much thanks again. Cool.
Im obliged for the article.Really looking forward to read more. Fantastic.
Some really superb info , Sword lily I found this.press release
Im thankful for the blog article.Really thank you! Much obliged.
tractor supply ivermectin pour on how long after taking ivermectin can you drink alcohol
Really appreciate you sharing this blog.Much thanks again. Fantastic.
There is apparently a lot to identify about this. I think you made some nice points in features also.
Wow, great article post.Really thank you! Really Cool.
I don’t even know how I finished up here, but I believed this put up was once great. I do not know who you’re however definitely you are going to a well-known blogger in case you aren’t already. Cheers!
I appreciate you sharing this post.
Enjoyed every bit of your article.Really looking forward to read more. Awesome.
Really informative article post.Much thanks again. Really Cool.
Thanks so much for the article post. Great.
Awesome blog article. Fantastic.
wow, awesome article post.Really looking forward to read more. Want more.
Major thanks for the blog.Much thanks again. Really Great.
History billiga kamagra Another birdie followed in unexpected fashion at the par-four 13th where he chipped in from an uphill lie in thick rough below the green, his ball popping up before tracking toward the cup some 40 feet away.
I have not checked in here for a while because I thought it was getting boring, but the last few posts are good quality so I guess I¡¦ll add you back to my daily bloglist. You deserve it my friend 🙂
Major thankies for the blog post.Thanks Again. Much obliged.
Piece of writing writing is also a fun, if you be familiarwith after that you can write if not it is complicatedto write.
how to write a persuasive essayhow to write an introduction paragraph for an essayessay creator
Oh my goodness! an amazing article dude. Thank you Nevertheless I am experiencing concern with ur rss . Don’t know why Unable to subscribe to it. Is there anybody getting equivalent rss problem? Anybody who is aware of kindly respond. Thnkx
I like looking through a post that can make people think. Also, thank you for allowing for me to comment!
Thẳng Soccer Thời Điểm Hôm Nay, Links Xem đá Bóng Trực Tuyến 24h keo nhà caiĐội tuyển chọn Việt Nam chỉ cần thiết một kết quả hòa có bàn thắng để lần loại hai góp mặt trên World Cup futsal. Nhưng, để thực hiện được điều này
modalert online provigil – provigil for sale
Hello, you used to write wonderful, but the last few posts have been kinda boring… I miss your tremendous writings. Past several posts are just a bit out of track! come on!
I really like and appreciate your post. Really Cool.
Thank you, I’ve recently been searching for info about this subject for ages and yours is the best I’ve came upon till now. But, what concerning the bottom line? Are you positive in regards to the source?
Great blog you’ve got here.. It’s difficult to find good quality writing like yours nowadays. I seriously appreciate individuals like you! Take care!!
A round of applause for your post.Really thank you! Really Great.
I do consider all of the concepts you’ve introduced for your post. They’re very convincing and can certainly work. Nonetheless, the posts are very short for starters. May you please extend them a little from subsequent time? Thanks for the post.
Very neat article. Cool.
wonderful points altogether, you simply gained a logo new reader. What might you recommend about your publish that you simply made some days ago? Any positive?
I am sure this piece of writing has touchedall the internet users, its really really fastidious post on building up new blog.
Major thankies for the blog post.Much thanks again. Really Great.
Great, thanks for sharing this article post. Much obliged.
Very informative article.Really thank you! Will read on…
Amazing! Its truly remarkable piece of writing, I have got much clear idea concerning from this piece of writing.
Really informative blog article.Really thank you!
Very good article post.Thanks Again. Cool.
writing essays help write my paper for me
It’s wonderful that you are getting thoughts from this piece of writing as well as from our dialogue made here.
Thanks-a-mundo for the blog post.Much thanks again. Keep writing.
Major thanks for the blog article. Will read on…
This is one awesome blog.Thanks Again. Cool.
Thanks again for the blog.Really thank you! Want more.
Great, thanks for sharing this article post.Really looking forward to read more. Much obliged.
Thank you for your blog post.Really thank you! Awesome.
Thanks-a-mundo for the blog post.Thanks Again. Keep writing.
wow, awesome blog post.Really looking forward to read more. Much obliged.
Wow, great article. Really Great.
Thank you ever so for you blog.Really looking forward to read more. Awesome.
Aw, this was an exceptionally good post. Finding the time and actual effort to produce a superb article… but what can I say…I hesitate a lot and never seem to get nearly anything done.
I don’t even understand how I finished up right here, but I assumed this publish used to be great.I don’t know who you are however definitely you’re going to a well-known blogger in case you arenot already. Cheers!my blog – Hentai
This is one awesome blog article.Really looking forward to read more. Cool.
The betting odds will develop progressively longer till you reach the rank outsider.
Great blog you’ve got here.. Itís hard to find good quality writing like yours these days. I really appreciate people like you! Take care!!
Hey! Do you know if they make any plugins to safeguard against hackers? I’m kinda paranoid about losing everything I’ve worked hard on. Any recommendations?
I value the blog.Much thanks again. Much obliged.
Incredible! This blog looks just like my old one! It’s on a entirely different subject but it has pretty much the same layout and design. Excellent choice of colors!
Hello, this weekend is pleasant for me, since this moment i am reading this impressive educational article hereat my home.
Everyone loves what you guys are up too. Such clever work and reporting! Keep up the awesome works guys I’ve incorporated you guys to my personal blogroll.
Thanks for another wonderful article. Where else may anybody get that type of info in such a perfect means of writing? I have a presentation next week, and I’m on the search for such info.
plaquenil pill hydroxychloroquine for covid
Thanks for sharing such a nice thinking, paragraph isnice, thats why i have read it fully
An intriguing discussion is worth comment. I think that you need to publish more about this topic, it might not be a taboo subject but usually people don’t discuss these topics. To the next! Many thanks!!
This text is invaluable. How can I find out more?
Thanks-a-mundo for the article.Much thanks again. Will read on…
Excellent blog you have got here.. It’s difficult to find high-quality writing like yours nowadays. I seriously appreciate people like you! Take care!!
ivermectin cream reviews stromectol scabies
hello!,I love your writing so so much! share we be in contactextra approximately your post on AOL? I need an expert on this area to resolve my problem.Maybe that’s you! Having a look ahead tosee you.
Incredible story there. What occurred after?Good luck!
Great blog post.Really looking forward to read more. Really Great.
Excellent read, I just passed this onto a friend who was doing a little research on that. And he actually bought me lunch since I found it for him smile Thus let me rephrase that: Thank you for lunch!
Aw, this was an extremely nice post. Taking a few minutes and actual effort to make a superb article… but what can I say… I put things off a whole lot and don’t seem to get nearly anything done.
Great blog you have here.. It’s hard to find good quality writing likeyours nowadays. I honestly appreciate people like you! Take care!!
194560 482294I believe your suggestion would be helpful for me. I will let you know if its work for me too. Thank you for sharing this beautiful articles. thanks a good deal 369384
Just what I was looking for, regards for putting up.
Thanks , I’ve just been looking for information about this topic for a while and yours isthe best I’ve found out so far. But, what concerning theconclusion? Are you sure about the source?
Thank you for your article.Really looking forward to read more. Want more.
Living here in England, I are often asked by people from the US about my favourite places to visit in Europe.
That is a good tip especially to those fresh to the blogosphere. Brief but very accurate information… Many thanks for sharing this one. A must read post!
whole thing without having side effect , people could take a signal.
Very neat article post.Really thank you! Will read on…
Really appreciate you sharing this article.Really looking forward to read more. Awesome.
I think this is a real great article post. Really Great.
This is a really good tip especially to those new to the blogosphere. Brief but very precise information?Thank you for sharing this one. A must read post!
Appreciate you sharing, great post.Really looking forward to read more. Much obliged.
Before each soccer match, make sure you take the time to do some pregame warm-ups and stretching.
how long does it take ivermectin to work how can i get ivermectin
Hello.This post was really interesting, especially because I was searching for thoughts on this issue last Sunday.
Hey, thanks for the blog.Really looking forward to read more. Great.
wow, awesome blog. Really Cool.
Very good blog.Thanks Again. Keep writing.
Major thankies for the blog article. Will read on…
Thanks so much for the blog article.Really looking forward to read more. Keep writing.
Thanks for the article post.Thanks Again.
Im obliged for the blog post.Thanks Again. Really Cool.
Appreciate you sharing, great blog post.Really thank you! Much obliged.
Great post.Much thanks again. Want more.
Major thanks for the article post.Much thanks again. Will read on…
w88This allows kids to observe ideas that buns be helpful in future age victimisation their highly-creative vision.
I really liked your blog article. Want more.
how to use tinder , tinder logintinder date
I appreciate you sharing this post.Much thanks again. Really Cool.
No matter if some one searches for his necessary thing, thus he/shewishes to be available that in detail, thus that thing is maintained over here.
Once your blog is more established, this list will be used to bring in money, and you will be thankful that you already took care of this.
Looking forward to reading more. Great blog.Much thanks again. Awesome.
Great article post.Really looking forward to read more. Want more.
A big thank you for your blog post.Much thanks again. Want more.
Looking forward to reading more. Great post.Really thank you!
Im thankful for the blog post.Much thanks again. Really Cool.
A big thank you for your post.Much thanks again. Really Great.
Thanks for sharing, this is a fantastic blog.Thanks Again. Awesome.
Major thanks for the blog.Really looking forward to read more. Awesome.
Thanks for the blog. Will read on…
This paragraph offers clear idea designed for the new people of blogging, that actually how to dorunning a blog.
Hello There. I found your blog using msn. That is an extremely well written article. I will be sure to bookmark it and come back to learn more of your helpful info. Thank you for the post. I’ll certainly comeback.
I wanted to thank you for this good read!! I certainly enjoyed every bit of it. I have got you book-marked to look at new things you post…
An intriguing discussion is worth comment. I thinkthat you need to write more about this issue, it might not be a taboo matter but typically people don’t speak about such subjects.To the next! Cheers!!
There is clearly a bunch to identify about this. I consider you made certain nice points in features also.My blog :: Vernita
Outstanding story there. What occurred after?Thanks!
hello!,I really like your writing very a lot! share we keep up a correspondence more about your post on AOL? I require an expert in this area to resolve my problem. May be that is you! Looking forward to look you.
about this since the very However, if you like to mod
You could certainly see your skills within the work you write. The sector hopes for even more passionate writers like you who aren’t afraid to say how they believe. Always follow your heart.
When someone writes an post he/she keeps the plan ofa user in his/her brain that how a user can be aware ofit. Thus that’s why this piece of writing is amazing. Thanks!
Thanks for sharing your thoughts. I truly appreciate your efforts and Iwill be waiting for your next write ups thank you once again.
It as wonderful that you are getting thoughts from this paragraph as well as from our dialogue made here.
I do not even know the way I finished up right here, however I assumed this publish was good.I do not recognise who you might be but certainly you’re going to awell-known blogger for those who are not already. Cheers!
Some really great info , Gladiolus I detected this. „Desire creates the power.” by Raymond Holliwell.
dissertation topics in education best dissertation writing services
This is one awesome blog article.Much thanks again. Much obliged.Loading…
Awesome post.Thanks Again. Keep writing.
There’s certainly a lot to know about this topic. I really like all of the points you’ve made.
wow, awesome blog article.Much thanks again. Really Great.
Hi there, of course this piece of writing is truly good and I have learned lot of things from it regarding blogging. thanks.
WOW just what I was searching for. Came here by searchingfor 앤젤레스 아리아나가 그녀와 함께 영화를 찍는 방법
it is really informative. I am gonna be careful
paying someone to write a paper writing an essay essay typer generator
Hi, after reading this remarkable paragraph i am as well happy to share my experience here with friends.
These are in fact great ideas in about blogging.You have touched some fastidious factors here. Any way keep up wrinting.
Thanks a lot for the blog.Really thank you! Will read on…
You can subscribe for a month, account, and it comes with the
Enjoyed every bit of your post.Thanks Again. Fantastic.
Your mode of describing the whole thing in this paragraphis really good, every one be capable of effortlessly knowit, Thanks a lot.
Hmm is anyone else encountering problems with the pictures on this blog loading? I’m trying to figure out if its a problem on my end or if it’s the blog. Any suggestions would be greatly appreciated.
Thanks a lot for the blog post.Much thanks again. Really Cool.
Thank you for creating this article. You do an awesome job with your blog. You made a fan in me.
There is certainly a great deal to learn about this topic. I really like all the points you’ve made.
Say, you got a nice blog.Much thanks again. Cool.
Normally I do not learn post on blogs, however I would liketo say that this write-up very forced me to check out and do it!Your writing style has been amazed me. Thanks, very nice post.
I like the valuable information you provide in your articles. I’ll bookmark your blog and check again here regularly. I am quite certain I’ll learn many new stuff right here! Best of luck for the next!
I’m very happy to read this. This is the kind of manual that needs to be given and not the accidental misinformation that is at the other blogs. Appreciate your sharing this best doc.
Hey There. I discovered your blog using msn. This is a really neatly written article.I will be sure to bookmark it and return to read more of your usefulinfo. Thank you for the post. I’ll definitely comeback.
Hi there! I’m at work browsing your blog from my new iphone 3gs! Just wanted to say I love reading through your blog and look forward to all your posts! Keep up the great work!
I am extremely impressed along with your writing talents and also with the layout to yourblog. Is this a paid subject or did you modify it yourself?Anyway keep up the nice high quality writing, it’s rare to peer a great blog like this one nowadays..
Thanks , I’ve recently been looking for info approximatelythis topic for a long time and yours is the best I’ve came upon till now.However, what about the bottom line? Are you sure concerning thesource?
You really deserve a big kiss right now. You are a very persuasive writer. What’s best will often be a little different for each person involved. Interesting content.
Asking questions are actually fastidious thing if you are not understanding something completely, except thisarticle provides nice understanding yet.
the shell to her ear and screamed. There was a hermit
Thank you for your post.Really looking forward to read more. Cool.
Fantastic material. Appreciate it. lisinopril
Good way of explaining, and good article to take data about my presentation topic, which i am going to convey in college.
generic prednisone for sale prednisone generic – prednisone pills for sale
Great, thanks for sharing this article. Awesome.
I delight in examining by means of an article which can make Guys and girls Consider. Also, thanks for permitting me to remark!
Muchos Gracias for your post. Much obliged.
Think about investments that provide fast annuities.
It’s aсtᥙallʏ a great and uѕeful piece of info.I am satiѕfied that you just shared this helpful info ith us.Please syay us informed like this. Thankѕ for sharing.
Say, you got a nice blog.Really thank you! Keep writing.
I really enjoy the blog post.Thanks Again. Cool.
Thank you for any other informative blog. The place else may I get that type of information written in such a perfect manner? I’ve a challenge that I’m simply now working on, and I have been on the glance out for such information.
Elimine las molestias, la máquina de publicación a plazos HP ENVY 6000 facilita la publicación
I truly appreciate this blog.Really thank you! Keep writing.
It as actually a great and useful piece of information. I am satisfied that you shared this useful tidbit with us. Please keep us informed like this. Thank you for sharing.
Major thankies for the article post.Really looking forward to read more. Keep writing.
Enjoyed every bit of your blog.Really thank you! Fantastic.
Aw, this was a really good post. Finding the time and actual effort to create a really goodarticle… but what can I say… I procrastinate a lot and don’t manage to get anything done.0mniartist asmr
Just wanna tell that this is invaluable, Thanks for taking your time to write this.
Hello There. I found your blog using msn. This is a very well written article. I?ll make sure to bookmark it and return to read more of your useful info. Thanks for the post. I?ll certainly return.
Excellent blog you’ve got here.. It’s difficult to find excellent writing like yours nowadays. I truly appreciate individuals like you! Take care!!
hydroxychloroquine pills ncov chloroquine
Too many blog writers nowadays yet just a few have posts worth spending time on reviewing.
Hi colleagues, pleasant paragraph and nice urging commented at this place, I am trulyenjoying by these.
State legislators viewed as this to basically ban all games of possibility andtypes of gambling.
When I initially commented I clicked the «Notify me when new comments are added» checkbox andnow each time a comment is added I get three e-mails with the same comment.Is there any way you can remove people from that service?Appreciate it!
I am not sure where you are getting your information, but great topic. I needs to spend some time learning much more or understanding more. Thanks for fantastic info I was looking for this info for my mission.
Superb post however , I was wondering if you could write a litte more on this subject?I’d be very thankful if you could elaborate alittle bit more. Appreciate it!
Very good article.Really thank you! Fantastic.
I cannot thank you enough for the blog.Much thanks again. Really Great.
These are actually wonderful ideas in about blogging. You havetouched some nice factors here. Any way keep up wrinting.
You need to take part in a contest for one of the greatest blogs online. I will highly recommend this blog!
tamoxifen citrate dosage tamoxifen mann tamoxifen dose mice
I cannot thank you enough for the blog.Really thank you! Awesome.
Very good article.Much thanks again. Will read on…
Really appreciate you sharing this article.Thanks Again.
Another thing I’ve noticed is that often for many people, bad credit is the consequence of circumstances beyond their control. One example is they may be actually saddled with illness and as a consequence they have higher bills for collections. Maybe it’s due to a employment loss or even the inability to work. Sometimes separation and divorce can send the finances in the undesired direction. Thanks sharing your ideas on this web site.
Major thanks for the article post.Much thanks again. Great.
The primary care in Franklin is exceptional. I feel assured knowing my wellbeing is in such experienced hands. Choosing this clinic was the best decision for my wellbeing.
Wow, great article. Cool.
I cannot thank you enough for the blog post.Really looking forward to read more. Awesome.
This distribution scheme offers excellent value with expert management. Consistent yields, reliable income, and striking success.
Thanks for sharing, this is a fantastic blog article.Really looking forward to read more. Want more.
I appreciate you sharing this blog.Thanks Again. Keep writing.
I really liked your blog.Thanks Again.
What’s up mates, fastidious paragraph and pleasant arguments commented here,I am in fact enjoying by these.
Wow, great blog post.Thanks Again. Really Cool.
Verify Canterbury vs Otago 4th Match Videos, Reports Articles On the net.
I appreciate you sharing this blog post.Thanks Again. Want more.
Wow! This could be one particular of the most helpful blogs We’ve ever arrive across on this subject. Basically Fantastic. I am also an expert in this topic so I can understand your hard work.
Aw, this was an extremely nice post. Taking a few minutes and actual effort to generate a really good articleÖ but what can I sayÖ I procrastinate a lot and don’t seem to get anything done.
This is a wonderful website. The site owner has carried out a superb job of putting it together, the info here is really insightful.
Good article. I’m dealing with a few of these issues as well..
What’s up mates, how is all, and what you would liketo say regarding this piece of writing, in my view itsgenuinely remarkable in favor of me.
I value the article post. Cool.
At the same time, there is another side of the formation and organization ofthe utterance.
There’s definately a lot to learn about this subject. I love all of the points you’ve made.
What’s Going down i’m new to this, I stumbled upon this I have discovered It positively helpful and ithas aided me out loads. I hope to give a contribution & help otherusers like its aided me. Good job.
excellent issues altogether, you just received a new reader. What might you recommend about your post that you made some days ago? Any positive?
I do not even know the way I stopped up right here, however I thought this put up used to be good. I do not recognise who you are however definitely you’re going to a well-known blogger if you happen to are not already. Cheers!
Lovely blog! I am loving it!! Will come back again. I am taking your feeds also
I really appreciate this post. I¡¦ve been looking everywhere for this! Thank goodness I found it on Bing. You’ve made my day! Thx again
Hello! treatment for peripheral neuropathy in feet sources
Major thankies for the article.Thanks Again. Really Cool.
Major thanks for the article post.Really thank you! Keep writing.
Amazing things here. I’m very glad to look your article.Thanks a lot and I’m looking ahead to contact you.Will you kindly drop me a e-mail?
I value the post.Really looking forward to read more. Fantastic.
Thanks again for the article post. Cool.
Kaci Kusumoto says:This information is magnificent. Nice write up. Thumbs up! You appear to know a lot about this.Reply 07/21/2020 at 8:34 pm
I needed to thank you for this excellent read!! I definitely loved every little bit of it. I have you bookmarked to look at new things you postÖ
Very informative post.Much thanks again.
Asking questions are really pleasant thing if you are not understanding anything totally, but thisarticle offers good understanding yet.
Thanks for every other wonderful article. Where else may anybody get that kind of info in such a perfect approach of writing? I have a presentation next week, and I am at the search for such information.
Thanks for the article post.Really looking forward to read more. Fantastic.
A big thank you for your article.Really thank you! Will read on…
I am now not sure the place you’re getting your info,however great topic. I needs to spend a while studying more orfiguring out more. Thank you for great info I was on the lookoutfor this information for my mission.
clomiphene tablets: clomiphene tablets – clomiphene generic
Thanks for some other fantastic post. Where else could anybody get that kind of information in such an ideal meansof writing? I have a presentation next week,and I am at the look for such information.
Thanks so much for the article.Really looking forward to read more. Really Cool.
Looking forward to reading more. Great post.Thanks Again. Keep writing.
I really liked your blog post.Really thank you! Keep writing.
I think this is a real great article.Really looking forward to read more. Keep writing.
Heya i am for the first time here. I came across this board and I tofind It truly useful & it helped me out a lot.I’m hoping to give something again and aid others like you helped me.
Post writing is also a excitement, if you know afterthat you can write or else it is complex to write.
I really liked your article. Will read on…
Very interesting topic, appreciate it for posting. „The rest is silence.” by William Shakespeare.
Thanks a lot for the post.Really looking forward to read more. Fantastic.
Hi, I do think this is an excellent blog. I stumbledupon it 😉 I am going to revisit yet again since i have book-marked it. Money and freedom is the best way to change, may you be rich and continue to help others.
Major thankies for the blog post. Want more.
Aw, this was an exceptionally good post. Taking the time and actual effort to create a good article… but what can I say… I procrastinate a lot and don’t seem to get anything done.
No matter if some one searches for his essential thing, so he/she wants to be available that in detail, therefore that thing ismaintained over here.
I appreciate you sharing this article.Really thank you! Really Cool.
Hello my loved one! I wish to say that this post is awesome, nice written and include almost all significant infos. I’d like to peer extra posts like this .
The Spirit of the Lord is with them that fear him.
What a information of un-ambiguity and preserveness of valuablefamiliarity concerning unexpected feelings.
Hey there! I just wanted to ask if you ever have any trouble with hackers? My last blog (wordpress) was hacked and I ended up losing months of hard work due to no data backup. Do you have any solutions to prevent hackers?
I needed to thank you for this good read!! I absolutely enjoyed every little bit of it. I have you book marked to check out new things you postÖ
Thanks for a marvelous posting! I really enjoyed reading it, you willbe a great author.I will always bookmark your blog and will come back from nowon. I want to encourage that you continue your great job, havea nice evening!
It?s hard to locate well-informed individuals on this subject, but you seem like you understand what you?re discussing! Many thanks
Muchos Gracias for your blog.Really looking forward to read more. Will read on…
Appreciate you sharing, great article post.Thanks Again. Will read on…
Enjoyed every bit of your blog post.Really thank you! Much obliged.
Thanks-a-mundo for the article post.Really thank you! Great.
Im obliged for the blog article. Much obliged.
I haven¡¦t checked in here for a while since I thought it was getting boring, but the last several posts are good quality so I guess I will add you back to my everyday bloglist. You deserve it my friend 🙂
Loved your blog post. I will return to view more.
Fantastic article post. Really Great.
zoloft bipolar can you drink alcohol on zoloft
Hi, yes this article is really fastidious and I have learned lot of things from it concerning blogging.thanks.
… [Trackback][…] Here you can find 25471 additional Information to that Topic: bellepetitedesign.com/favorite-beauty-products-of-all-time/ […]
Really informative article. Will read on…
I appreciate you sharing this blog article. Great.
Muchos Gracias for your blog post.Much thanks again. Keep writing.
What’s up, just wanted to say, I loved this blog post. It was funny. Keep on posting!
Really appreciate you sharing this blog.Much thanks again. Really Cool.
Melisa Şenolsun Masumlar Apartmanı dizisinde hangi karaktere hayat verecek? Melisa Şenolsun kimdir, kaç yaşında?
I value the post.Thanks Again. Really Great.
Appreciate you sharing, great blog post.Much thanks again. Cool.
Hi there colleagues, pleasant piece of writing and fastidious arguments commented here, I am in fact enjoying by these.
I am so grateful for your blog post.Much thanks again. Awesome.
Great post. I am going through a few of these issues as well..
Great article post.Really thank you!
You could definitely see your expertise within the work you write. The sector hopes for more passionate writers like you who aren’t afraid to say how they believe. At all times follow your heart.
Major thanks for the blog post.Thanks Again. Cool.
Heya i’m for the first time here. I came across this board and I find It reallyhelpful & it helped me out much. I hope to offer something again and aid others such as youaided me. n (Cheryle)
Hello my friend! I want to say that this article is amazing, nice written and come with almost all vital infos. I would like to see more posts like this.
This post gives clear idea in support of the new viewers of blogging, that really how to do running a blog.
When I originally commented I clicked the “Notify me when new comments are added” checkbox and now each time a comment is added I get four emails with the same comment. Is there any way you can remove me from that service?
Hello, I enjoy reading through your article. I like to write alittle comment to support you.
Really no matter if someone doesn’t be aware of then its up toother viewers that they will assist, so here it occurs.
Say, you got a nice article post.Much thanks again.
I really liked your post.Much thanks again. Great.
Hey, thanks for the post.Much thanks again. Much obliged.
Say, you got a nice article.Really looking forward to read more. Cool.
Great blog post.Really thank you! Great.
Thanks for sharing, this is a fantastic blog article.Much thanks again. Awesome.
wow, awesome blog.Thanks Again. Want more.
Thanks so much for the article.Really thank you! Really Great.
Really enjoyed this blog post.Thanks Again. Great.
Thanks a lot for the article.Really thank you! Will read on…
A big thank you for your post. Great.
This is one awesome blog article.Thanks Again. Much obliged.
Hey! I just wanted to ask if you ever have any problems with hackers?My last blog (wordpress) was hacked and I ended up losing months of hard work dueto no back up. Do you have any methods to protect against hackers?
There’s noticeably a bundle to find out about this. I assume you made sure nice points in options also.
I appreciate you sharing this blog article.Really looking forward to read more. Really Cool.Loading…
Very interesting subject, thanks for putting up. «Wrinkles should merely indicate where smiles have been.» by Mark Twain.
Rzdzod – will you do my homework Zfmanw kqypey
Excellent blog you’ve got here.. It’s hard to find good quality writing like yours these days.I honestly appreciate people like you! Take care!!
Hello my family member! I want to say that this article is amazing, nice written and come with almost all significant infos. I’d like to see extra posts like this .
Aw, this was a very nice post. Spending some time and actual effort to generate a really good article… but what can I say… I hesitate a lot and never manage to get nearly anything done.
Isotretinoin With Next Day Delivery Cod Only
I don’t even know the way I stopped up right here, but I thought this publish used to be great. I don’t recognize who you are but definitely you are going to a famous blogger in case you aren’t already 😉 Cheers!
A motivating discussion is definitely worth comment. I believe that you ought to publish more about this subject, it may not be a taboo subject but generally folks don’t speak about such topics. To the next! Best wishes!!
ivermectin brand name ivermectin cream uk – generic ivermectin cream
Hi there, its nice post regarding media print, we all understand media is a wonderful source of data.
Greetings! Very helpful advice in this particular article! It is the little changes which will make the greatest changes. Thanks for sharing!
I enjoy reading an article that will make men and women think. Also, thanks for allowing me to comment!
I really enjoy the blog post.Really looking forward to read more. Keep writing.
I am no longer sure the place you are getting your info, but great topic.I needs to spend some time learning more or working out more.Thank you for wonderful info I was searching for this info for my mission.
bisoprolol classification ramipril classification furosemide medication
Wow, this paragraph is good, my sister is anlyzing such things, sso Iam going to inform her.
cbd oil side effects on kidneys cbd oil side effects stomach pain gas best cbd oil for pain for sale
Hi, I log on to your blogs daily. Your story-telling style is witty, keepup the good work!
I cannot thank you enough for the blog article.Thanks Again. Awesome.
Appreciate you sharing, great blog.
I like looking through a post that will make people think. Also, many thanks for allowing for me to comment!
Bardzo interesujące informacje! Idealnie to, czego szukałem! przenośny generator tlenu przenośny generator tlenu.
Normally I do not learn article on blogs, but I wish to say that this write-up very forced me to check out and do it! Your writing taste has been amazed me. Thanks, very nice article.
This is a really good tip especially to those new to the blogosphere. Simple but very accurate infoÖ Thanks for sharing this one. A must read post!
to write some content for your blog in exchange for a link back to
I enjoy reading through a post that can make people think. Also, many thanks for permitting me to comment!
furosemide over the counter rx furosemide nus tet
Really informative article post.Thanks Again.
Looking forward to reading more. Great blog.Thanks Again. Fantastic.
I value the post.Thanks Again. Will read on…
I value the blog article.Thanks Again.
Greetings! Very helpful advice on this article! It is the little changes that make the biggest changes. Thanks a lot for sharing!
I am so grateful for your blog.Thanks Again. Cool.
What’s up, always i used to check blog postshere early in the daylight, since i like to learn more and more.
Thank youu for the good writeup. It in fact was a amusement accountit. Loook advanced to more added agrreeable from you!By the way, how can we communicate?
Awesome blog post. Great.
You could definitely see your enthusiasm within the paintings you write.The sector hopes for even more passionate writers like you who are not afraid to sayhow they believe. Always go after your heart.My blog; Nuubu
Thank you for your article.Much thanks again. Will read on…
สล็อตออนไลน์เกมคาสิโนยอดฮิตชั่วกับชั่วกัลป์ เล่นง่าย แจ็คพอตแตกไวจำต้องที่ UFABET จ่ายจริง จ่ายเต็ม มีเกมให้เลือกเยอะมากทั้งยังพนันบอล บาคาร่า ยิงปลา มาเว็บนี้เว็บไซต์เดียวโคตรคุ้ม สร้างรายได้ง่ายจบที่เว็บ UFABET ได้เลยครับผม
ivermectin lotion for lice stromectol for sale – stromectol online
Muchos Gracias for your blog post.Much thanks again. Much obliged.
Thanks for the article post.Really looking forward to read more. Really Great.
I blog often and I really thank you for your content. This great article has truly peaked my interest. I will take a note of your blog and keep checking for new details about once per week. I subscribed to your Feed too.
Great blog article. Really Great.
I think this is a real great blog post.Really looking forward to read more. Want more.
I appreciate you sharing this post. Awesome.
Fantastic article.Thanks Again. Really Cool.
Enjoyed every bit of your blog.Thanks Again. Much obliged.
A big thank you for your blog. Great.
whoah this blog is excellent i like studying your articles.Stay up the great work! You understand, a lot of persons are looking around for this information, you can aid them greatly.
Lovely just what I was looking for. Thanks how to lose weight theauthor for taking his clock time on this one.
I am now not certain where you’re getting your information, however good topic. I needs to spend some time finding out more or understanding more. Thank you for magnificent info I was searching for this info for my mission.
Doѡnload MIDI Converter Studio to a rercognized location.
Appreciate you sharing, great article post. Great.
Thanks-a-mundo for the blog article.Really thank you! Want more.
Thanks for the good writeup. It in fact was once a amusement account it. Glance advanced to far brought agreeable from you! However, how could we keep up a correspondence?
I am so grateful for your blog.Much thanks again. Really Cool.
Thank you for the good writeup. It in fact used to be a enjoyment account it. Look advanced to far brought agreeable from you! However, how can we keep up a correspondence?
I really enjoy the post.Thanks Again. Fantastic.
Awesome things here. I am very glad to see your article.Thank you so much and I am looking ahead to contact you.Will you kindly drop me a e-mail?สล็อต
Really informative blog article.Really looking forward to read more. Really Great.
Really enjoyed this post.Much thanks again. Keep writing.
A fascinating discussion is definitely worth comment. I do believe that you ought to write more about this topic, it might not be a taboo subject but typically folks don’t talk about these topics. To the next! Kind regards!!
An interesting discussion is definitely worth comment. I believe that you need to write more on this subject matter, it may not be a taboo matter but generally folks don’t discuss these issues. To the next! All the best!!
Hey there! I know this is somewhat off topic but I was wondering if you knew where I could get a captcha plugin for my comment form? I’m using the same blog platform as yours and I’m having difficulty finding one? Thanks a lot!
Really informative article. Really Cool.
excellent points altogether, you simply gained a new reader. What would you recommend about your put up that you simply made a few days ago? Any sure?
This piece of content was awesome Thanks a lot for making it. You have a fan in me. Talk soon.
Really appreciate you sharing this blog.Really thank you! Great.
I blog quite often and I really thank you for your information. The article has truly peaked my interest. I’m going to bookmark your blog and keep checking for new information about once a week. I subscribed to your Feed too.
overseas pharmacies shipping to usa: online indian pharmacies generic pills india
and that would end up being some really want to raise awareness
Major thankies for the blog.Thanks Again. Cool.
I cannot thank you enough for the blog article.Much thanks again. Will read on…
Muchos Gracias for your blog post.Much thanks again. Fantastic.
Very neat blog post.Thanks Again. Much obliged.
Hey, thanks for the blog article.Really looking forward to read more. Great.
It’s going to be ending of mine day, however before ending I am reading thiswonderful post to increase my knowledge.
Hello my family member! I want to say that this post is awesome, nice written and come with approximately all important infos. I’d like to look more posts like this . otertbe.se/map18.php positivt Г¤l test gravid
Your mode of describing the whole thing in this piece of writing is in fact nice, every one be capable of effortlessly understand it, Thanks a lot.
เกมส์ใหม่ ค่ายPG 💥เกมส์ ใหม่มาแรง แจ็คพอตแตกหนักๆโบนัสเกมส์ รางวัลใหญ่ แตกกระจาย!!!เล่นง่าย ได้จริง จ่ายจริง ปลอดภัย 100📲ฝาก-ถอน ไม่มีขั้นต่ำ 😘
Hey! Do you know if they make any plugins to help with SEO? I’m trying to get my blog to rank for some targeted keywords but I’m not seeing very good results. If you know of any please share. Appreciate it!
Fantastic blog article. Keep writing.
generic allegra 7253 allegra medication – benadryl 44329
I wanted to thank you for this wonderful read!! I certainly enjoyed every bit of it. I have got you book-marked to look at new things you post…
Great, thanks for sharing this blog post.Really looking forward to read more.
Thanks , I have just been looking for info approximately this topic for a long time and yours is the greatest I’ve found out so far. However, what in regards to the conclusion? Are you certain concerning the source?
avery park apartments rentberry scam ico 30m$ raised apartment treadmill
ivermectin otc ivermectin over the counter – ivermectin
wow, awesome blog article.Thanks Again. Want more.
I value the post.Really looking forward to read more. Want more.
I really liked your blog post.Really looking forward to read more. Cool.
Very informative blog post.Much thanks again. Fantastic.
Great blog article.Thanks Again. Really Cool.
I am so grateful for your article post.Much thanks again. Fantastic.
A round of applause for your post.Really thank you! Awesome.
This is one awesome article post.Really looking forward to read more. Want more.
Im obliged for the blog post.Thanks Again.
I was able to find good info from your articles.my blog post :: mpc-install.com
doxycycline generic doxycycline for sale – doxycycline hyc
Hey, you used to write magnificent, but the last few posts have been kinda boringK I miss your super writings. Past several posts are just a bit out of track! come on!
I really like and appreciate your post. Really Great.
It’s enormous that you are getting ideas from this post as wellas from our argument made here.
A big thank you for your blog.Thanks Again.
Thanks for the good writeup. It in fact used to be a leisure account it. Look complicated to more delivered agreeable from you! However, how could we keep up a correspondence?
hello!,I really like your writing very a lot! percentage we keep up a correspondence extra about your post on AOL?I require an expert on this space to resolve my problem. Maybethat’s you! Taking a look ahead to look you.
ivermectin injectable for cattle topical ivermectin for rosacea
A round of applause for your article post.Really thank you! Really Cool.
Was ist neu für mich, ich bin über das hier gestolpert Ich habe es unbedingt entdeckt und es hat mir sehr geholfen. Ich hoffe, einen Beitrag zu leisten & zu helfen. andere Kunden wie sein unterstütztes Ich. Guter Job.
I really like and appreciate your blog article.Really looking forward to read more. Keep writing.
Thank you ever so for you blog article.Really looking forward to read more. Will read on
Las 20 mejores cámaras de reparto de conocidos de la actualidad, han cambiado un pequeño
Precisely what I was looking for, appreciate it for putting up.Here is my blog Sound Joy Earbuds Review
Amazing forum posts. Thanks a lot. canadian pharmacy online
Heya! I just wanted to ask if you ever have any issues with hackers? My last blog (wordpress) was hacked and I ended up losing many months of hard work due to no back up. Do you have any solutions to stop hackers?
Nice post. I was checking constantly this blogand I am impressed! Extremely helpful info specifically the last part 🙂I care for such info much. I was looking for this particular info for a long time.Thank you and best of luck.My blog :: diet plan
Thanks for sharing your thoughts about on. Regards
An interesting discussion is definitely worth comment. There’s no doubt that that you need to publish more about this subject, it might not be a taboo subject but usually people don’t discuss these issues. To the next! All the best!!
It’s actually a nice and useful piece of information. I’m glad that you shared this helpful info with us. Please keep us up to date like this. Thanks for sharing.
What a material of un-ambiguity and preserveness of precious experience concerning unexpected feelings.
Im obliged for the article.Thanks Again. Keep writing.
Wow that was unusual. I just wrote an really long comment but after I clicked submit my comment didn’t show up. Grrrr… well I’m not writing all that over again. Anyway, just wanted to say wonderful blog!
I really liked your blog.Much thanks again. Want more.
online canadian pharmacy reviews – best rated canadian pharmacy canadian pharmacy reviews
That is a really good tip especially to those fresh to the blogosphere. Simple but very accurate infoÖ Appreciate your sharing this one. A must read article!
desoxyn online pharmacy methadone online pharmacy
I like the helpful information you provide in your articles.I’ll bookmark your blog and check again here regularly. I’m quite sureI will learn many new stuff right here! Best of luck for the next!
Truly quite a lot of terrific advice!write my essay reviews thesis paper best writing services online
There is definately a great deal to know about this subject. I love all the points you’ve made.
Really appreciate you sharing this blog post.Thanks Again. Really Great.
erectile dysfunction medicine – best ed treatment ed medications
Wow! This could be one particular of the most beneficial blogs We’ve ever arrive across on this subject. Actually Fantastic. I am also an expert in this topic therefore I can understand your effort.
i love action movies and my idol is none other than Gerard Butler. this guy really rocks*
ivermectin for chickens ivermectin for coronavirus mayo clinic
provigil side effects provigil pill provigil medication
Very neat article post.Much thanks again. Will read on…
I am glad that it turned out so well and I hope it will continue in the .future because it is so worthwhile and meaningful to the community.a disability is an example of what type of factor
It’s hard to come by educated people about this subject, but you seem like you knowwhat you’re talking about! Thanks
meloxicam high risk strengths of meloxicam meloxicam dose pig
I found so many interesting stuff in your blog especially its discussion. From the tons of comments on your articles, I guess I am not the only one having all the enjoyment here! keep up the good work.
It is in point of fact a great and useful piece of info. I am satisfied that you just shared this helpful information with us. Please stay us informed like this. Thanks for sharing.
What’s up friends, its enormous post on the topic of tutoringand completely explained,keep it up all the time.
Hi there! Do you use Twitter? I’d like to follow you if that would beok. I’m absolutely enjoying your blog and look forward to new posts.
Awesome blog post.Much thanks again. Keep writing.
ล็อตออนไลน์ มือถือ นั้นมีธีมให้เลือกหลากหลาย นักพนันอาจจะเลือกไม่ถูกก็ลองหาอ่านจากรีวิว เล่นสล็อตออนไลน์ ให้ได้เงิน ดูก่อนว่าธีมไหนคนเล่นเยอะ และอาจจะได้เจอกับเทคนิคใหม่ ๆ ที่เหล่านักพนันมืออาชีพนำมาแชร์ เรื่องจริง
When someone writes an post he/she keeps the thought of a user in his/her mind that how a user can understand it. Thus that’s why this post is great. Thanks!
tri amoxicillin500g amoxicillinamoxicillin online pharmacy uk Unfak Drulk
what is tinder , tinder apphow to use tinder
edit my paper – paper writer how to write a hiring letter
northwest canada pharmacy online pharmacy delivery usa
how does chloroquine work hydroxychloroquine online chloroquine tablet
chloroquine phosphate aralen aralen phosphate – chloroquine for sale
Usually I don’t read post on blogs, but I would like to say that this write-up very pressured me to take a look at and do so! Your writing style has been surprised me. Thanks, very nice article.
Generally I don’t read post on blogs, but I wish to say that this write-up very forced me to try and do it! Your writing style has been surprised me. Thanks, quite nice article.
trusted online pharmacy – ed pills canadian pharmacy no rx needed or pharmacy home delivery
Enjoyed reading through this, very good stuff,appreciate it.
Excellent way of describing, and pleasant paragraph to getdata on the topic of my presentation subject,which i am going to present in school.
I?¦ll right away grab your rss feed as I can not to find your e-mail subscription hyperlink or e-newsletter service. Do you have any? Kindly permit me understand in order that I may subscribe. Thanks.
Hi there mates, how is everything, and what you desire to sayconcerning this piece of writing, in my view its actually amazing in favor of me.
slots online slots online free online slots
Just wanna state that this is handy, Thanks fortaking your time to write this.my blog; mois system
I do accept as true with all the concepts you have presented on your post.They are really convincing and can certainly work.Still, the posts are too short for beginners.May you please lengthen them a bit from subsequent time? Thank you for the post.
ed meds indian pharmacies without an rx – ways to treat erectile dysfunction
It’s actually a great and useful piece ofinfo. I am glad that you just shared this useful info with us.Please stay us up to date like this. Thank you for sharing.Feel free to visit my blog post :: Green Flame CBD Gummies
The only thing I lament is not having found your blog before.
Hello! I know this is somewhat off topic but I was wondering if you knew where I could find a captcha plugin for my comment form? I’m using the same blog platform as yours and I’m having trouble finding one? Thanks a lot!
Piece of writing writing is also a fun, if you know then youcan write if not it is complex to write.
I’m really impressed with your writing skillsas well as with the layout on your blog. Is this apaid theme or did you modify it yourself? Either way keep up the nice quality writing, it’srare to see a great blog like this one these days.
Nice post. I used to be checking constantly this blog and I’m inspired! Extremely helpful info specifically the closing section 🙂 I maintain such information much. I was seeking this certain info for a very long time. Thank you and good luck.
Very informative article.Much thanks again. Much obliged.
It’s going to be finish of mine day, but before end I am reading this wonderful piece of writing to improve my know-how.
Wow that was unusual. I just wrote an very long comment but after I clicked submit mycomment didn’t appear. Grrrr… well I’m not writing all that over again. Anyway, just wanted to say great blog!
Great information. Lucky me I ran across your blog by chance (stumbleupon).I have bookmarked it for later!
It’s exhausting to find educated people on this matter, however you sound like you know what you’re speaking about! Thanks
chloroquine walmart fda hydroxychloroquine dosage for hydroxychloroquine
Thanks , I’ve just been looking for info about this subject for a long time and yours is the greatest I have found out till now.But, what about the bottom line? Are you certain about the source?
It’s fantastic that you are getting thoughts from this piece of writing as well as from ourargument made at this time.
Thank you for the auspicious writeup. It in reality used to be a amusement account it.Glance complicated to far introduced agreeable from you!By the way, how can we keep in touch?
Hey there! I could have sworn I’ve been to this blog before but after reading through some of the post I realized it’s new to me. Anyways, I’m definitely delighted I found it and I’ll be bookmarking and checking back frequently!
Say, you got a nice blog.Really looking forward to read more. Want more.
Trực Tiếp Bóng Đá Hôm Nay, Link Xem Soccer Trực Tuyến 24h 777.com.vnĐội tuyển futsal nước Việt Nam đã được một trận đấu đồng ý được trước đối thủ đầy sức mạnh Lebanon. Kết trái Bà Rịa-Vũng Tàu vs Bình Phước hôm nay 18h00 ngày 5/5, Hạng nhất nước ta.
triamterene hydrochlorothiazide lisinopril/hctz dosage
Exceptional post however I was wondering if you could write a litte more on this topic? I’d be very thankful if you could elaborate a little bit more. Thank you!
texas state board of pharmacy ed medications rx pharmacy
hello brother, I follow you closely, first of all, thank you for accepting my comment, I wish you continued success.!!Loading…
hello!,I love your writing so so much! percentage we be in contact more approximately your post on AOL? I need an expert in this area to solve my problem. May be that’s you! Having a look forward to peer you.
As a Newbie, I am alwaays browwsing online for articles that can be of assistance to me.Thank you
In the event you don’t have a printer or don’t want to acquire a singleFree Coupons – Get Free Coupon Online – Store Shipping Couponfree coupons
Thank you for sharing your thoughts. I truly appreciate your efforts and I am waiting for your further post thanks once again.
Hi there! I could have sworn I’ve been to this blog before but after browsing through some of the post I realized it’s new to me. Nonetheless, I’m definitely glad I found it and I’ll be bookmarking and checking back often!
Good info. Lucky me I recently found your blog by chance (stumbleupon).I’ve book marked it for later!
Looking forward to reading more. Great article post. Much obliged.
How do you do? custom serevent electron cutout Facing difficult weather conditions, they aretrying to take the vessel to an Italian port.
I’ll right away grasp your rss feed as I can’t in finding your email subscription link or e-newsletter service. Do you’ve any? Please let me recognise so that I could subscribe. Thanks.
Hi there to all, for the reason that I am actually keen of reading this blog’s post to be updatedon a regular basis. It includes nice information.
Whoa quite a lot of useful facts!help me with my essayresume writing service
Hello there! I could have sworn I’ve been to this blog before but after looking at a few of the posts I realized it’s new to me. Anyhow, I’m definitely delighted I stumbled upon it and I’ll be book-marking it and checking back regularly.
Pretty nice post. i want to sleep just stumbled upon your blog and wanted to say that I’ve truly enjoyed surfing around your blog posts.After all I’ll be subscribing to your rss feed and I hope you write again soon!
Thanks , I’ve just been looking for info about this topic for a long time and yours is the best I have came upon till now. But, what in regards to the conclusion? Are you certain in regards to the supply?
Amazing! Its really amazing post, I have got much clear idea regarding from this article.
I quite like looking through an article that will make people think. Also, thank you for allowing me to comment!
Hi my friend! I want to say that this post is amazing, nice written and include almost all important infos.I would like to peer more posts like this .
I need to to thank you for this excellent read!! I absolutely enjoyed every little bit of it. I’ve got you saved as a favorite to look at new stuff you postÖ
Howdy! Do you know if they make any plugins to safeguard against hackers?I’m kinda paranoid about losing everything I’ve worked hard on.Any recommendations?
numerous editions of PlayStation, tik tok free followers hack
Thank you for your article post.Thanks Again. Fantastic.
I really enjoy the blog article.Much thanks again. Keep writing.
Hey, thanks for the blog.Much thanks again. Want more.
Appreciate you sharing, great post. Really Great.
I appreciate you sharing this blog post.Much thanks again.
Really enjoyed this article.Thanks Again. Awesome.
Major thanks for the article.Much thanks again. Fantastic.
Thank you ever so for you article post.Much thanks again. Fantastic.
Really appreciate you sharing this blog post. Want more.
Thank you for your post.Thanks Again. Keep writing.
Muchos Gracias for your post.Much thanks again. Really Great.
Enjoyed every bit of your blog article.Really thank you! Keep writing.
Enjoyed every bit of your article post. Want more.
I like the valuable info you supply for your articles.I’ll bookmark your blog and take a look at once more hereregularly. I’m relatively certain I will be told plenty ofnew stuff proper here! Good luck for the following!
Normally I don’t learn article on blogs, however I would like to say that this write-up very pressured me to take a look at and do it! Your writing taste has been amazed me. Thank you, very nice article.
I always spent my half an hour to read this blog’s articles daily along with a mug of coffee.
Very neat blog post.Really looking forward to read more. Cool.
Very nice layout and wonderful subject material , nothing else we need : D.
Hi my family member! I wish to say that this post is amazing, nice written and come with approximately all vital infos. I’d like to peer more posts like this.
I need to to thank you for this excellent read!! I definitelyloved every bit of it. I’ve got you bookmarked to check out new things you post…
replica rolex design is actually serious、 useful not really substantial fancy.
Thanks a lot for the blog article.
It챠s hard to come by knowledgeable people in this particular topic, however, you seem like you know what you챠re talking about! Thanks
Academic essay writers custom law essays custom admission essay
pharmacy store online pharmacy without insurance
I really like your article. It’s evident that you have a lot knowledge on this topic. Your points are well made and relatable. Thanks for writing engaging and interesting material.a disability may be present in which of the following
Generally I don’t read post on blogs, but I wish to say that this write-up very forced me to try and do it! Your writing style has been amazed me. Thanks, quite nice post.
I personally at the same time were dealing with some an identical trouble for just a few Christmas the seasons up to the point When i got a few important guidelines derived from one of connected with my fellows.
Very informative blog post.Really thank you!
tyLY0F Just a smiling visitant here to share the love (:, btw outstanding style.
It’s going to be end of mine day, but before ending I am reading thisimpressive paragraph to increase my experience.
There is definately a lot to find out about this subject.I love all of the points you’ve made.
I like the valuable info you provide in your articles. I’ll bookmark your blog and check again here frequently. I’m quite certain I will learn lots of new stuff right here! Good luck for the next!
chloroquine primaquine side effects for hydroxychloroquine
It’s impressive that you are getting ideas from thisarticle as well as from our dialogue made at this place.
ed meds: male erectile pills best male erectile dysfunction pill
ivermectin 250ml ivermectin bestellen ivermectin and covid
Good day! I simply would like to give you a big thumbs up for the excellent information you have here on this post. I’ll be returning to your blog for more soon.
An additional issue is that video games are generally serious anyway with the major f토토ocus on understanding rather than amusement.
Fantastic blog article. Really Great.
Hello my friend! I wish to say that this post is awesome,great written and include almost all important infos. I would like to peer extra posts like this .
Heya! I just wanted to ask if you ever have any issues with hackers?My last blog (wordpress) was hacked and I ended up losing manymonths of hard work due to no data backup. Do you have anysolutions to stop hackers?
I love looking through a post that will make men and women think. Also, many thanks for allowing for me to comment!
Well I really liked reading it. This article provided by you is very constructive for proper planning.
wow, awesome blog article. Will read on…
I dont even know how I ended up here, but I thought this post was great. I don’t know who you are but certainly you are going to a famous blogger if you aren’t already 😉 Cheers!
Very well written information. It will be valuable to anybody who usess it, including myself. Keep doing what you are doing – i will definitely read more posts.
I don’t even know how I ended up here, but I thought this post wasgreat. I don’t know who you are but definitely you’re goingto a famous blogger if you aren’t already 😉 Cheers!
I do believe all of the ideas you’ve offered for your post. They are very convincing and will definitely work. Still, the posts are too quick for novices. May just you please extend them a bit from next time? Thanks for the post.
There’s certainly a lot to find out about this subject. I really like all of the points you have made.
Hello! I’ve been reading your blog for a long time now andfinally got the courage to go ahead and give you ashout out from Houston Tx! Just wanted to say keep up the fantastic job!
Hi there, its nice paragraph regarding media print, we all know media is a great source ofinformation.
This is one awesome post.Really thank you! Want more.
Howdy! Do you use Twitter? I’d like to follow youif that would be ok. I’m absolutely enjoying your blog and look forward to new updates.
No one tells you find out how to touch upon blogs.
edgewater village apartments doral view apartments
Good day! Would you mind if I share your blog with my twitter group? There’s a lot of folks that I think would really appreciate your content. Please let me know. Many thanks
ivermectin rosacea reddit ivermectin tractor supply
I loved your post.Really looking forward to read more. Really Great.
I will right away grab your rss as I can’t find your email subscription link or newsletter service. Do you have any? Please let me know in order that I could subscribe. Thanks.
Thanks, I ave recently been looking for info about this subject for a while and yours is the greatest I ave found out so far. However, what concerning the bottom line? Are you sure about the source?
Thanks for the post, can I set it up so I receive an update sent in an email when you write a fresh update?
I enjoy what you guys are usually up too. This sort of clever work and exposure! Keep up the excellent works guys I’ve included you guys to my blogroll.
Muchos Gracias for your article.Thanks Again. Fantastic.
I read this piece of writing fully concerning the resemblance of newest and previous technologies, it’s awesome article.
Hi my family member! I wish to say that this article is awesome, nice written and come with approximately all important infos. I would like to see extra posts like this.
Is anyone here in a position to recommend Bare Essentials? Thanks x
Thanks a lot for the blog post.Really looking forward to read more. Much obliged.
ucqgmocqg fkdrx ltzodxu wyhm jnbyvnaqjmqhzjc
I enjoy, cause I discovered just what I used to be looking for. You have ended my 4 day lengthy hunt! God Bless you man. Have a great day. Bye
Hello there, just became alert to your blog through Google, and found that it’s truly informative. I am gonna watch out for brussels. I will be grateful if you continue this in future. A lot of people will be benefited from your writing. Cheers!
Well I sincerely enjoyed studying it. This post provided by you is very constructive for accurate planning.
Thanks for sharing your thoughts. I really appreciate your efforts and I am waiting foryour further write ups thank you once again.
This piece of writing provides clear idea in support of thenew people of blogging, that genuinely how to do blogging.
Really appreciate you sharing this blog.Much thanks again. Cool.
Hi there, its fastidious piece of writing about media print, we all be aware of mediais a impressive source of information.
Great blog post! I’ll be back to see your next piece! Thank you!
There is visibly a bunch to realize about this. I believe you made certain good points in features also.
There is clearly a bunch to realize about this. I assume you made certain good points in features also.
I want to to thank you for this fantastic read!! I definitely loved every bit of it. I’ve got you book-marked to check out new things you postÖ
Thanks for every other magnificent article. Where else may anybody get that kind of info in such an ideal manner of writing?I’ve a presentation subsequent week, and I’m on the look for such information.
Muchos Gracias for your post.Much thanks again. Awesome.
I read this article completely concerning the difference of most recent and preceding technologies, it’s amazing article.
stromectol for pinworms nih approved ivermectin
Hello, this weekend is fastidious in favor of me, as this moment i am reading this enormous educational article here at my house.
Heya i am for the first time here. I found this board and Ifind It really useful & it helped me out a lot. I hope to give something back and aid others like you aidedme.
play slots online slots online slot games
Very good blog article.Thanks Again. Really Great.
And the jobs I saw right here do not seem to show up on other job search engines.
Enjoyed looking at this, very good stuff, thankyou . „It is in justice that the ordering of society is centered.” by Aristotle.
Hello! I just wanted to ask if you ever have any trouble withhackers? My last blog (wordpress) was hacked and I ended up losing many months of hard workdue to no backup. Do you have any methods to protect against hackers?
sildenafil at walmart sildenafil side effect
You have very nice post and pictures, please have a look at our photo toursin the temples of Angkorinstapaper.com
Outstanding post however I was wondering if you could write a litte more on this subject?I’d be very grateful if you could elaborate a little bit further.Cheers!
Health to the hands of the person who made the application, it works smoothly ????
Explore char tex’s board “Hairstyles to Try” on Pinterest. See more ideas about short hair styles, hair cuts, hair styles.
Thank you ever so for you article. Want more.
This is one awesome article post. Cool.
A round of applause for your blog post.Thanks Again.
A round of applause for your post.Really thank you! Keep writing.
Really appreciate you sharing this post.Really looking forward to read more. Will read on…
Great, thanks for sharing this blog post. Will read on…
I think this is a real great article post.Much thanks again. Cool.
I am so grateful for your article.Really looking forward to read more. Want more.
Appreciate you sharing, great post.Really thank you! Cool.
I value the article.Thanks Again. Much obliged.
I really enjoy the blog post.
Thanks so much for the post.Much thanks again. Keep writing.
Im obliged for the blog article.Really looking forward to read more. Fantastic.
Thank you for your article post.Really thank you! Really Great.
Major thankies for the blog post.Much thanks again. Will read on…
I truly appreciate this blog.Much thanks again. Great.
Major thankies for the blog article.Really looking forward to read more. Really Cool.
This is one awesome blog.Much thanks again. Keep writing.
A round of applause for your post.Really thank you! Will read on…
Thanks so much for the article post.Thanks Again.
ivermectin 6 ivermectin gel – ivermectin human
Awesome blog article.Much thanks again. Keep writing.
Hi there! This is my first visit to your blog! We are a collection of volunteers and starting a new initiative in a community in the same niche.Your blog provided us valuable information to work on. You have done a extraordinary job!
Terrific post but I was wondering if you could write a litte more on this subject? I’d be very grateful if you could elaborate a little bit further. Many thanks!
Aw, this was an extremely nice post. Taking a few minutes and actual effort to produce a really good articleÖ but what can I sayÖ I hesitate a lot and never seem to get anything done.
Major thanks for the article.Thanks Again. Cool.
Aw, this was an exceptionally nice post. Taking a few minutes and actual effort to produce a very good articleÖ but what can I sayÖ I put things off a lot and don’t seem to get nearly anything done.
Thanks for the good writeup. It actually was a enjoyment account it. Glance advanced to more brought agreeable from you! However, how can we be in contact?
This blog was… how do I say it? Relevant!! Finally I have found something that helped me. Thanks!
I think this is a real great article.Much thanks again. Want more.
I will right away take hold of your rss feed as I can’t in finding your email subscription link or e-newsletter service. Do you’ve any? Kindly allow me recognise so that I may just subscribe. Thanks.
Thanks on your marvelous posting! I seriously enjoyed reading it,you are a great author. I will be sure to bookmark your blog and definitely will comeback from now on. I want to encourage one to continue your great work, havea nice morning!
Heya i am for the first time here. I found this board and I find Ittruly useful & it helped me out much. I’m hoping to offer one thing back and aid others suchas you aided me.
I am not positive where you are getting your info, but great topic.I must spend some time learning much more or figuring out more.Thank you for wonderful info I was searching for this information natural treatment for eczema my mission.
That is a very good tip particularly to those new to the blogosphere. Simple but very accurate infoÖ Thank you for sharing this one. A must read article!
Im thankful for the post.Really looking forward to read more. Great.
Highly descriptive post, I loved that a lot. Willthere be a part 2?
Hey, thanks for the article. Really Great.
I like the valuable material presented in your short articles.
I like the valuable info you provide on your articles. I will bookmark your blog and check once more here frequently. I’m somewhat sure I will be informed plenty of new stuff right here! Best of luck for the following!
Really enjoyed this blog post.Really looking forward to read more. Great.
I like the valuable info you provide in your articles. I’ll bookmark your blog and check again here regularly.I am quite certain I’ll learn lots of new stuff right here!Good luck for the next!
Aw, this was an exceptionally nice post. Taking a few minutes and actual effort to make a good article… butwhat can I say… I hesitate a whole lot and nevermanage to get nearly anything done.
Im grateful for the blog post.Much thanks again. Really Cool.
Say, you got a nice blog article.Really thank you!
Very good article.Really thank you! Cool.
This is one awesome article.Thanks Again. Great.
wow, awesome blog. Keep writing.
Very informative post. Really Great.
Really informative blog post.Thanks Again. Really Great.
Major thanks for the article post.Really thank you! Keep writing.
Exceptional post however I was wanting to know if you could write a litte more on this topic?I’d be very thankful if you could elaborate alittle bit further. Appreciate it!
Aw, this was a very good post. Spending some time and actual effort to make a good article… but what can I say… I procrastinate a lot and never seem to get anything done.
This is one awesome blog post.Much thanks again. Awesome.
Excellent post. I was checking constantly this blog and I’m impressed! Extremely helpful info specifically the last part 🙂 I care for such info much. I was seeking this certain info for a long time. Thank you and best of luck.
It’s truly a great and helpful piece of info.I am happy that you just shared this helpful info with us.Please stay us informed like this. Thanks for sharing.
Thanks so much for the article.
PSN code. Obviously, if you get who likes to enjoy a game from
389507 303217This really is an excellent write-up and I totally understand where your coming from inside the third section. Perfect read, Ill regularly follow the other reads. 68481
This blog was… how do I say it? Relevant!! Finally I have found something thathelped me. Thanks a lot!
dissertation help online personal essay essay writer auto essay typer
Muchos Gracias for your article post. Fantastic.
Im grateful for the blog article.Thanks Again. Great.
Im grateful for the blog article.Thanks Again. Keep writing.
Really informative article.Really thank you! Awesome.
I really like and appreciate your post. Cool.
Wow, great article.Really thank you! Fantastic.
Hey, thanks for the article.Really thank you! Cool.
Fantastic post.
Looking forward to reading more. Great article.Thanks Again. Awesome.
Thanks-a-mundo for the blog article.Really looking forward to read more. Fantastic.
Thanks so much for the blog.Really thank you! Awesome.
Thanks for the article.Much thanks again. Awesome.
This is one awesome blog article.Thanks Again. Keep writing.
Wow, great article post. Keep writing.
Thank you for your blog.Thanks Again. Awesome.
Attractive element of content. I simply stumbled upon your blog and in accession capital to say that I acquirein fact enjoyed account your blog posts. Any way I’ll be subscribing on your feeds and even I achievementyou access consistently quickly.
These are actually enormous ideas in concerning blogging.You have touched some good things here. Any way keep up wrinting.my blog post: Compoise 360X CBD Reviews
I’m now not sure the place you are getting your information, however goodtopic. I needs to spend some time learning more orfiguring out more. Thank you for magnificentinformation I was searching for this infofor my mission.
Wonderful info, With thanks!writing a good essay for college thesis editing custom writing service
I’m extremely impressed with your writing skills as well as with the layout on your blog. Is this a paid theme or did you modify it yourself? Either way keep up the excellent quality writing, it is rare to see a nice blog like this one today.
magic mushrooms[…]Wonderful story, reckoned we could combine several unrelated information, nonetheless genuinely worth taking a look, whoa did one understand about Mid East has got extra problerms too […]
ivermectin paste for scabies ivermectin injectable for cattle
They might be either affordable or expensive (but solar sections are certainly worth considering) based on your requirements
Nicely put, Many thanks.essay on help dissertation defintion pay for writing
I need to to thank you for this very good read!! I absolutely loved every bit of it. I’ve got you book-marked to check out new things you postÖ
slots games free slots for real money slots games free
There’s noticeably a bundle to know about this. I assume you made sure good points in options also.
An intriguing discussion is definitely worth comment. I think that you should write more about this subject, it might not be a taboo subject but generally people don’t discuss these issues. To the next! Best wishes!!
how often can you take prilosec does omeprazole cause gas
each timje i used tto reaad smaller articles which also clear their motive, andthat is also happening with this pieece of wriiting which I am reading at thisplace.
Receive a sister or brother?La OSEM concluyo su temporada 138 en Tlalnepantla
Very neat post.Really looking forward to read more. Much obliged.
pay for essay writing uk – expert essay writers how to write an about me essay
I like what you guys tend to be up too. This kind of clever work and coverage!Keep up the amazing works guys I’ve included you guys to my personal blogroll.
Normally I don’t learn article on blogs, however I would like to say that this write-up very forced me to take a look at and do so! Your writing taste has been surprised me. Thank you, very great article.
Hi there, I enjoy reading through your article. I wanted to write a little commentto support you.
Hey, you used to write wonderful, but the last several posts have been kinda boring?K I miss your great writings. Past several posts are just a little bit out of track! come on!
I cannot thank you enough for the blog.Much thanks again. Much obliged.
Looking forward to reading more. Great blog article.Thanks Again.
I value the article post.Really thank you! Want more.
Great, thanks for sharing this blog post.Really thank you!
Thanks for the blog article.Really looking forward to read more. Really Great.
Say, you got a nice blog article.Much thanks again. Really Cool.
Fantastic post.Really thank you!
Say, you got a nice article post.Much thanks again. Really Cool.
Looking forward to reading more. Great blog post.Thanks Again.
Thanks-a-mundo for the post.Thanks Again. Really Great.
It’s an awesome piece of writing in favor of all the online users; they will getbenefit from it I am sure.
Thanks so much for the article.Really thank you! Want more.
Hey just wanted to give you a quick heads up and let you know a few of the pictures aren’t loadingcorrectly. I’m not sure why but I think its a linking issue.I’ve tried it in two different internet browsersand both show the same results.
Currently it appears like BlogEngine is the preferred blogging platform available right now. (from what I’ve read) Is that what you’re using on your blog?
Hey there! I just want to offer you a big thumbs up for your excellent information you’ve got here on this post. I’ll be returning to your blog for more soon.
Im obliged for the blog post.Much thanks again. Want more.
Wonderful blog! I found it while surfing around on Yahoo News. Do you have any tips on how to get listed in Yahoo News? I’ve been trying for a while but I never seem to get there! Appreciate it
It’s enormous that you are getting ideas from this postas well as from our discussion made at thistime.
Great, thanks for sharing this post. Much obliged.
Muchos Gracias for your blog article.Much thanks again. Cool.
I am so grateful for your article.
Really informative blog post.Really thank you! Really Great.
wow, awesome blog article.Much thanks again. Really Great.
Your method of describing the whole thing in this article is trulygood, all be capable of effortlessly be aware of it,Thanks a lot.
lasix furosemide generic lasix – generic lasix
Hello.This article was really fascinating, particularly because I was searching for thoughts on this subject last Monday.
Fantastic post.Thanks Again.
And in co, you may develop some superior suppression forms that. clomid purchase Hpmooj omcxxv
Nice write up. I enjoyed your post. Thank you. This information is magnificent. I have been looking everywhere for this!
I believe you have noted some very interesting points,thank you for the post.Here is my blog … frun-test.sakura.ne.jp
628677 316322There is noticeably a bundle to know about this. I assume you made certain good points in functions also. 5591
I really like and appreciate your post.
Thanks-a-mundo for the article.Really looking forward to read more. Will read on…
Wow, great post.Much thanks again. Awesome.
Great, thanks for sharing this blog post.Really looking forward to read more. Really Great.
Fantastic blog post.Really thank you! Fantastic.
Very neat article.Really looking forward to read more. Fantastic.
Major thanks for the post.Much thanks again. Want more.
I truly appreciate this blog article.Much thanks again. Will read on…
Really enjoyed this blog.Really looking forward to read more. Much obliged.
Thanks a lot for the article post.Really thank you! Great.
Wow, great blog. Want more.
I loved your article post.Really thank you! Awesome.
Im thankful for the blog.Much thanks again. Much obliged.
Thanks a lot for the article.Thanks Again. Keep writing.
Thanks for sharing, this is a fantastic blog post.Really thank you!
ivermectin manufacturers ivermectin horse dewormer
I really liked your blog post.Really looking forward to read more. Fantastic.
Thanks for the blog.Really looking forward to read more. Will read on…
I value the article post. Will read on…
Enjoyed every bit of your article.Thanks Again.
Appreciate you sharing, great blog post. Really Great.
Hey, thanks for the post.Really looking forward to read more. Want more.
azithromycin breastfeeding antibiotic azithromycin how to reduce side effects of azithromycin how long does azithromycin work
I really like and appreciate your post.Really looking forward to read more. Cool.
My brother recommended I might like this blog. He was entirely right.This post truly made my day. You can not imagine just how much time I had spent forthis information! Thanks!
Hello! I’ve been reading your blog for some time now and finally got the courageto go ahead and give you a shout out from Humble Tx!Just wanted to tell you keep up the great work!
Thank you for your post.Thanks Again. Keep writing.
I do not even know how I ended up here, but I thought this post wasgreat. I do not know who you are but certainly you’re going to a famous blogger if you are not already😉 Cheers!
Hey! I know this is kinda off topic but I was wondering if you knew where I could locate a captcha plugin for mycomment form? I’m using the same blog platform as yours and I’mhaving trouble finding one? Thanks a lot!
Hi, I do believe this is a great blog. I stumbledupon it 😉 I’m going to return once again since i have saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to help others.
I value the blog.Really looking forward to read more. Cool.
Usually, if a bettor believes the underdog not onlywill cover but they will win outright, bettors will bet the moneyline on the underdog which could net a greaterpayout.
Very energetic article, I enjoyed that a lot.Will there be a part 2?
Im grateful for the post.Thanks Again. Keep writing.
online pharmacy quick delivery: us online pharmacy – northern pharmacy canada
Your method of describing all in this post is truly good, all be capable of simply understand it, Thanks a lot.
I loved your blog.Really looking forward to read more. Really Great.
I truly appreciate this post.Really looking forward to read more. Cool.
That is a very good tip especially to those fresh to the blogosphere. Brief but very precise information… Thanks for sharing this one. A must read article!
stromectol pills canada – ivermectin for human stromectol for head lice
At this time it seems like Expression Engine is the best blogging platform available right now. (from what I’ve read) Is that what you are using on your blog?
A big thank you for your article.Really thank you! Will read on…
I loved your blog article.Really looking forward to read more. Really Great.
Thanks again for the article post.Really thank you! Really Cool.
Looking forward to reading more. Great article.Really thank you! Awesome.
My brain gave up fighting for blood and my cock took the majority share of it, intelligent thought was not in my favor at that moment.
I like what you guys are up too. This type of clever work and exposure! Keep up the terrific works guys I’ve incorporated you guys to my personal blogroll.
I blog quite often and I seriously appreciate your content.The article has truly peaked my interest. I am going to book mark your blog and keep checking fornew information about once a week. I opted in for your RSS feedas well.
Aw, this was a really nice post. Taking the time and actual effort tocreate a very good article… but what can I say… I procrastinate a lot and don’t manage to getnearly anything done.
Im thankful for the blog post.Really thank you! Really Great.
750449 163024A very exciting go by way of, I may not agree completely, but you do make some actually legitimate factors. 482986
Hello, after reading this remarkable post i am as well glad to share my experiencehere with mates.
I really liked your post.Really looking forward to read more. Really Cool.
modalert provigil medication – provigil over the counter
I think this is a real great blog.Thanks Again. Great.
7-11 otc ed pills – reddit best ed pills best rhino ed pills
I’ll right away snatch your rss as I can not find your e-mail subscription link or newsletter service. Do you have any? Kindly let me recognise so that I could subscribe. Thanks.
Looking forward to reading more. Great blog post.Much thanks again. Much obliged.
Whoa. That was a fantastic short article. Please keep writing for the reason that I like your style.
Hey, thanks for the blog article.Much thanks again.
I love reading through an article that will make people think. Also, thank you for allowing me to comment!
Hi, I check your new stuff like every week. Your humoristic style isawesome, keep up the good work!
Wealthy and traveling anywhere and whenever I want with my doggie, plus helping get dogs fixed, and those that need homes, and organizations that do thus and such.
Aw, this was a very good post. Finding the time and actual effort to generate a top notch article?but what can I say?I hesitate a whole lot and never manage to get nearly anything done.
Aw, this was an incredibly good post. Taking a few minutes and actual effort to generate a very good article… but what can I say… I put things off a lot and don’t manage to get anything done.
There’s certainly a great deal to learn about this topic. I like all of the points you have made.
“Even though the odds are extremely low, the investment is incredibly modest,” he stated.
Thank you for the auspicious writeup. Itin fact was a amusement account it. Look advanced to more added agreeable from you!However, how could we communicate?
I am so grateful for your blog.Much thanks again. Cool.
Heya! I’m at work browsing your blog from my new iphone 4! Just wanted to say I love reading through your blog and look forward to all your posts! Keep up the excellent work!
Thanks for your personal marvelous posting! I certainlyenjoyed reading it, you will be a great author. I will make certain to bookmark yourblog and may come back later on. I want to encourage continue your great writing, have a nice evening!
It’s really a great and useful piece of information. I’m happy that you shared this useful info with us.Please keep us informed like this. Thanksfor sharing.
Hi there! Do you use Twitter? I’d like to follow you if that would be okay.I’m definitely enjoying your blog and look forward tonew posts.
Muchos Gracias for your blog post.Thanks Again. Cool.
Excellent post however I was wondering if you could write a litte more on this subject? I’d be very grateful if you could elaborate a little bit more. Thanks!
generic clomid over the counter walmart Sooth Exams
Hello there! This post couldn’t be written any better! Reading throughthis post reminds me of my previous room mate!He always kept talking about this. I will forward this articleto him. Pretty sure he will have a good read. Manythanks for sharing!
These are truly enormous ideas in regarding blogging.You have touched some fastidious factorshere. Any way keep up wrinting.
It is actually a nice and helpful piece of information. I am satisfied that you just shared this helpful information with us. Please stay us informed like this. Thanks for sharing.
tadacip 20 for sale — generic tadacip tadacip online
What as up i am kavin, its my first occasion to commenting anywhere, when i read this paragraph i thought i could also make comment due to this sensible piece of writing.
Everyone loves it whenever people get together and share thoughts. Great blog, stick with it.
Fantastic article post.Much thanks again. Keep writing.
Good day! This is my first visit to your blog! We are a group of volunteers andstarting a new project in a community in the same niche.Your blog provided us useful information to work on. You havedone a outstanding job!
Thank you, I’ve recently been looking for info approximately this subject for ages and yours is the greatest I’ve discovered so far. But, what about the bottom line? Are you positive in regards to the supply?
It really is near close to impossible to encounter well-advised men or women on this niche, although you appear like you comprehend what exactly you’re preaching about! Thanks A Lot
This is one awesome article. Great.
Thank you ever so for you blog.Much thanks again. Great.
Fantastic blog article.Really looking forward to read more. Keep writing.
Very good blog. Cool.
Say, you got a nice article.Much thanks again. Cool.
Thanks a lot for the article post.Really thank you! Fantastic.
Enjoyed every bit of your blog.Much thanks again. Really Cool.
Great article.Much thanks again. Keep writing.
Really appreciate you sharing this post.Really looking forward to read more. Will read on…
A big thank you for your article.Really thank you! Want more.
Wow, great post.Much thanks again. Want more.
A big thank you for your blog post.Thanks Again. Really Great.
Great, thanks for sharing this blog post. Awesome.
A big thank you for your blog article.Really looking forward to read more. Want more.
This is one awesome article.Really thank you!
Really informative article post.Really looking forward to read more. Fantastic.
Enjoyed every bit of your blog article. Keep writing.
Thanks a lot for the blog.Really looking forward to read more. Fantastic.
This is one awesome article.Really looking forward to read more. Much obliged.
Hey, thanks for the post.Thanks Again. Cool.
I am so grateful for your post.Much thanks again. Fantastic.
A big thank you for your article.Thanks Again. Awesome.
I value the blog.Really looking forward to read more.
Thanks-a-mundo for the blog.Really thank you! Really Cool.
I really enjoy the blog.Really looking forward to read more. Keep writing.
I value the post.Thanks Again. Awesome.
Very neat article.Really looking forward to read more. Great.
A round of applause for your post. Much obliged.
Thank you ever so for you article.Much thanks again. Want more.
Im obliged for the blog. Really Great.
Thanks for sharing, this is a fantastic blog.Thanks Again. Really Cool.
Im thankful for the blog post.Much thanks again. Keep writing.
Really enjoyed this blog. Much obliged.
This is one awesome blog.Really thank you! Awesome.
Muchos Gracias for your article.Really thank you! Cool.
Thanks for the article post.Thanks Again. Cool.
Enjoyed every bit of your post. Really Cool.
I value the article post.Much thanks again. Want more.
Very good post.Thanks Again. Much obliged.
Enjoyed every bit of your post. Really Great.
Very neat blog.Much thanks again. Cool.
Fantastic article.Really thank you!
Say, you got a nice article post.Thanks Again. Cool.
Major thanks for the article post.Really looking forward to read more. Keep writing.
Aw, this was an incredibly nice post. Taking a few minutes and actual effort to generate a top notch articleÖ but what can I sayÖ I put things off a whole lot and don’t seem to get anything done.
I love what you guys are usually up too. This sort of cleverwork and reporting! Keep up the wonderful works guys I’ve added you guys to my own blogroll.
Very informative article post.Much thanks again. Want more.
I value the post.Thanks Again. Really Cool.
Thank you for your blog article.Much thanks again. Want more.
Major thanks for the blog.Much thanks again. Awesome.
Really enjoyed this blog.Much thanks again. Cool.
Very neat post.Really thank you! Cool.
Thanks a lot for the blog.Really thank you! Really Great.
Thanks for the article.Really thank you! Cool.
I really enjoy the post. Great.
wow, awesome blog post.Much thanks again. Really Great.
Im thankful for the post. Awesome.
Awesome blog article.Much thanks again. Want more.
I couldn챠t refrain from commenting. Very well written!
Greetings! Very useful advice in this particular post! It’s the little changes that make the biggest changes. Thanks a lot for sharing!
I loved your blog post.Really thank you! Much obliged.
Major thanks for the post.Really thank you! Much obliged.
Enjoyed every bit of your blog article.Thanks Again. Keep writing.
Say, you got a nice article.Much thanks again. Really Cool.
I value the blog post. Great.
Wow, great blog article. Really Cool.
Fantastic blog.Really looking forward to read more. Really Cool.
Thanks a lot for the blog.Thanks Again. Really Cool.
wow, awesome blog article.Much thanks again. Cool.
Very good blog.Much thanks again. Really Cool.
Enjoyed every bit of your article post. Will read on…
I appreciate you sharing this blog article.Thanks Again. Keep writing.
Appreciate you sharing, great article.Really looking forward to read more. Awesome.
I value the blog article.Thanks Again. Awesome.
Im thankful for the article post.Thanks Again. Great.
Very neat blog.Thanks Again. Will read on…
Thanks a lot for the post.Much thanks again. Fantastic.
Muchos Gracias for your blog.Really thank you! Awesome.
Wow, great post.Really thank you!
I really like and appreciate your blog article.Thanks Again. Fantastic.
Really informative blog article.Thanks Again. Keep writing.
I truly appreciate this blog.Much thanks again. Cool.
Looking forward to reading more. Great blog article. Will read on…
I really liked your blog post.Really looking forward to read more.
Really informative article post.Really looking forward to read more. Cool.
Thanks a lot for the blog article.Thanks Again. Great.
Spot on with this write-up, I honestly believe that this amazing site needs far more attention. I’ll probably be returning to see more, thanks for the information.
You made some good points there. I looked on the internet for additional information about the issue and found most people will go along with your views on this site.
Pretty! This was a really wonderful article. Thank you for supplying this info.
Good write-up. I absolutely appreciate this site. Stick with it!
You’ve made some really good points there. I checked on the web for more information about the issue and found most individuals will go along with your views on this site.
Your style is so unique in comparison to other people I have read stuff from. Thank you for posting when you have the opportunity, Guess I’ll just bookmark this page.
I seriously love your website.. Pleasant colors & theme. Did you build this web site yourself? Please reply back as I’m attempting to create my own site and would love to know where you got this from or just what the theme is named. Thank you.
After I originally left a comment I appear to have clicked the -Notify me when new comments are added- checkbox and from now on each time a comment is added I receive 4 emails with the exact same comment. Is there a means you can remove me from that service? Kudos.
This website certainly has all the information and facts I wanted concerning this subject and didn’t know who to ask.
You need to be a part of a contest for one of the greatest sites on the net. I’m going to recommend this web site!
Good article. I’m facing some of these issues as well..
Good site you have got here.. It’s difficult to find high quality writing like yours nowadays. I truly appreciate individuals like you! Take care!!
Wonderful post! We are linking to this great content on our website. Keep up the good writing.
Oh my goodness! Awesome article dude! Thanks, However I am experiencing difficulties with your RSS. I don’t understand why I am unable to join it. Is there anybody else getting the same RSS problems? Anyone who knows the solution will you kindly respond? Thanks.
This blog was… how do you say it? Relevant!! Finally I’ve found something that helped me. Thanks.
When I initially left a comment I seem to have clicked the -Notify me when new comments are added- checkbox and now each time a comment is added I recieve 4 emails with the same comment. There has to be a way you can remove me from that service? Kudos.
You should take part in a contest for one of the most useful sites on the web. I’m going to highly recommend this blog!
Everything is very open with a precise description of the challenges. It was truly informative. Your site is very useful. Thank you for sharing!
You’re so awesome! I don’t think I’ve read anything like this before. So good to find someone with a few original thoughts on this topic. Really.. thanks for starting this up. This site is one thing that’s needed on the internet, someone with a bit of originality.
This is a good tip particularly to those new to the blogosphere.Brief but very accurate information… Thanks for sharing this one.A must read post!
Hi there! This article could not be written much better! Reading through this article reminds me of my previous roommate! He always kept talking about this. I’ll send this article to him. Pretty sure he’ll have a great read. Thanks for sharing!
This is the perfect website for anyone who wishes to understand this topic. You know a whole lot its almost tough to argue with you (not that I really will need to…HaHa). You definitely put a brand new spin on a subject that’s been written about for decades. Excellent stuff, just wonderful.
This is a really good tip especially to those new to the blogosphere. Brief but very precise infoÖ Appreciate your sharing this one. A must read post!
how to switch from xanax to klonopin buspar mixed with klonopin is valium more sedating than klonopin
You have made some good points there. I checked on the web for more info about the issue and found most individuals will go along with your views on this website.
Right here is the right blog for everyone who really wants to understand this topic. You know a whole lot its almost hard to argue with you (not that I really would want to…HaHa). You definitely put a fresh spin on a subject that’s been written about for decades. Great stuff, just wonderful.
Way cool! Some very valid points! I appreciate you penning this article and the rest of the website is very good.
I really love your blog.. Excellent colors & theme. Did you create this web site yourself? Please reply back as I’m planning to create my very own site and want to know where you got this from or just what the theme is named. Many thanks!
Oh my goodness! Impressive article dude! Thanks, However I am having troubles with your RSS. I don’t know the reason why I am unable to join it. Is there anybody having the same RSS problems? Anybody who knows the solution can you kindly respond? Thanx!
That is a good tip especially to those fresh to the blogosphere. Short but very precise information… Appreciate your sharing this one. A must read article.
script pharmacy legitimate canadian internet pharmacies
Hmm is anyone else encountering problems with the images on this blog loading?I’m trying to determine if its a problem on my end or if it’s theblog. Any feed-back would be greatly appreciated.
It¡¦s really a great and helpful piece of information. I am happy that you just shared this useful info with us. Please keep us informed like this. Thank you for sharing.
I do not even know how I ended up here, but I thought this post was good. I do not know who you are but certainly you are going to a famous blogger if you aren’t already
Hello! I just wanted to ask if you ever have any problems with hackers?My last blog (wordpress) was hacked and I ended up losing months ofhard work due to no backup. Do you have anysolutions to protect against hackers?
Very good blog.Much thanks again. Really Cool.
Hello! I just wanted to ask if you ever have any trouble with hackers?My last blog (wordpress) was hacked and I ended up losing many months of hard work due tono back up. Do you have any solutions to preventhackers?
My brother suggested I might like this blog. He was once entirely right. This submit truly made my day. You can not believe just how so much time I had spent for this info! Thank you!
Wow! After all I got a blog from where I be able to really obtain helpful facts regarding my study and knowledge.Here is my blog post – a913.vip
Hi, just wanted to say, I loved this blog post.It was inspiring. Keep on posting!
I’d need to check with you here. Which isn’t one thing I normally do! I get pleasure from studying a publish that will make people think. Additionally, thanks for allowing me to comment!
With thanks, I enjoy it!college essay writer for pay write my essay i need help writing a thesis statement
Hello there, just became aware of your blog throughGoogle, and found that it’s truly informative. I’m gonna watch outfor brussels. I’ll appreciate if you continuethis in future. A lot of people will be benefited from your writing.Cheers!
The next time I read a blog, Hopefully it does not disappoint me as much as this particular one. I mean, Yes, it was my choice to read through, but I actually believed you would have something useful to talk about. All I hear is a bunch of crying about something you can fix if you were not too busy looking for attention.
After I initially commented I seem to have clicked the -Notify me when new comments are added- checkbox and from now on each time a comment is added I get four emails with the same comment. Perhaps there is a way you can remove me from that service? Thanks.
I was more than happy to uncover this page. I need to to thank you for your time due to this fantastic read!! I definitely appreciated every little bit of it and I have you bookmarked to look at new information on your web site.
I like it when folks get together and share views. Great blog, keep it up.
Hey there! I just want to offer you a big thumbs up for the great info you have here on this post. I’ll be returning to your site for more soon.
Very good post! We will be linking to this great article on our site. Keep up the great writing.
Howdy! This post couldn’t be written any better! Going through this post reminds me of my previous roommate! He constantly kept preaching about this. I most certainly will send this information to him. Fairly certain he’ll have a very good read. Thank you for sharing!
There’s definately a great deal to find out about this issue. I really like all of the points you’ve made.
Good post. I learn something totally new and challenging on blogs I stumbleupon on a daily basis. It’s always interesting to read through articles from other authors and use a little something from other web sites.
You’ve made some really good points there. I looked on the internet to learn more about the issue and found most individuals will go along with your views on this website.
An intriguing discussion is definitely worth comment. There’s no doubt that that you should publish more about this issue, it might not be a taboo subject but typically folks don’t discuss these issues. To the next! All the best.
Aw, this was an incredibly good post. Finding the time and actual effort to produce a top notch article… but what can I say… I procrastinate a whole lot and never seem to get anything done.
Hello there! I simply want to give you a big thumbs up for your excellent info you have got right here on this post. I’ll be coming back to your web site for more soon.
You’re so cool! I do not suppose I have read a single thing like that before. So good to find another person with a few genuine thoughts on this issue. Seriously.. many thanks for starting this up. This web site is one thing that’s needed on the internet, someone with some originality.
Having read this I believed it was extremely informative. I appreciate you finding the time and effort to put this article together. I once again find myself personally spending a lot of time both reading and leaving comments. But so what, it was still worthwhile.
Aw, this was a very nice post. Taking the time and actual effort to generate a good article… but what can I say… I hesitate a whole lot and don’t manage to get anything done.
Hi! I could have sworn I’ve visited your blog before but after going through a few of the posts I realized it’s new to me. Regardless, I’m certainly pleased I found it and I’ll be book-marking it and checking back frequently.
Aw, this was an exceptionally good post. Taking a few minutes and actual effort to produce a good article… but what can I say… I put things off a whole lot and never seem to get nearly anything done.
I absolutely love your site.. Great colors & theme. Did you develop this website yourself? Please reply back as I’m planning to create my own website and would love to know where you got this from or what the theme is called. Kudos.
I love it when individuals get together and share ideas. Great blog, continue the good work!
Your style is very unique compared to other folks I have read stuff from. Thanks for posting when you’ve got the opportunity, Guess I will just book mark this site.
Good day! I could have sworn I’ve been to this website before but after going through some of the posts I realized it’s new to me. Nonetheless, I’m definitely happy I came across it and I’ll be bookmarking it and checking back frequently!
I have to thank you for the efforts you’ve put in writing this website. I’m hoping to view the same high-grade blog posts by you later on as well. In truth, your creative writing abilities has motivated me to get my very own website now 😉
After exploring a handful of the blog articles on your blog, I honestly appreciate your technique of writing a blog. I book-marked it to my bookmark website list and will be checking back soon. Please visit my web site too and tell me what you think.
Having read this I believed it was extremely enlightening. I appreciate you taking the time and effort to put this informative article together. I once again find myself personally spending way too much time both reading and posting comments. But so what, it was still worth it!
Having read this I believed it was extremely informative. I appreciate you taking the time and energy to put this short article together. I once again find myself personally spending a lot of time both reading and posting comments. But so what, it was still worth it.
Good information. Lucky me I discovered your site by chance (stumbleupon). I’ve book-marked it for later!
Spot on with this write-up, I honestly feel this site needs a lot more attention. I’ll probably be back again to read more, thanks for the info.
An outstanding share! I have just forwarded this onto a colleague who was conducting a little homework on this. And he actually bought me lunch simply because I stumbled upon it for him… lol. So allow me to reword this…. Thank YOU for the meal!! But yeah, thanx for spending time to discuss this matter here on your internet site.
Greetings! Very helpful advice within this post! It is the little changes that will make the most significant changes. Thanks a lot for sharing!
This website certainly has all the info I wanted about this subject and didn’t know who to ask.
This website truly has all the info I wanted about this subject and didn’t know who to ask.
An intriguing discussion is worth comment. I believe that you need to write more about this issue, it may not be a taboo subject but typically people don’t talk about these issues. To the next! All the best!
Can I simply say what a relief to discover someone who actually understands what they are talking about over the internet. You certainly realize how to bring an issue to light and make it important. A lot more people should read this and understand this side of the story. I was surprised you’re not more popular given that you certainly possess the gift.
Spot on with this write-up, I honestly think this amazing site needs a lot more attention. I’ll probably be returning to read through more, thanks for the information!
Way cool! Some extremely valid points! I appreciate you penning this article and also the rest of the site is very good.
Pretty! This has been an extremely wonderful post. Thank you for providing this info.
Having read this I believed it was extremely informative. I appreciate you finding the time and effort to put this article together. I once again find myself spending a lot of time both reading and commenting. But so what, it was still worthwhile!
Excellent write-up. I certainly appreciate this site. Continue the good work!
Howdy! This article could not be written any better! Going through this post reminds me of my previous roommate! He continually kept talking about this. I am going to send this post to him. Fairly certain he’s going to have a very good read. Many thanks for sharing!
Good post. I learn something new and challenging on blogs I stumbleupon on a daily basis. It will always be interesting to read articles from other writers and practice something from their web sites.
You should be a part of a contest for one of the greatest blogs on the web. I will recommend this web site!
May I just say what a relief to find a person that truly understands what they’re discussing over the internet. You definitely know how to bring an issue to light and make it important. A lot more people have to look at this and understand this side of your story. I was surprised that you are not more popular because you surely possess the gift.
You’re so cool! I don’t think I’ve read something like this before. So good to find someone with a few genuine thoughts on this topic. Seriously.. thank you for starting this up. This website is one thing that is required on the internet, someone with a little originality.
An interesting discussion is definitely worth comment. I do believe that you should write more about this topic, it might not be a taboo matter but generally people don’t discuss such subjects. To the next! Best wishes.
I wanted to thank you for this very good read!! I certainly enjoyed every little bit of it. I have got you book marked to check out new stuff you post…
This is a topic which is near to my heart… Best wishes! Exactly where are your contact details though?
Right here is the right web site for anybody who really wants to find out about this topic. You understand a whole lot its almost tough to argue with you (not that I really would want to…HaHa). You definitely put a new spin on a subject which has been written about for a long time. Wonderful stuff, just excellent.
You’re so awesome! I don’t suppose I’ve truly read anything like this before. So wonderful to discover somebody with genuine thoughts on this issue. Seriously.. thank you for starting this up. This web site is something that is needed on the web, someone with a bit of originality.
Good info. Lucky me I recently found your website by accident (stumbleupon). I have saved as a favorite for later.
Howdy! This article couldn’t be written much better! Looking through this post reminds me of my previous roommate! He continually kept preaching about this. I’ll forward this post to him. Pretty sure he’s going to have a very good read. Thank you for sharing!
It’s hard to find knowledgeable people on this subject, however, you sound like you know what you’re talking about! Thanks
You’re so interesting! I do not suppose I’ve truly read a single thing like this before. So wonderful to find somebody with a few unique thoughts on this subject matter. Seriously.. thanks for starting this up. This site is one thing that’s needed on the web, someone with some originality.
Way cool! Some very valid points! I appreciate you writing this article and the rest of the website is also really good.
I’m impressed, I must say. Rarely do I encounter a blog that’s both equally educative and amusing, and let me tell you, you have hit the nail on the head. The problem is something which not enough folks are speaking intelligently about. Now i’m very happy that I came across this in my hunt for something regarding this.
Next time I read a blog, I hope that it won’t fail me as much as this particular one. I mean, I know it was my choice to read, nonetheless I really believed you would probably have something helpful to say. All I hear is a bunch of complaining about something that you could possibly fix if you weren’t too busy seeking attention.
I’m excited to uncover this website. I want to to thank you for your time just for this fantastic read!! I definitely enjoyed every bit of it and I have you saved to fav to check out new stuff on your web site.
Hello! I could have sworn I’ve visited this web site before but after looking at some of the articles I realized it’s new to me. Nonetheless, I’m definitely delighted I stumbled upon it and I’ll be book-marking it and checking back regularly!
There is certainly a great deal to find out about this subject. I love all of the points you made.
Very good article. I will be dealing with a few of these issues as well..
Very good information. Lucky me I found your blog by accident (stumbleupon). I’ve book marked it for later.
After looking over a handful of the blog posts on your web page, I really like your way of blogging. I saved it to my bookmark website list and will be checking back soon. Please check out my website too and tell me what you think.
Way cool! Some extremely valid points! I appreciate you penning this article and the rest of the site is very good.
Oh my goodness! Impressive article dude! Thanks, However I am having difficulties with your RSS. I don’t know the reason why I am unable to subscribe to it. Is there anybody else having identical RSS problems? Anybody who knows the solution will you kindly respond? Thanx!
This is a topic that is near to my heart… Thank you! Exactly where can I find the contact details for questions?
This is a topic which is close to my heart… Many thanks! Exactly where can I find the contact details for questions?
You have made some really good points there. I checked on the web to learn more about the issue and found most individuals will go along with your views on this website.
I would like to thank you for the efforts you have put in penning this blog. I am hoping to view the same high-grade content by you later on as well. In truth, your creative writing abilities has encouraged me to get my very own website now 😉
Your style is very unique in comparison to other folks I have read stuff from. Thanks for posting when you have the opportunity, Guess I will just book mark this blog.
This site was… how do you say it? Relevant!! Finally I’ve found something that helped me. Thanks.
Everything is very open with a precise explanation of the challenges. It was definitely informative. Your website is useful. Many thanks for sharing.
Hi, I do believe this is an excellent web site. I stumbledupon it 😉 I will come back yet again since I saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to guide others.
There is definately a lot to find out about this issue. I really like all the points you’ve made.
This is a topic that’s near to my heart… Many thanks! Where can I find the contact details for questions?
Very nice blog post. I definitely love this website. Continue the good work!
Pretty! This was an extremely wonderful post. Many thanks for providing this information.
Good post. I learn something totally new and challenging on websites I stumbleupon on a daily basis. It will always be useful to read content from other authors and use something from other websites.
You’re so interesting! I do not think I’ve truly read something like this before. So wonderful to find another person with a few genuine thoughts on this issue. Really.. thanks for starting this up. This web site is one thing that is required on the web, someone with a little originality.
This excellent website really has all of the information I needed concerning this subject and didn’t know who to ask.
Spot on with this write-up, I honestly believe this site needs much more attention. I’ll probably be returning to see more, thanks for the advice.
This is a topic that’s near to my heart… Best wishes! Where are your contact details though?
You should be a part of a contest for one of the best sites on the web. I most certainly will highly recommend this website!
Hello there! This blog post couldn’t be written any better! Going through this post reminds me of my previous roommate! He continually kept preaching about this. I will forward this information to him. Fairly certain he’s going to have a good read. Many thanks for sharing!
Good post! We are linking to this great post on our site. Keep up the great writing.
Spot on with this write-up, I really think this web site needs a great deal more attention. I’ll probably be returning to read through more, thanks for the info!
Good blog post. I certainly appreciate this site. Keep it up!
I seriously love your blog.. Pleasant colors & theme. Did you develop this web site yourself? Please reply back as I’m hoping to create my very own website and want to learn where you got this from or just what the theme is called. Thanks.
Great post. I’m experiencing some of these issues as well..
I was very pleased to uncover this web site. I want to to thank you for ones time due to this wonderful read!! I definitely loved every bit of it and I have you saved as a favorite to check out new stuff in your blog.
Your style is unique compared to other people I’ve read stuff from. Thanks for posting when you have the opportunity, Guess I will just bookmark this blog.
This web site really has all of the information and facts I wanted concerning this subject and didn’t know who to ask.
Can I simply say what a comfort to find an individual who truly understands what they are talking about on the internet. You certainly understand how to bring a problem to light and make it important. More people have to look at this and understand this side of the story. I was surprised that you’re not more popular because you surely possess the gift.
I used to be able to find good information from your articles.
I’m amazed, I have to admit. Rarely do I come across a blog that’s equally educative and amusing, and let me tell you, you have hit the nail on the head. The problem is something too few people are speaking intelligently about. I am very happy I stumbled across this in my search for something relating to this.
This is the right site for everyone who wishes to find out about this topic. You know a whole lot its almost hard to argue with you (not that I personally will need to…HaHa). You certainly put a brand new spin on a topic which has been written about for decades. Great stuff, just wonderful.
Pretty! This was an extremely wonderful article. Thanks for providing these details.
I really like it when people get together and share ideas. Great website, keep it up!
I needed to thank you for this very good read!! I absolutely loved every bit of it. I have you saved as a favorite to check out new things you post…
I blog often and I really thank you for your information. Your article has truly peaked my interest. I will book mark your blog and keep checking for new information about once per week. I opted in for your RSS feed too.
Saved as a favorite, I love your web site!
This is a topic that’s near to my heart… Many thanks! Where can I find the contact details for questions?
This is the right website for anyone who wants to find out about this topic. You understand so much its almost hard to argue with you (not that I actually will need to…HaHa). You definitely put a brand new spin on a topic that’s been discussed for a long time. Wonderful stuff, just wonderful.
Howdy! This blog post could not be written any better! Going through this post reminds me of my previous roommate! He continually kept talking about this. I am going to forward this information to him. Fairly certain he’s going to have a good read. Many thanks for sharing!
Nice post. I learn something totally new and challenging on sites I stumbleupon on a daily basis. It’s always useful to read through content from other writers and use a little something from their sites.
I’m impressed, I have to admit. Seldom do I come across a blog that’s equally educative and amusing, and without a doubt, you’ve hit the nail on the head. The issue is something which too few men and women are speaking intelligently about. I am very happy that I came across this during my search for something relating to this.
The next time I read a blog, Hopefully it won’t fail me just as much as this one. I mean, Yes, it was my choice to read, but I actually believed you would probably have something useful to say. All I hear is a bunch of crying about something that you could possibly fix if you weren’t too busy looking for attention.
Your style is very unique compared to other folks I have read stuff from. Many thanks for posting when you have the opportunity, Guess I’ll just bookmark this blog.
Good web site you’ve got here.. It’s difficult to find high quality writing like yours nowadays. I seriously appreciate individuals like you! Take care!!
Greetings! Very useful advice in this particular post! It is the little changes that produce the most important changes. Many thanks for sharing!
I was able to find good advice from your blog posts.
After checking out a handful of the articles on your web site, I honestly like your technique of blogging. I added it to my bookmark webpage list and will be checking back soon. Take a look at my web site too and let me know what you think.
It’s difficult to find educated people in this particular subject, however, you sound like you know what you’re talking about! Thanks
You’re so interesting! I don’t believe I’ve read a single thing like that before. So good to find someone with some genuine thoughts on this subject matter. Really.. many thanks for starting this up. This site is something that is needed on the web, someone with some originality.
Way cool! Some very valid points! I appreciate you writing this write-up and the rest of the site is very good.
Very good information. Lucky me I found your blog by chance (stumbleupon). I have saved it for later.
I was able to find good info from your blog articles.
They’re licensed arborists and employees are insured.
Betpas resmi yeni giriş adresi olarak hizmet veriyoruz. Betpas güncel giriş adresi kaç oldu , şikayet ve canlı bahis oyunları
I seriously love your website.. Pleasant colors & theme. Did you build this site yourself? Please reply back as I’m attempting to create my own blog and would love to find out where you got this from or exactly what the theme is named. Thanks.
clindamycin antibiotic clindamycin for acne warnings for clindamycin
May I just say what a comfort to uncover a person that really knows what they’re discussing on the internet. You definitely know how to bring an issue to light and make it important. More people really need to look at this and understand this side of the story. I was surprised you are not more popular since you surely possess the gift.
This is the right web site for anybody who hopes to find out about this topic. You understand so much its almost hard to argue with you (not that I personally will need to…HaHa). You certainly put a new spin on a topic which has been written about for ages. Great stuff, just wonderful.
Right here is the perfect site for everyone who hopes to understand this topic. You know a whole lot its almost hard to argue with you (not that I really would want to…HaHa). You certainly put a fresh spin on a subject which has been written about for decades. Excellent stuff, just wonderful.
Hi, I do think this is a great web site. I stumbledupon it 😉 I may return yet again since I saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to help other people.
Hello! I simply would like to offer you a huge thumbs up for your excellent info you have here on this post. I’ll be returning to your website for more soon.
This site really has all the information and facts I needed concerning this subject and didn’t know who to ask.
This is a topic that is near to my heart… Thank you! Exactly where can I find the contact details for questions?
This site was… how do you say it? Relevant!! Finally I’ve found something that helped me. Thank you!
I’m amazed, I have to admit. Rarely do I come across a blog that’s equally educative and amusing, and without a doubt, you’ve hit the nail on the head. The issue is something that too few folks are speaking intelligently about. Now i’m very happy that I stumbled across this in my search for something concerning this.
This is the perfect webpage for everyone who hopes to find out about this topic. You realize so much its almost tough to argue with you (not that I actually will need to…HaHa). You definitely put a brand new spin on a topic that has been written about for decades. Great stuff, just great.
It’s hard to find well-informed people on this subject, however, you sound like you know what you’re talking about! Thanks
It’s nearly impossible to find knowledgeable people in this particular subject, but you seem like you know what you’re talking about! Thanks
Great post. I will be dealing with many of these issues as well..
This is a very good tip particularly to those new to the blogosphere. Short but very accurate info… Thank you for sharing this one. A must read article.
This website was… how do you say it? Relevant!! Finally I have found something that helped me. Thank you!
When I initially commented I seem to have clicked the -Notify me when new comments are added- checkbox and from now on every time a comment is added I recieve four emails with the exact same comment. There has to be an easy method you are able to remove me from that service? Thanks a lot.
Excellent post. I definitely love this website. Continue the good work!
When I originally left a comment I appear to have clicked the -Notify me when new comments are added- checkbox and from now on every time a comment is added I get four emails with the exact same comment. There has to be a means you can remove me from that service? Thank you.
Good article. I absolutely appreciate this site. Thanks!
Greetings! Very helpful advice within this post! It is the little changes which will make the most important changes. Thanks a lot for sharing!
You made some decent points there. I looked on the net for additional information about the issue and found most people will go along with your views on this web site.
Spot on with this write-up, I seriously feel this site needs much more attention. I’ll probably be returning to see more, thanks for the advice.
An interesting discussion is worth comment. I do think that you need to publish more about this subject matter, it may not be a taboo matter but typically folks don’t speak about such issues. To the next! Cheers.
After looking over a few of the blog articles on your blog, I truly like your way of blogging. I book-marked it to my bookmark site list and will be checking back in the near future. Please check out my web site too and tell me what you think.
Your style is very unique in comparison to other folks I have read stuff from. I appreciate you for posting when you have the opportunity, Guess I’ll just bookmark this blog.
This is a great tip particularly to those fresh to the blogosphere. Short but very accurate info… Thank you for sharing this one. A must read post!
This is a good tip particularly to those fresh to the blogosphere. Simple but very accurate info… Thanks for sharing this one. A must read post!
Great article! We are linking to this great post on our website. Keep up the good writing.
Way cool! Some very valid points! I appreciate you penning this article and also the rest of the site is really good.
I’m very happy to discover this great site. I want to to thank you for ones time for this fantastic read!! I definitely appreciated every part of it and i also have you bookmarked to see new stuff in your website.
Hi, There’s no doubt that your website might be having web browser compatibility issues. When I take a look at your web site in Safari, it looks fine however, when opening in I.E., it has some overlapping issues. I merely wanted to give you a quick heads up! Besides that, fantastic site.
An outstanding share! I’ve just forwarded this onto a colleague who had been doing a little research on this. And he in fact ordered me dinner simply because I found it for him… lol. So let me reword this…. Thank YOU for the meal!! But yeah, thanx for spending time to discuss this topic here on your web page.
Good post. I will be going through some of these issues as well..
Hi, I do think this is an excellent website. I stumbledupon it 😉 I will return yet again since i have book-marked it. Money and freedom is the best way to change, may you be rich and continue to guide other people.
Hi there, There’s no doubt that your site might be having internet browser compatibility issues. Whenever I take a look at your site in Safari, it looks fine however, when opening in Internet Explorer, it’s got some overlapping issues. I simply wanted to give you a quick heads up! Besides that, wonderful blog!
This is the perfect web site for anyone who would like to understand this topic. You understand so much its almost tough to argue with you (not that I personally would want to…HaHa). You definitely put a brand new spin on a topic that’s been written about for years. Wonderful stuff, just wonderful.
It’s difficult to find knowledgeable people for this topic, but you sound like you know what you’re talking about! Thanks
An outstanding share! I’ve just forwarded this onto a coworker who had been doing a little research on this. And he actually ordered me dinner simply because I discovered it for him… lol. So let me reword this…. Thanks for the meal!! But yeah, thanks for spending some time to talk about this issue here on your blog.
This is a really good tip particularly to those fresh to the blogosphere. Simple but very accurate info… Many thanks for sharing this one. A must read article!
Great web site you’ve got here.. It’s hard to find quality writing like yours nowadays. I truly appreciate individuals like you! Take care!!
I was able to find good advice from your blog posts.
After looking over a few of the articles on your website, I really like your way of blogging. I book marked it to my bookmark site list and will be checking back soon. Please check out my website too and tell me your opinion.
bookmarked!!, I love your website.
Hi! I could have sworn I’ve been to your blog before but after browsing through some of the posts I realized it’s new to me. Nonetheless, I’m definitely delighted I found it and I’ll be bookmarking it and checking back regularly!
Good day! I just wish to offer you a big thumbs up for your excellent information you have got right here on this post. I will be coming back to your site for more soon.
Hi there! I could have sworn I’ve been to your blog before but after looking at some of the posts I realized it’s new to me. Anyhow, I’m certainly happy I found it and I’ll be bookmarking it and checking back frequently.
Nice post. I learn something new and challenging on websites I stumbleupon everyday. It will always be exciting to read content from other writers and practice a little something from other sites.
I am continuously browsing online for posts that can facilitate me. Thanks!
Hi to every , since I am actually eager of reading this blog’s post to be updated daily. It contains good material.
It’s an amazing piece of writing designed for all the internet users; they will get benefit from it I am sure.
Hi, I do believe this is a great site. I stumbledupon it 😉 I am going to come back once again since i have bookmarked it. Money and freedom is the best way to change, may you be rich and continue to guide other people.
Hi, I do believe this is a great web site. I stumbledupon it 😉 I’m going to revisit once again since I book marked it. Money and freedom is the best way to change, may you be rich and continue to help other people.
There’s definately a great deal to learn about this topic. I love all the points you have made.
Very nice post. I definitely appreciate this website. Stick with it!
After I initially left a comment I appear to have clicked the -Notify me when new comments are added- checkbox and now whenever a comment is added I get 4 emails with the same comment. There has to be an easy method you are able to remove me from that service? Many thanks.
There is certainly a great deal to learn about this subject. I love all the points you’ve made.
There is certainly a great deal to learn about this subject. I love all the points you have made.
Howdy! This blog post couldn’t be written much better! Reading through this article reminds me of my previous roommate! He always kept preaching about this. I will forward this information to him. Fairly certain he’s going to have a good read. Thank you for sharing!
I really like reading through a post that can make people think. Also, thanks for allowing me to comment.
When I originally commented I seem to have clicked on the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I receive 4 emails with the same comment. There has to be a means you are able to remove me from that service? Thank you.
Hi there! This blog post couldn’t be written much better! Going through this post reminds me of my previous roommate! He continually kept preaching about this. I am going to forward this information to him. Fairly certain he will have a very good read. Thank you for sharing!
I’m very pleased to discover this page. I want to to thank you for ones time just for this wonderful read!! I definitely liked every little bit of it and I have you saved to fav to look at new things in your web site.
You made some good points there. I looked on the net to learn more about the issue and found most people will go along with your views on this web site.
I truly love your blog.. Very nice colors & theme. Did you develop this amazing site yourself? Please reply back as I’m wanting to create my own site and would love to learn where you got this from or just what the theme is named. Kudos.
Your style is unique compared to other people I’ve read stuff from. Thank you for posting when you’ve got the opportunity, Guess I’ll just bookmark this web site.
Very good information. Lucky me I ran across your blog by accident (stumbleupon). I’ve book marked it for later!
You are so awesome! I don’t think I’ve read through a single thing like this before. So great to find another person with a few genuine thoughts on this subject matter. Really.. thanks for starting this up. This website is one thing that is needed on the web, someone with a bit of originality.
I seriously love your website.. Excellent colors & theme. Did you develop this web site yourself? Please reply back as I’m wanting to create my very own website and want to know where you got this from or just what the theme is named. Cheers!
May I just say what a relief to discover somebody that genuinely knows what they are discussing on the internet. You actually realize how to bring an issue to light and make it important. More and more people need to look at this and understand this side of the story. I was surprised that you are not more popular because you definitely have the gift.
I’d like to thank you for the efforts you have put in penning this blog. I really hope to check out the same high-grade blog posts from you later on as well. In fact, your creative writing abilities has motivated me to get my very own blog now 😉
You’re so awesome! I do not suppose I’ve truly read something like that before. So nice to discover another person with unique thoughts on this subject. Really.. thank you for starting this up. This web site is something that is needed on the web, someone with some originality.
Greetings! Very useful advice within this post! It is the little changes which will make the most important changes. Thanks for sharing!
You made some decent points there. I checked on the internet to find out more about the issue and found most individuals will go along with your views on this site.
I blog frequently and I genuinely appreciate your information. The article has really peaked my interest. I’m going to book mark your site and keep checking for new details about once a week. I opted in for your RSS feed too.
It’s hard to find knowledgeable people for this topic, however, you seem like you know what you’re talking about! Thanks
You have made some decent points there. I looked on the web to find out more about the issue and found most people will go along with your views on this site.
I would like to thank you for the efforts you have put in penning this website. I’m hoping to check out the same high-grade content from you in the future as well. In truth, your creative writing abilities has motivated me to get my own, personal site now 😉
Way cool! Some extremely valid points! I appreciate you penning this post plus the rest of the website is also really good.
This is a topic that is close to my heart… Cheers! Where are your contact details though?
Good post. I learn something totally new and challenging on blogs I stumbleupon every day. It’s always exciting to read through articles from other authors and use something from their websites.
Aw, this was a very good post. Finding the time and actual effort to create a really good article… but what can I say… I put things off a whole lot and never seem to get nearly anything done.
Good post. I’m facing a few of these issues as well..
Oh my goodness! Impressive article dude! Thanks, However I am going through problems with your RSS. I don’t understand the reason why I can’t subscribe to it. Is there anybody having the same RSS issues? Anyone that knows the solution will you kindly respond? Thanks!!
I really love your blog.. Very nice colors & theme. Did you build this website yourself? Please reply back as I’m attempting to create my very own website and would love to learn where you got this from or exactly what the theme is named. Many thanks.
sapphire clinic
doktor kbb
dr güncel
dr kandulu
hairneva
dr şaban
I couldn’t resist commenting. Well written!
When I initially left a comment I seem to have clicked on the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I recieve 4 emails with the same comment. There has to be a way you can remove me from that service? Thanks a lot.
I was able to find good information from your blog articles.
An outstanding share! I’ve just forwarded this onto a colleague who was conducting a little research on this. And he actually bought me lunch because I stumbled upon it for him… lol. So let me reword this…. Thanks for the meal!! But yeah, thanx for spending the time to talk about this matter here on your site.
Having read this I believed it was really informative. I appreciate you finding the time and effort to put this article together. I once again find myself spending a significant amount of time both reading and leaving comments. But so what, it was still worthwhile!
Right here is the right site for everyone who wishes to understand this topic. You know so much its almost hard to argue with you (not that I personally will need to…HaHa). You definitely put a fresh spin on a topic which has been discussed for many years. Excellent stuff, just great.
After exploring a number of the articles on your web site, I truly like your way of writing a blog. I bookmarked it to my bookmark webpage list and will be checking back soon. Take a look at my web site too and tell me how you feel.
Aw, this was a very good post. Spending some time and actual effort to produce a great article… but what can I say… I hesitate a whole lot and never manage to get anything done.
hairneva
I would like to thank you for the efforts you’ve put in writing this blog. I am hoping to view the same high-grade blog posts from you in the future as well. In truth, your creative writing abilities has encouraged me to get my own, personal site now 😉
Greetings, I do believe your site could possibly be having browser compatibility problems. Whenever I take a look at your website in Safari, it looks fine however, if opening in I.E., it has some overlapping issues. I just wanted to give you a quick heads up! Apart from that, wonderful blog!
You are so awesome! I do not believe I’ve truly read through a single thing like that before. So wonderful to find somebody with a few genuine thoughts on this topic. Seriously.. many thanks for starting this up. This web site is something that is required on the web, someone with a little originality.
This is a topic which is near to my heart… Thank you! Where are your contact details though?
Pretty! This has been an extremely wonderful article. Many thanks for supplying this info.
A motivating discussion is definitely worth comment. I believe that you should publish more about this subject matter, it might not be a taboo matter but generally people do not talk about these issues. To the next! Kind regards.
Right here is the right webpage for anyone who wants to find out about this topic. You know so much its almost hard to argue with you (not that I really would want to…HaHa). You certainly put a brand new spin on a topic that’s been written about for a long time. Excellent stuff, just wonderful.
Good information. Lucky me I recently found your site by accident (stumbleupon). I have saved it for later.
Oh my goodness! Awesome article dude! Thank you so much, However I am encountering problems with your RSS. I don’t know the reason why I cannot subscribe to it. Is there anybody having the same RSS problems? Anyone that knows the solution can you kindly respond? Thanks.
Howdy, I do think your web site might be having web browser compatibility issues. Whenever I take a look at your blog in Safari, it looks fine however when opening in I.E., it’s got some overlapping issues. I just wanted to provide you with a quick heads up! Other than that, fantastic blog.
When I originally left a comment I appear to have clicked on the -Notify me when new comments are added- checkbox and now whenever a comment is added I get 4 emails with the same comment. There has to be an easy method you can remove me from that service? Thanks a lot.
Hello there! This blog post couldn’t be written much better! Looking through this post reminds me of my previous roommate! He constantly kept talking about this. I most certainly will send this information to him. Fairly certain he will have a great read. Many thanks for sharing!
medhair
This is the perfect webpage for anybody who would like to understand this topic. You realize so much its almost hard to argue with you (not that I actually would want to…HaHa). You definitely put a new spin on a topic that’s been discussed for a long time. Wonderful stuff, just wonderful.
You have made some good points there. I checked on the web for more information about the issue and found most people will go along with your views on this site.
Aw, this was an incredibly nice post. Taking the time and actual effort to generate a good article… but what can I say… I hesitate a lot and never seem to get anything done.
After I initially commented I seem to have clicked on the -Notify me when new comments are added- checkbox and now every time a comment is added I get four emails with the exact same comment. There has to be an easy method you can remove me from that service? Cheers.
Excellent blog post. I certainly love this site. Thanks!
I need to to thank you for this good read!! I certainly loved every little bit of it. I have you saved as a favorite to check out new stuff you post…
An outstanding share! I’ve just forwarded this onto a colleague who has been doing a little research on this. And he actually ordered me dinner because I found it for him… lol. So allow me to reword this…. Thanks for the meal!! But yeah, thanks for spending some time to discuss this matter here on your site.
An intriguing discussion is definitely worth comment. I believe that you ought to write more about this issue, it might not be a taboo matter but usually people don’t talk about such subjects. To the next! Many thanks.
Pretty! This was an extremely wonderful post. Thanks for providing this information.
smile
dr terziler
esteworld
dr terziler
Aw, this was a really good post. Taking the time and actual effort to create a superb article… but what can I say… I put things off a whole lot and don’t manage to get nearly anything done.
Very good info. Lucky me I came across your blog by accident (stumbleupon). I have bookmarked it for later!
I’m amazed, I have to admit. Seldom do I encounter a blog that’s equally educative and amusing, and let me tell you, you have hit the nail on the head. The problem is something that not enough people are speaking intelligently about. Now i’m very happy that I stumbled across this in my search for something concerning this.
Hello there, I do believe your blog could be having browser compatibility issues. When I look at your blog in Safari, it looks fine however when opening in Internet Explorer, it’s got some overlapping issues. I simply wanted to give you a quick heads up! Besides that, great blog!
Howdy! I could have sworn I’ve been to this blog before but after reading through some of the post I realized it’s new to me. Nonetheless, I’m definitely delighted I found it and I’ll be bookmarking and checking back frequently!
esteworld
sapphire hair clinic
Excellent article. I definitely love this website. Keep it up!
A motivating discussion is worth comment. I believe that you ought to write more on this issue, it might not be a taboo subject but usually people do not discuss such subjects. To the next! Cheers.
Very nice blog post. I absolutely appreciate this site. Stick with it!
Good information. Lucky me I found your blog by accident (stumbleupon). I’ve saved it for later!
Nice post. I learn something new and challenging on sites I stumbleupon every day. It will always be exciting to read content from other authors and use something from their sites.
I was able to find good info from your blog posts.
I love looking through an article that will make men and women think. Also, thanks for allowing me to comment.
This site was… how do I say it? Relevant!! Finally I’ve found something that helped me. Thank you!
Next time I read a blog, I hope that it doesn’t disappoint me just as much as this one. After all, I know it was my choice to read through, but I really thought you would probably have something useful to say. All I hear is a bunch of crying about something you can fix if you were not too busy searching for attention.
Right here is the perfect website for anybody who wants to understand this topic. You understand so much its almost hard to argue with you (not that I actually would want to…HaHa). You definitely put a new spin on a topic that’s been discussed for many years. Wonderful stuff, just excellent.
Hello there! This post could not be written much better! Reading through this article reminds me of my previous roommate! He constantly kept preaching about this. I’ll forward this post to him. Fairly certain he will have a good read. Thank you for sharing!
I really like reading an article that will make men and women think. Also, many thanks for allowing me to comment.
Everything is very open with a precise description of the challenges. It was definitely informative. Your site is very helpful. Thank you for sharing!
I’m impressed, I have to admit. Rarely do I come across a blog that’s equally educative and engaging, and without a doubt, you have hit the nail on the head. The problem is something which too few folks are speaking intelligently about. I’m very happy I stumbled across this during my search for something regarding this.
This page truly has all the info I needed concerning this subject and didn’t know who to ask.
I’d like to thank you for the efforts you have put in writing this site. I really hope to check out the same high-grade blog posts by you later on as well. In fact, your creative writing abilities has encouraged me to get my own, personal blog now 😉
This is a topic that’s near to my heart… Cheers! Where can I find the contact details for questions?
Having read this I believed it was extremely enlightening. I appreciate you finding the time and energy to put this information together. I once again find myself spending a significant amount of time both reading and leaving comments. But so what, it was still worth it!
You’ve made some good points there. I checked on the internet for more info about the issue and found most people will go along with your views on this site.
I seriously love your site.. Pleasant colors & theme. Did you build this web site yourself? Please reply back as I’m attempting to create my own site and would love to know where you got this from or what the theme is named. Thanks!
bookmarked!!, I love your site!
Great article. I will be going through many of these issues as well..
Hello there! This post couldn’t be written much better! Going through this post reminds me of my previous roommate! He always kept talking about this. I’ll forward this post to him. Pretty sure he’ll have a great read. I appreciate you for sharing!
Aw, this was an extremely nice post. Spending some time and actual effort to produce a great article… but what can I say… I procrastinate a whole lot and don’t seem to get nearly anything done.
Hi, I do believe this is an excellent website. I stumbledupon it 😉 I will return once again since i have saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to help other people.
Everything is very open with a really clear explanation of the issues. It was definitely informative. Your website is useful. Many thanks for sharing!
Having read this I thought it was very informative. I appreciate you finding the time and energy to put this information together. I once again find myself personally spending a lot of time both reading and leaving comments. But so what, it was still worth it.
I blog often and I seriously appreciate your content. Your article has really peaked my interest. I will book mark your blog and keep checking for new information about once a week. I opted in for your Feed as well.
It’s difficult to find knowledgeable people on this subject, however, you seem like you know what you’re talking about! Thanks
I’d like to thank you for the efforts you’ve put in penning this site. I’m hoping to check out the same high-grade blog posts by you later on as well. In fact, your creative writing abilities has inspired me to get my very own website now 😉
Hi, I do think this is a great blog. I stumbledupon it 😉 I am going to come back once again since I bookmarked it. Money and freedom is the greatest way to change, may you be rich and continue to guide other people.
Saved as a favorite, I really like your site!
Good day! I could have sworn I’ve been to this site before but after going through many of the articles I realized it’s new to me. Regardless, I’m certainly pleased I came across it and I’ll be bookmarking it and checking back frequently.
I couldn’t refrain from commenting. Perfectly written.
Hi, I do think this is a great blog. I stumbledupon it 😉 I’m going to revisit yet again since i have book-marked it. Money and freedom is the best way to change, may you be rich and continue to guide others.
This page certainly has all of the info I wanted about this subject and didn’t know who to ask.
No matter if some one searches for his necessary thing,thus he/she wants to be available that in detail, therefore that thing is maintained over here.
Hello.This post was really motivating, particularly since I was looking for thoughts on this issue last Friday.
An outstanding share! I’ve just forwarded this onto a coworker who had been conducting a little homework on this. And he in fact bought me dinner because I found it for him… lol. So let me reword this…. Thank YOU for the meal!! But yeah, thanks for spending time to talk about this matter here on your web page.
Aw, this was a very good post. Spending some time and actual effort to produce a good article… but what can I say… I hesitate a lot and don’t seem to get nearly anything done.
Howdy! This post could not be written any better! Looking at this article reminds me of my previous roommate! He always kept preaching about this. I most certainly will send this article to him. Fairly certain he will have a good read. Thank you for sharing!
Very good information. Lucky me I ran across your blog by accident (stumbleupon). I’ve book-marked it for later.
Oh my goodness! Incredible article dude! Thanks, However I am experiencing problems with your RSS. I don’t know why I can’t subscribe to it. Is there anybody else getting identical RSS issues? Anyone who knows the solution will you kindly respond? Thanks.
I’m extremely pleased to discover this page. I wanted to thank you for ones time for this fantastic read!! I definitely savored every part of it and i also have you bookmarked to see new information on your site.
After looking at a few of the blog posts on your site, I really appreciate your way of blogging. I book-marked it to my bookmark webpage list and will be checking back soon. Please check out my website too and tell me what you think.
Right here is the perfect site for everyone who really wants to find out about this topic. You know so much its almost tough to argue with you (not that I really would want to…HaHa). You definitely put a fresh spin on a topic that’s been written about for years. Excellent stuff, just great.
This site certainly has all the information I wanted about this subject and didn’t know who to ask.
Hi, I believe your site may be having web browser compatibility problems. When I look at your web site in Safari, it looks fine however when opening in I.E., it has some overlapping issues. I merely wanted to provide you with a quick heads up! Apart from that, great blog!
This page really has all the information and facts I wanted concerning this subject and didn’t know who to ask.
This site was… how do you say it? Relevant!! Finally I’ve found something which helped me. Thanks a lot.
That is a very good tip particularly to those fresh to the blogosphere. Short but very accurate info… Thanks for sharing this one. A must read post.
This website was… how do you say it? Relevant!! Finally I have found something which helped me. Cheers.
I seriously love your blog.. Excellent colors & theme. Did you create this site yourself? Please reply back as I’m wanting to create my own blog and would like to know where you got this from or just what the theme is called. Appreciate it.
It’s hard to come by knowledgeable people for this subject, however, you sound like you know what you’re talking about! Thanks
I was able to find good advice from your blog posts.
I blog quite often and I seriously thank you for your content. This article has truly peaked my interest. I’m going to take a note of your site and keep checking for new information about once a week. I subscribed to your Feed too.
I’m very pleased to discover this site. I want to to thank you for your time just for this fantastic read!! I definitely really liked every part of it and I have you saved as a favorite to look at new information on your site.
You made some decent points there. I checked on the net to find out more about the issue and found most individuals will go along with your views on this site.
Good post. I am dealing with many of these issues as well..
Spot on with this write-up, I absolutely feel this web site needs much more attention. I’ll probably be returning to read through more, thanks for the information.
An intriguing discussion is worth comment. There’s no doubt that that you should publish more on this topic, it might not be a taboo subject but generally people don’t talk about these issues. To the next! Many thanks!
Hi, I do think this is an excellent site. I stumbledupon it 😉 I’m going to come back once again since i have book marked it. Money and freedom is the best way to change, may you be rich and continue to help other people.
I really love your blog.. Pleasant colors & theme. Did you develop this website yourself? Please reply back as I’m hoping to create my very own website and would like to find out where you got this from or exactly what the theme is called. Thank you!
You ought to take part in a contest for one of the best blogs on the internet. I will highly recommend this blog!
I’m very pleased to find this great site. I need to to thank you for your time for this wonderful read!! I definitely really liked every part of it and I have you book marked to look at new information on your site.
There is certainly a lot to find out about this issue. I like all of the points you have made.
May I simply just say what a comfort to discover somebody who genuinely understands what they’re talking about on the net. You certainly understand how to bring a problem to light and make it important. More people ought to check this out and understand this side of your story. It’s surprising you’re not more popular given that you surely possess the gift.
Spot on with this write-up, I seriously believe this site needs much more attention. I’ll probably be back again to read through more, thanks for the advice.
Everything is very open with a very clear clarification of the issues. It was really informative. Your site is extremely helpful. Thank you for sharing!
You made some good points there. I looked on the web for additional information about the issue and found most people will go along with your views on this site.
Hello there! I could have sworn I’ve visited this blog before but after going through a few of the posts I realized it’s new to me. Anyways, I’m certainly delighted I discovered it and I’ll be book-marking it and checking back often.
It’s hard to come by educated people for this topic, however, you sound like you know what you’re talking about! Thanks
You have made some really good points there. I looked on the internet to learn more about the issue and found most individuals will go along with your views on this site.
This is a topic that is close to my heart… Thank you! Exactly where can I find the contact details for questions?
You’re so awesome! I don’t think I have read through something like that before. So wonderful to discover someone with unique thoughts on this subject. Seriously.. thank you for starting this up. This website is something that is needed on the web, someone with a little originality.
Aw, this was a very nice post. Finding the time and actual effort to create a superb article… but what can I say… I procrastinate a whole lot and don’t manage to get nearly anything done.
An outstanding share! I’ve just forwarded this onto a friend who has been doing a little homework on this. And he actually bought me breakfast because I discovered it for him… lol. So allow me to reword this…. Thanks for the meal!! But yeah, thanx for spending time to discuss this issue here on your website.
bookmarked!!, I love your blog!
The next time I read a blog, Hopefully it does not disappoint me as much as this particular one. After all, Yes, it was my choice to read through, however I genuinely believed you would have something interesting to talk about. All I hear is a bunch of complaining about something that you could fix if you weren’t too busy looking for attention.
Excellent post. I’m experiencing some of these issues as well..
I would like to thank you for the efforts you’ve put in penning this site. I’m hoping to view the same high-grade blog posts from you later on as well. In fact, your creative writing abilities has encouraged me to get my very own site now 😉
Greetings! Very useful advice in this particular article! It’s the little changes that will make the biggest changes. Thanks for sharing!
This site was… how do you say it? Relevant!! Finally I’ve found something that helped me. Thank you!
Everyone loves it when folks get together and share opinions. Great website, keep it up!
Oh my goodness! Amazing article dude! Thank you, However I am experiencing troubles with your RSS. I don’t know the reason why I am unable to subscribe to it. Is there anyone else getting similar RSS issues? Anybody who knows the answer can you kindly respond? Thanx.
I truly love your blog.. Pleasant colors & theme. Did you create this web site yourself? Please reply back as I’m attempting to create my very own website and would like to know where you got this from or exactly what the theme is named. Thanks!
Spot on with this write-up, I actually feel this site needs far more attention. I’ll probably be back again to see more, thanks for the info!
Excellent blog you’ve got here.. It’s difficult to find good quality writing like yours these days. I honestly appreciate people like you! Take care!!
I couldn’t refrain from commenting. Well written.
You’ve made some good points there. I checked on the internet for more info about the issue and found most individuals will go along with your views on this site.
Having read this I thought it was extremely enlightening. I appreciate you finding the time and energy to put this content together. I once again find myself spending a significant amount of time both reading and commenting. But so what, it was still worth it!
May I simply just say what a relief to find someone that genuinely understands what they are discussing over the internet. You certainly realize how to bring an issue to light and make it important. A lot more people must read this and understand this side of the story. It’s surprising you aren’t more popular since you definitely have the gift.
Greetings! Very helpful advice in this particular post! It is the little changes that will make the largest changes. Many thanks for sharing!
I blog often and I genuinely thank you for your information. The article has truly peaked my interest. I’m going to take a note of your website and keep checking for new details about once a week. I opted in for your RSS feed as well.
Having read this I thought it was rather enlightening. I appreciate you taking the time and energy to put this article together. I once again find myself personally spending way too much time both reading and commenting. But so what, it was still worth it!
After I initially left a comment I seem to have clicked the -Notify me when new comments are added- checkbox and from now on each time a comment is added I recieve 4 emails with the same comment. There has to be a way you are able to remove me from that service? Appreciate it.
Hello! I simply wish to offer you a huge thumbs up for the great information you’ve got right here on this post. I will be coming back to your blog for more soon.
Good day! I could have sworn I’ve visited this web site before but after looking at some of the articles I realized it’s new to me. Nonetheless, I’m definitely happy I stumbled upon it and I’ll be book-marking it and checking back often.
This is a good tip especially to those new to the blogosphere. Short but very precise info… Thank you for sharing this one. A must read post!
It’s hard to find experienced people on this subject, but you sound like you know what you’re talking about! Thanks
After looking over a few of the blog articles on your site, I truly appreciate your way of writing a blog. I saved as a favorite it to my bookmark webpage list and will be checking back soon. Please visit my website too and tell me what you think.
Oh my goodness! Incredible article dude! Many thanks, However I am going through troubles with your RSS. I don’t understand why I cannot subscribe to it. Is there anyone else having identical RSS issues? Anybody who knows the solution can you kindly respond? Thanks!
Greetings! Very helpful advice within this article! It’s the little changes which will make the largest changes. Many thanks for sharing!
Hi there! I simply want to give you a huge thumbs up for the great info you have right here on this post. I am coming back to your web site for more soon.
When I initially left a comment I appear to have clicked on the -Notify me when new comments are added- checkbox and now each time a comment is added I recieve four emails with the same comment. Is there a means you are able to remove me from that service? Thank you.
Nice post. I learn something totally new and challenging on websites I stumbleupon everyday. It will always be interesting to read articles from other writers and practice a little something from their sites.
Having read this I thought it was really enlightening. I appreciate you spending some time and effort to put this article together. I once again find myself personally spending a significant amount of time both reading and posting comments. But so what, it was still worthwhile!
Aw, this was an incredibly good post. Spending some time and actual effort to produce a superb article… but what can I say… I put things off a whole lot and don’t seem to get nearly anything done.
Hello! I could have sworn I’ve visited your blog before but after browsing through many of the articles I realized it’s new to me. Anyhow, I’m definitely delighted I found it and I’ll be book-marking it and checking back frequently!
It’s difficult to find knowledgeable people for this topic, but you seem like you know what you’re talking about! Thanks
Everything is very open with a very clear clarification of the challenges. It was really informative. Your site is very useful. Thank you for sharing.
I needed to thank you for this wonderful read!! I absolutely enjoyed every bit of it. I have got you bookmarked to check out new stuff you post…
Spot on with this write-up, I really think this web site needs a lot more attention. I’ll probably be returning to read more, thanks for the advice.
It’s difficult to find knowledgeable people on this subject, however, you seem like you know what you’re talking about! Thanks
Hello! I simply would like to give you a big thumbs up for the excellent information you have got right here on this post. I am returning to your web site for more soon.
I could not resist commenting. Very well written!
I like reading through an article that will make people think. Also, thank you for permitting me to comment.
I’m amazed, I must say. Rarely do I encounter a blog that’s both educative and engaging, and let me tell you, you’ve hit the nail on the head. The issue is something which too few people are speaking intelligently about. I am very happy I came across this during my search for something regarding this.
Right here is the perfect site for everyone who would like to find out about this topic. You know so much its almost tough to argue with you (not that I personally will need to…HaHa). You certainly put a brand new spin on a subject that’s been written about for ages. Great stuff, just wonderful.
I really like it whenever people come together and share views. Great blog, continue the good work!
Having read this I believed it was extremely informative. I appreciate you finding the time and effort to put this article together. I once again find myself personally spending a significant amount of time both reading and commenting. But so what, it was still worthwhile.
Spot on with this write-up, I honestly think this amazing site needs far more attention. I’ll probably be back again to read more, thanks for the info!
Pretty! This was an incredibly wonderful article. Thank you for supplying this info.
Hi there! This post could not be written much better! Reading through this post reminds me of my previous roommate! He continually kept preaching about this. I will forward this information to him. Pretty sure he will have a good read. Many thanks for sharing!
Very good post. I am dealing with some of these issues as well..
This page truly has all of the information I wanted concerning this subject and didn’t know who to ask.
A fascinating discussion is definitely worth comment. I do think that you should write more about this subject, it might not be a taboo matter but typically people don’t speak about such subjects. To the next! Cheers!
After looking over a number of the articles on your web page, I really appreciate your technique of blogging. I book marked it to my bookmark site list and will be checking back soon. Take a look at my website as well and tell me your opinion.
This website really has all of the info I wanted concerning this subject and didn’t know who to ask.
I’m impressed, I must say. Rarely do I encounter a blog that’s both equally educative and engaging, and without a doubt, you’ve hit the nail on the head. The problem is something which too few men and women are speaking intelligently about. I’m very happy that I came across this in my search for something concerning this.
Oh my goodness! Awesome article dude! Thanks, However I am encountering troubles with your RSS. I don’t understand why I can’t subscribe to it. Is there anybody getting similar RSS problems? Anyone that knows the solution can you kindly respond? Thanx.
Aw, this was a really nice post. Taking the time and actual effort to make a very good article… but what can I say… I hesitate a whole lot and don’t seem to get nearly anything done.
There’s definately a great deal to find out about this topic. I love all of the points you made.
Very good write-up. I definitely appreciate this site. Stick with it!
Oh my goodness! Amazing article dude! Thank you, However I am encountering difficulties with your RSS. I don’t know the reason why I can’t join it. Is there anybody else getting similar RSS problems? Anybody who knows the solution will you kindly respond? Thanx!
I like it whenever people get together and share ideas. Great website, keep it up!
I wanted to thank you for this excellent read!! I definitely enjoyed every bit of it. I have got you book-marked to check out new stuff you post…
Way cool! Some extremely valid points! I appreciate you writing this write-up and the rest of the site is also very good.
Hi there, I think your blog could be having browser compatibility problems. Whenever I take a look at your site in Safari, it looks fine however, when opening in IE, it’s got some overlapping issues. I merely wanted to provide you with a quick heads up! Other than that, wonderful website.
Great blog you have got here.. It’s hard to find good quality writing like yours nowadays. I truly appreciate people like you! Take care!!
Oh my goodness! Amazing article dude! Thanks, However I am having issues with your RSS. I don’t know the reason why I can’t subscribe to it. Is there anybody getting similar RSS problems? Anybody who knows the answer will you kindly respond? Thanks.
Saved as a favorite, I like your web site!
Good web site you have got here.. It’s difficult to find good quality writing like yours nowadays. I truly appreciate people like you! Take care!!
Very nice write-up. I absolutely love this site. Thanks!
When I originally left a comment I appear to have clicked on the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I receive 4 emails with the same comment. Is there a way you are able to remove me from that service? Appreciate it.
Great web site you have here.. It’s difficult to find high-quality writing like yours nowadays. I truly appreciate people like you! Take care!!
Hi there! I simply would like to offer you a big thumbs up for the great information you’ve got right here on this post. I am coming back to your web site for more soon.
I’m amazed, I must say. Rarely do I come across a blog that’s both equally educative and interesting, and without a doubt, you have hit the nail on the head. The problem is something that too few folks are speaking intelligently about. Now i’m very happy I found this in my hunt for something relating to this.
This web site certainly has all the info I wanted concerning this subject and didn’t know who to ask.
Hello! I could have sworn I’ve been to this site before but after going through some of the articles I realized it’s new to me. Anyhow, I’m certainly happy I came across it and I’ll be bookmarking it and checking back frequently!
Great information. Lucky me I found your website by chance (stumbleupon). I have bookmarked it for later!
Good day! I could have sworn I’ve visited this website before but after browsing through many of the articles I realized it’s new to me. Nonetheless, I’m certainly pleased I stumbled upon it and I’ll be book-marking it and checking back frequently.
Good post. I learn something totally new and challenging on websites I stumbleupon everyday. It will always be interesting to read content from other authors and practice a little something from other web sites.
Hi, I do believe this is an excellent web site. I stumbledupon it 😉 I may return once again since I book-marked it. Money and freedom is the greatest way to change, may you be rich and continue to help others.
I’m impressed, I must say. Seldom do I come across a blog that’s equally educative and interesting, and let me tell you, you have hit the nail on the head. The problem is something too few folks are speaking intelligently about. I’m very happy I found this in my hunt for something regarding this.
After I originally left a comment I seem to have clicked on the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I get four emails with the exact same comment. There has to be a means you are able to remove me from that service? Appreciate it.
I really love your site.. Pleasant colors & theme. Did you develop this amazing site yourself? Please reply back as I’m wanting to create my very own blog and would love to find out where you got this from or just what the theme is named. Appreciate it.
Very good article. I certainly appreciate this website. Keep it up!
Nice post. I learn something new and challenging on sites I stumbleupon every day. It’s always useful to read through articles from other authors and use something from other websites.
Hello there! I simply wish to give you a big thumbs up for your excellent information you have right here on this post. I will be returning to your blog for more soon.
Aw, this was an extremely good post. Finding the time and actual effort to produce a superb article… but what can I say… I procrastinate a lot and never seem to get anything done.
Having read this I believed it was extremely enlightening. I appreciate you taking the time and effort to put this content together. I once again find myself spending a significant amount of time both reading and commenting. But so what, it was still worth it!
Hi there, I do think your web site may be having web browser compatibility issues. When I look at your website in Safari, it looks fine however, when opening in I.E., it has some overlapping issues. I merely wanted to provide you with a quick heads up! Apart from that, wonderful site!
You ought to take part in a contest for one of the best blogs on the internet. I will highly recommend this blog!
Great information. Lucky me I discovered your site by chance (stumbleupon). I have book-marked it for later.
Hi there! This post could not be written much better! Looking at this post reminds me of my previous roommate! He always kept talking about this. I am going to forward this information to him. Pretty sure he will have a good read. Thank you for sharing!
Very good post. I am going through a few of these issues as well..
A fascinating discussion is worth comment. I do believe that you should publish more about this subject matter, it may not be a taboo subject but typically people do not talk about such subjects. To the next! Many thanks!
After looking over a number of the blog articles on your web page, I truly appreciate your way of writing a blog. I added it to my bookmark website list and will be checking back in the near future. Please check out my web site as well and tell me how you feel.
This is the perfect webpage for anyone who wants to find out about this topic. You realize a whole lot its almost hard to argue with you (not that I really will need to…HaHa). You definitely put a fresh spin on a subject that has been written about for decades. Excellent stuff, just wonderful.
Oh my goodness! Awesome article dude! Thank you so much, However I am encountering problems with your RSS. I don’t understand the reason why I cannot join it. Is there anybody else having the same RSS problems? Anyone that knows the answer can you kindly respond? Thanx!!
Hello, I do believe your website could possibly be having web browser compatibility issues. When I take a look at your site in Safari, it looks fine however, when opening in IE, it’s got some overlapping issues. I simply wanted to give you a quick heads up! Besides that, wonderful site.
Hi, I do think this is a great blog. I stumbledupon it 😉 I may return yet again since I bookmarked it. Money and freedom is the best way to change, may you be rich and continue to help others.
Right here is the right site for anyone who wants to find out about this topic. You understand a whole lot its almost hard to argue with you (not that I really would want to…HaHa). You certainly put a new spin on a subject which has been written about for decades. Excellent stuff, just great.
Oh my goodness! Awesome article dude! Thank you, However I am going through difficulties with your RSS. I don’t understand the reason why I am unable to subscribe to it. Is there anybody having identical RSS issues? Anyone who knows the solution can you kindly respond? Thanks!!
The next time I read a blog, I hope that it doesn’t fail me just as much as this particular one. I mean, Yes, it was my choice to read, but I actually thought you’d have something useful to say. All I hear is a bunch of whining about something you can fix if you weren’t too busy seeking attention.
You’re so awesome! I don’t suppose I have read a single thing like that before. So great to discover another person with some genuine thoughts on this subject matter. Seriously.. many thanks for starting this up. This site is something that is required on the internet, someone with some originality.
Greetings, There’s no doubt that your web site could possibly be having browser compatibility problems. Whenever I take a look at your blog in Safari, it looks fine but when opening in IE, it has some overlapping issues. I simply wanted to give you a quick heads up! Besides that, great blog.
I seriously love your site.. Great colors & theme. Did you build this site yourself? Please reply back as I’m looking to create my own personal site and would like to know where you got this from or just what the theme is named. Kudos.
Everyone loves it when people get together and share ideas. Great site, continue the good work!
Spot on with this write-up, I honestly feel this site needs much more attention. I’ll probably be returning to read through more, thanks for the information.
I absolutely love your blog.. Pleasant colors & theme. Did you create this amazing site yourself? Please reply back as I’m wanting to create my own personal site and would like to find out where you got this from or exactly what the theme is named. Thank you!
I seriously love your website.. Very nice colors & theme. Did you create this web site yourself? Please reply back as I’m hoping to create my own personal site and would like to know where you got this from or exactly what the theme is named. Cheers!
You made some decent points there. I checked on the web for additional information about the issue and found most people will go along with your views on this web site.
You should be a part of a contest for one of the greatest sites on the net. I will highly recommend this blog!
You’re so cool! I don’t think I have read anything like this before. So nice to find another person with some genuine thoughts on this topic. Really.. thanks for starting this up. This site is one thing that is required on the web, someone with some originality.
After going over a few of the blog articles on your site, I truly appreciate your technique of writing a blog. I added it to my bookmark webpage list and will be checking back in the near future. Take a look at my web site as well and let me know your opinion.
Hello, I think your blog might be having web browser compatibility issues. Whenever I look at your blog in Safari, it looks fine however, when opening in I.E., it has some overlapping issues. I just wanted to provide you with a quick heads up! Other than that, great blog.
Everything is very open with a very clear description of the issues. It was really informative. Your site is very useful. Thank you for sharing!
Everything is very open with a really clear explanation of the challenges. It was truly informative. Your site is useful. Thank you for sharing.
This page definitely has all the info I needed about this subject and didn’t know who to ask.
I’d like to thank you for the efforts you have put in writing this website. I really hope to see the same high-grade content by you later on as well. In fact, your creative writing abilities has motivated me to get my own website now 😉
Very nice post. I absolutely appreciate this website. Thanks!
You’ve made some really good points there. I looked on the web to learn more about the issue and found most people will go along with your views on this site.
I must thank you for the efforts you have put in penning this blog. I really hope to view the same high-grade blog posts by you in the future as well. In fact, your creative writing abilities has inspired me to get my own, personal site now 😉
A fascinating discussion is definitely worth comment. I do believe that you should publish more about this topic, it may not be a taboo subject but generally people do not talk about these issues. To the next! Many thanks!
This is a topic which is close to my heart… Many thanks! Exactly where can I find the contact details for questions?
Great article. I’m dealing with many of these issues as well..
Everything is very open with a really clear explanation of the challenges. It was definitely informative. Your site is very helpful. Many thanks for sharing!
After I initially left a comment I seem to have clicked on the -Notify me when new comments are added- checkbox and from now on each time a comment is added I receive 4 emails with the same comment. There has to be a way you are able to remove me from that service? Cheers.
The next time I read a blog, Hopefully it doesn’t fail me just as much as this particular one. I mean, Yes, it was my choice to read through, nonetheless I really thought you would probably have something useful to talk about. All I hear is a bunch of whining about something that you could fix if you were not too busy searching for attention.
Greetings! Very helpful advice in this particular post! It is the little changes that will make the most important changes. Thanks for sharing!
May I simply say what a comfort to discover someone who truly knows what they are talking about on the web. You actually realize how to bring a problem to light and make it important. More and more people ought to read this and understand this side of your story. I can’t believe you are not more popular since you surely possess the gift.
The very next time I read a blog, Hopefully it doesn’t disappoint me as much as this particular one. After all, Yes, it was my choice to read through, however I really believed you would probably have something useful to talk about. All I hear is a bunch of crying about something that you could possibly fix if you weren’t too busy seeking attention.
That is a great tip especially to those new to the blogosphere. Brief but very accurate information… Many thanks for sharing this one. A must read post!
Good site you have got here.. It’s hard to find high quality writing like yours nowadays. I really appreciate individuals like you! Take care!!
Way cool! Some very valid points! I appreciate you writing this article plus the rest of the site is really good.
You’re so awesome! I don’t believe I’ve truly read through anything like this before. So great to discover another person with a few genuine thoughts on this subject. Seriously.. many thanks for starting this up. This web site is one thing that’s needed on the internet, someone with a bit of originality.
After looking over a number of the blog posts on your site, I honestly like your way of writing a blog. I added it to my bookmark site list and will be checking back soon. Please check out my web site too and let me know what you think.
That is a very good tip especially to those fresh to the blogosphere. Brief but very precise info… Thank you for sharing this one. A must read article!
I’m very happy to discover this web site. I need to to thank you for your time just for this wonderful read!! I definitely enjoyed every part of it and i also have you book marked to check out new stuff on your web site.
Excellent article. I certainly appreciate this website. Keep writing!
This site truly has all the information I wanted concerning this subject and didn’t know who to ask.
This is a topic that is close to my heart… Cheers! Exactly where are your contact details though?
An impressive share! I have just forwarded this onto a friend who was conducting a little homework on this. And he in fact bought me breakfast because I stumbled upon it for him… lol. So allow me to reword this…. Thanks for the meal!! But yeah, thanks for spending some time to discuss this issue here on your blog.
Spot on with this write-up, I seriously feel this website needs much more attention. I’ll probably be back again to read through more, thanks for the advice.
This is a topic which is near to my heart… Thank you! Exactly where can I find the contact details for questions?
Good post! We are linking to this great content on our website. Keep up the good writing.
This website definitely has all the information and facts I wanted about this subject and didn’t know who to ask.
I could not refrain from commenting. Well written!
Pretty! This has been a really wonderful article. Many thanks for supplying this info.
I enjoy reading through an article that will make men and women think. Also, thanks for allowing me to comment.
Greetings! Very useful advice within this post! It’s the little changes which will make the largest changes. Many thanks for sharing!
Pretty! This has been an incredibly wonderful post. Thank you for supplying these details.
Aw, this was a very nice post. Taking a few minutes and actual effort to create a top notch article… but what can I say… I put things off a whole lot and never seem to get nearly anything done.
I’d like to thank you for the efforts you have put in writing this site. I’m hoping to see the same high-grade content from you later on as well. In truth, your creative writing abilities has inspired me to get my very own site now 😉
Very good post. I’m dealing with some of these issues as well..
I really love your blog.. Very nice colors & theme. Did you build this amazing site yourself? Please reply back as I’m looking to create my very own website and would love to learn where you got this from or what the theme is called. Kudos!
Good post. I am facing some of these issues as well..
Spot on with this write-up, I absolutely believe that this amazing site needs much more attention. I’ll probably be returning to see more, thanks for the info.
This website was… how do I say it? Relevant!! Finally I’ve found something which helped me. Kudos.
Hi, I do believe your web site might be having browser compatibility problems. When I take a look at your web site in Safari, it looks fine however, when opening in I.E., it has some overlapping issues. I simply wanted to provide you with a quick heads up! Other than that, wonderful blog!
Hi, I believe your web site might be having web browser compatibility issues. When I take a look at your site in Safari, it looks fine however, if opening in IE, it has some overlapping issues. I just wanted to give you a quick heads up! Other than that, great website!
Way cool! Some extremely valid points! I appreciate you penning this article and also the rest of the site is also very good.
After I originally left a comment I appear to have clicked the -Notify me when new comments are added- checkbox and from now on every time a comment is added I recieve four emails with the exact same comment. Perhaps there is a way you are able to remove me from that service? Thanks a lot.
I like reading a post that will make men and women think. Also, thanks for allowing me to comment.
Good post. I learn something new and challenging on blogs I stumbleupon everyday. It will always be interesting to read articles from other writers and practice a little something from other web sites.
I couldn’t resist commenting. Perfectly written.
You’re so interesting! I don’t think I have read through something like this before. So wonderful to find another person with a few unique thoughts on this subject. Seriously.. thanks for starting this up. This site is something that is required on the internet, someone with some originality.
Everything is very open with a very clear clarification of the issues. It was really informative. Your site is very helpful. Thanks for sharing.
Spot on with this write-up, I seriously believe that this amazing site needs far more attention. I’ll probably be returning to read more, thanks for the info.
You made some really good points there. I looked on the net for more info about the issue and found most individuals will go along with your views on this website.
When I originally commented I appear to have clicked the -Notify me when new comments are added- checkbox and from now on each time a comment is added I recieve four emails with the same comment. Is there an easy method you are able to remove me from that service? Thanks a lot.
I used to be able to find good info from your blog posts.
This site was… how do you say it? Relevant!! Finally I’ve found something which helped me. Kudos!
Aw, this was a very nice post. Taking a few minutes and actual effort to generate a top notch article… but what can I say… I procrastinate a lot and never manage to get nearly anything done.
I used to be able to find good info from your articles.
Hi! I simply would like to offer you a huge thumbs up for the excellent info you have got here on this post. I’ll be returning to your website for more soon.
Aw, this was a really nice post. Finding the time and actual effort to create a superb article… but what can I say… I hesitate a whole lot and never seem to get anything done.
I really like it whenever people get together and share views. Great blog, continue the good work.
Next time I read a blog, I hope that it does not disappoint me as much as this particular one. After all, I know it was my choice to read, nonetheless I truly thought you would probably have something interesting to talk about. All I hear is a bunch of crying about something that you could possibly fix if you weren’t too busy looking for attention.
This site was… how do I say it? Relevant!! Finally I’ve found something that helped me. Thanks.
You need to take part in a contest for one of the greatest websites on the internet. I am going to recommend this website!
Aw, this was an extremely good post. Finding the time and actual effort to produce a superb article… but what can I say… I hesitate a whole lot and never manage to get nearly anything done.
Pretty! This has been a really wonderful post. Thank you for supplying this information.
I’d like to thank you for the efforts you’ve put in writing this website. I’m hoping to view the same high-grade blog posts by you in the future as well. In truth, your creative writing abilities has motivated me to get my own, personal site now 😉
May I just say what a comfort to discover someone who actually knows what they’re discussing online. You actually realize how to bring an issue to light and make it important. A lot more people need to look at this and understand this side of your story. I was surprised you are not more popular given that you most certainly possess the gift.
This site was… how do I say it? Relevant!! Finally I have found something that helped me. Cheers.
Good post. I definitely love this site. Thanks!
I have to thank you for the efforts you’ve put in writing this website. I am hoping to see the same high-grade blog posts by you in the future as well. In truth, your creative writing abilities has encouraged me to get my own, personal website now 😉
Good information. Lucky me I found your site by accident (stumbleupon). I’ve saved as a favorite for later!
Hi, I do think this is a great web site. I stumbledupon it 😉 I’m going to return once again since I book marked it. Money and freedom is the best way to change, may you be rich and continue to guide others.
This page truly has all of the information and facts I needed concerning this subject and didn’t know who to ask.
Very good post. I am dealing with a few of these issues as well..
Good post. I learn something totally new and challenging on sites I stumbleupon everyday. It’s always useful to read articles from other writers and practice a little something from other web sites.
Good day! I simply want to offer you a big thumbs up for your excellent information you have got here on this post. I’ll be coming back to your blog for more soon.
Pretty! This was an extremely wonderful article. Thanks for providing these details.
Everything is very open with a clear explanation of the challenges. It was really informative. Your site is very useful. Thanks for sharing!
Right here is the right blog for anybody who hopes to find out about this topic. You realize a whole lot its almost hard to argue with you (not that I really will need to…HaHa). You definitely put a fresh spin on a subject that’s been discussed for years. Great stuff, just great.
I love it when individuals come together and share opinions. Great website, keep it up.
Very good info. Lucky me I found your blog by chance (stumbleupon). I have bookmarked it for later!
Hi there! This post couldn’t be written any better! Looking through this article reminds me of my previous roommate! He continually kept preaching about this. I’ll forward this information to him. Pretty sure he’s going to have a great read. I appreciate you for sharing!
You’re so interesting! I don’t believe I’ve read something like that before. So good to discover another person with genuine thoughts on this subject. Really.. many thanks for starting this up. This website is something that is required on the web, someone with a little originality.
Excellent post. I am facing a few of these issues as well..
Right here is the right site for everyone who wants to find out about this topic. You realize so much its almost hard to argue with you (not that I personally would want to…HaHa). You definitely put a new spin on a subject that’s been written about for ages. Wonderful stuff, just excellent.
This is the perfect web site for anyone who wishes to understand this topic. You know so much its almost tough to argue with you (not that I really will need to…HaHa). You certainly put a new spin on a topic that has been written about for a long time. Great stuff, just wonderful.
Oh my goodness! Incredible article dude! Thanks, However I am going through issues with your RSS. I don’t know the reason why I can’t join it. Is there anyone else getting identical RSS issues? Anybody who knows the solution can you kindly respond? Thanx!!
Everyone loves it when people come together and share opinions. Great site, stick with it!
Spot on with this write-up, I actually believe this site needs a great deal more attention. I’ll probably be back again to see more, thanks for the info!
An impressive share! I have just forwarded this onto a colleague who was conducting a little homework on this. And he in fact bought me lunch simply because I found it for him… lol. So allow me to reword this…. Thank YOU for the meal!! But yeah, thanks for spending the time to discuss this subject here on your web page.
I used to be able to find good information from your blog posts.
I could not refrain from commenting. Very well written!
Aw, this was an extremely good post. Taking the time and actual effort to make a very good article… but what can I say… I procrastinate a whole lot and don’t seem to get anything done.
The very next time I read a blog, I hope that it doesn’t fail me as much as this one. I mean, Yes, it was my choice to read through, but I actually believed you’d have something helpful to say. All I hear is a bunch of whining about something that you could fix if you were not too busy seeking attention.
This is a topic that’s close to my heart… Take care! Where are your contact details though?
Greetings! Very helpful advice within this post! It is the little changes that produce the biggest changes. Thanks a lot for sharing!
Saved as a favorite, I like your web site.
Excellent article. I am dealing with many of these issues as well..
You are so cool! I don’t believe I have read something like that before. So nice to find someone with original thoughts on this topic. Seriously.. thank you for starting this up. This site is one thing that’s needed on the web, someone with a bit of originality.
You should be a part of a contest for one of the best websites online. I most certainly will recommend this web site!
I could not resist commenting. Exceptionally well written.
I needed to thank you for this wonderful read!! I certainly enjoyed every bit of it. I have you saved as a favorite to look at new things you post…
The next time I read a blog, I hope that it doesn’t fail me just as much as this one. After all, Yes, it was my choice to read through, however I truly thought you’d have something interesting to talk about. All I hear is a bunch of moaning about something that you can fix if you weren’t too busy searching for attention.
Spot on with this write-up, I honestly believe that this site needs much more attention. I’ll probably be back again to read through more, thanks for the info!
This is a topic that is close to my heart… Cheers! Where can I find the contact details for questions?
Greetings! Very useful advice in this particular post! It is the little changes that make the biggest changes. Thanks for sharing!
Excellent post. I certainly love this website. Continue the good work!
I was able to find good info from your blog posts.
You are so interesting! I do not believe I’ve truly read anything like that before. So great to find someone with some genuine thoughts on this issue. Really.. thank you for starting this up. This web site is one thing that is needed on the internet, someone with a bit of originality.
Excellent article. I’m experiencing many of these issues as well..
Spot on with this write-up, I really feel this web site needs a lot more attention. I’ll probably be returning to read more, thanks for the information.
Next time I read a blog, Hopefully it does not fail me just as much as this particular one. I mean, I know it was my choice to read, but I really thought you’d have something useful to say. All I hear is a bunch of moaning about something you can fix if you were not too busy looking for attention.
Hello, I think your web site could possibly be having browser compatibility issues. When I take a look at your blog in Safari, it looks fine however when opening in Internet Explorer, it’s got some overlapping issues. I merely wanted to provide you with a quick heads up! Besides that, excellent website.
An impressive share! I have just forwarded this onto a colleague who has been doing a little homework on this. And he in fact bought me breakfast simply because I discovered it for him… lol. So allow me to reword this…. Thank YOU for the meal!! But yeah, thanx for spending time to discuss this topic here on your internet site.
You’re so interesting! I do not suppose I’ve truly read through anything like that before. So great to discover another person with original thoughts on this subject. Really.. thanks for starting this up. This site is something that’s needed on the web, someone with a little originality.
Hi, I do think this is a great blog. I stumbledupon it 😉 I may revisit once again since I book marked it. Money and freedom is the best way to change, may you be rich and continue to help other people.
Good post. I learn something totally new and challenging on sites I stumbleupon everyday. It will always be exciting to read articles from other writers and use something from their sites.
I was more than happy to discover this web site. I wanted to thank you for your time for this particularly fantastic read!! I definitely savored every bit of it and i also have you book-marked to look at new things in your site.
There is certainly a great deal to find out about this subject. I love all of the points you’ve made.
I blog frequently and I truly appreciate your information. This great article has truly peaked my interest. I’m going to bookmark your site and keep checking for new information about once a week. I opted in for your Feed as well.
I need to to thank you for this excellent read!! I definitely enjoyed every bit of it. I have got you bookmarked to check out new things you post…
After going over a handful of the articles on your blog, I honestly like your technique of blogging. I saved as a favorite it to my bookmark site list and will be checking back in the near future. Take a look at my web site as well and tell me your opinion.
I’m impressed, I have to admit. Seldom do I encounter a blog that’s both educative and amusing, and without a doubt, you have hit the nail on the head. The problem is something that not enough people are speaking intelligently about. I am very happy that I stumbled across this in my search for something regarding this.
Good day! I just want to give you a huge thumbs up for the excellent information you have got here on this post. I am coming back to your site for more soon.
I really like reading through an article that can make men and women think. Also, thank you for allowing for me to comment.
Thanks a lot for the blog article.Much thanks again. Fantastic.
You are so awesome! I don’t think I’ve read through anything like that before. So great to discover somebody with some genuine thoughts on this topic. Really.. thanks for starting this up. This web site is one thing that is required on the web, someone with a little originality.
This site truly has all the information and facts I wanted concerning this subject and didn’t know who to ask.
That is a very good tip particularly to those fresh to the blogosphere. Short but very accurate info… Thanks for sharing this one. A must read article.
This site definitely has all of the information I needed about this subject and didn’t know who to ask.
I absolutely love your website.. Great colors & theme. Did you create this site yourself? Please reply back as I’m looking to create my own personal site and want to know where you got this from or exactly what the theme is named. Kudos.
Hi! I simply would like to give you a big thumbs up for the great info you’ve got right here on this post. I am coming back to your site for more soon.
Pretty! This was a really wonderful article. Thanks for providing this information.
Aw, this was a really nice post. Taking a few minutes and actual effort to make a very good article… but what can I say… I put things off a whole lot and don’t seem to get anything done.
When I initially left a comment I appear to have clicked the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I recieve 4 emails with the exact same comment. Perhaps there is a way you are able to remove me from that service? Thank you.
Really enjoyed this article.Thanks Again. Fantastic.
I’d like to thank you for the efforts you’ve put in writing this blog. I’m hoping to see the same high-grade content from you in the future as well. In fact, your creative writing abilities has motivated me to get my own site now 😉
Your style is so unique compared to other folks I’ve read stuff from. Thank you for posting when you have the opportunity, Guess I’ll just book mark this site.
I like looking through an article that can make people think. Also, thanks for allowing me to comment.
You’ve made some really good points there. I checked on the internet for more info about the issue and found most people will go along with your views on this web site.
An outstanding share! I’ve just forwarded this onto a friend who had been doing a little homework on this. And he actually ordered me breakfast due to the fact that I found it for him… lol. So let me reword this…. Thank YOU for the meal!! But yeah, thanks for spending some time to talk about this issue here on your blog.
Good post. I learn something new and challenging on sites I stumbleupon on a daily basis. It will always be interesting to read articles from other authors and use a little something from their web sites.
When I originally left a comment I appear to have clicked the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I get four emails with the same comment. There has to be a means you are able to remove me from that service? Many thanks.
I want to to thank you for this very good read!! I certainly loved every little bit of it. I have got you book-marked to look at new things you post…
An outstanding share! I have just forwarded this onto a coworker who was conducting a little research on this. And he in fact ordered me dinner because I stumbled upon it for him… lol. So let me reword this…. Thanks for the meal!! But yeah, thanx for spending some time to discuss this subject here on your site.
Aw, this was a really nice post. Finding the time and actual effort to make a really good article… but what can I say… I procrastinate a lot and don’t manage to get anything done.
I seriously love your website.. Excellent colors & theme. Did you make this amazing site yourself? Please reply back as I’m planning to create my own website and would like to know where you got this from or exactly what the theme is called. Cheers.
Everyone loves it when people get together and share opinions. Great blog, keep it up.
I’m more than happy to find this page. I wanted to thank you for your time just for this fantastic read!! I definitely appreciated every bit of it and i also have you saved as a favorite to look at new stuff in your website.
You made some really good points there. I looked on the internet to find out more about the issue and found most individuals will go along with your views on this website.
This is a topic that is near to my heart… Best wishes! Where are your contact details though?
There is certainly a great deal to know about this subject. I love all of the points you have made.
Greetings! Very useful advice within this article! It is the little changes that will make the most significant changes. Thanks a lot for sharing!
I really like it whenever people come together and share ideas. Great blog, keep it up.
You’re so cool! I do not believe I’ve truly read through anything like that before. So nice to discover another person with some original thoughts on this subject. Seriously.. thank you for starting this up. This website is something that is required on the web, someone with some originality.
Everything is very open with a precise explanation of the challenges. It was truly informative. Your site is extremely helpful. Thank you for sharing!
Hello there! This blog post couldn’t be written any better! Reading through this post reminds me of my previous roommate! He constantly kept preaching about this. I will send this information to him. Pretty sure he’s going to have a good read. Many thanks for sharing!
I blog often and I really appreciate your content. The article has truly peaked my interest. I will take a note of your blog and keep checking for new information about once per week. I subscribed to your RSS feed as well.
Pretty! This was an incredibly wonderful post. Thanks for providing this info.
After going over a few of the blog posts on your site, I honestly like your way of writing a blog. I book-marked it to my bookmark site list and will be checking back in the near future. Please check out my website as well and tell me what you think.
You have made some decent points there. I checked on the web to learn more about the issue and found most people will go along with your views on this website.
This site was… how do you say it? Relevant!! Finally I’ve found something which helped me. Cheers.
It’s hard to find experienced people on this topic, however, you seem like you know what you’re talking about! Thanks
Hello! I could have sworn I’ve been to this website before but after browsing through many of the articles I realized it’s new to me. Anyways, I’m definitely pleased I found it and I’ll be bookmarking it and checking back often!
Howdy! I just would like to offer you a big thumbs up for the excellent information you have got right here on this post. I’ll be coming back to your website for more soon.
This is the right web site for everyone who really wants to find out about this topic. You understand a whole lot its almost hard to argue with you (not that I really would want to…HaHa). You certainly put a new spin on a topic that’s been discussed for years. Excellent stuff, just great.
Thank you for your article post.Thanks Again. Will read on…
Greetings! Very useful advice in this particular post! It is the little changes that make the greatest changes. Thanks a lot for sharing!
This is a topic that’s near to my heart… Thank you! Where are your contact details though?
Howdy! I just want to give you a huge thumbs up for the great information you have got right here on this post. I am coming back to your website for more soon.
Howdy, I do think your blog may be having internet browser compatibility problems. When I look at your website in Safari, it looks fine however, when opening in I.E., it’s got some overlapping issues. I merely wanted to give you a quick heads up! Aside from that, excellent site.
Way cool! Some extremely valid points! I appreciate you writing this write-up plus the rest of the website is extremely good.
Howdy, There’s no doubt that your website could be having web browser compatibility problems. Whenever I look at your site in Safari, it looks fine however, when opening in IE, it’s got some overlapping issues. I just wanted to give you a quick heads up! Other than that, great site!
I could not resist commenting. Very well written!
Greetings! Very helpful advice in this particular article! It is the little changes that make the most significant changes. Thanks for sharing!
Hello there! I could have sworn I’ve been to this website before but after going through some of the articles I realized it’s new to me. Nonetheless, I’m certainly delighted I stumbled upon it and I’ll be book-marking it and checking back regularly.
Way cool! Some extremely valid points! I appreciate you writing this post plus the rest of the site is very good.
Wonderful article! We will be linking to this particularly great article on our site. Keep up the great writing.
The next time I read a blog, I hope that it doesn’t fail me as much as this one. I mean, I know it was my choice to read through, however I genuinely thought you would probably have something interesting to talk about. All I hear is a bunch of moaning about something you could fix if you weren’t too busy searching for attention.
Spot on with this write-up, I actually believe that this website needs a great deal more attention. I’ll probably be returning to see more, thanks for the advice!
Spot on with this write-up, I truly believe this amazing site needs much more attention. I’ll probably be back again to read through more, thanks for the information.
Aw, this was a really nice post. Taking the time and actual effort to make a very good article… but what can I say… I hesitate a lot and don’t seem to get nearly anything done.
May I just say what a relief to uncover someone that actually understands what they’re talking about over the internet. You definitely know how to bring a problem to light and make it important. More and more people need to read this and understand this side of your story. It’s surprising you’re not more popular because you definitely possess the gift.
I like it when individuals come together and share views. Great site, keep it up.
Oh my goodness! Awesome article dude! Thank you, However I am going through issues with your RSS. I don’t understand why I am unable to subscribe to it. Is there anybody else getting identical RSS problems? Anyone who knows the solution can you kindly respond? Thanks.
An interesting discussion is definitely worth comment. There’s no doubt that that you need to publish more on this subject, it might not be a taboo matter but typically folks don’t discuss these topics. To the next! Cheers!
Hi, I do think your blog may be having internet browser compatibility problems. Whenever I look at your blog in Safari, it looks fine however, when opening in I.E., it has some overlapping issues. I simply wanted to provide you with a quick heads up! Aside from that, fantastic website!
Very good post. I definitely appreciate this site. Thanks!
Greetings! Very useful advice within this article! It is the little changes that make the most important changes. Thanks a lot for sharing!
Spot on with this write-up, I truly think this site needs much more attention. I’ll probably be back again to read more, thanks for the info.
Everything is very open with a very clear clarification of the issues. It was truly informative. Your site is extremely helpful. Thank you for sharing!
After checking out a handful of the blog posts on your website, I seriously like your way of writing a blog. I book marked it to my bookmark website list and will be checking back in the near future. Please check out my web site as well and tell me your opinion.
Hello there! This article could not be written any better! Going through this article reminds me of my previous roommate! He continually kept talking about this. I am going to send this post to him. Fairly certain he’ll have a great read. Many thanks for sharing!
Excellent web site you have got here.. It’s difficult to find high quality writing like yours nowadays. I seriously appreciate individuals like you! Take care!!
You have made some good points there. I looked on the web for more info about the issue and found most people will go along with your views on this web site.
Good article. I am facing many of these issues as well..
An interesting discussion is definitely worth comment. There’s no doubt that that you need to write more on this topic, it might not be a taboo matter but typically folks don’t speak about such issues. To the next! All the best.
Good day! I could have sworn I’ve visited your blog before but after browsing through a few of the articles I realized it’s new to me. Anyhow, I’m definitely delighted I came across it and I’ll be bookmarking it and checking back regularly.
You are so cool! I do not suppose I’ve truly read something like this before. So great to find another person with some genuine thoughts on this topic. Seriously.. many thanks for starting this up. This website is something that’s needed on the web, someone with a bit of originality.
Way cool! Some extremely valid points! I appreciate you writing this article and the rest of the website is also very good.
Everything is very open with a clear description of the issues. It was definitely informative. Your website is very useful. Thank you for sharing!
bookmarked!!, I love your site!
Hello there! I could have sworn I’ve visited this website before but after going through many of the articles I realized it’s new to me. Nonetheless, I’m certainly delighted I discovered it and I’ll be book-marking it and checking back often!
Hi, I do think this is a great site. I stumbledupon it 😉 I may return once again since I book-marked it. Money and freedom is the greatest way to change, may you be rich and continue to guide others.
Your style is very unique in comparison to other folks I’ve read stuff from. Thank you for posting when you have the opportunity, Guess I will just book mark this blog.
Pretty! This has been a really wonderful article. Many thanks for supplying this info.
Very good post. I definitely love this website. Keep it up!
Having read this I believed it was really informative. I appreciate you taking the time and energy to put this content together. I once again find myself spending a lot of time both reading and posting comments. But so what, it was still worthwhile!
I wanted to thank you for this excellent read!! I definitely loved every bit of it. I’ve got you saved as a favorite to check out new stuff you post…
Aw, this was an exceptionally good post. Taking the time and actual effort to create a very good article… but what can I say… I put things off a lot and never manage to get nearly anything done.
After going over a handful of the blog articles on your blog, I really appreciate your way of writing a blog. I saved it to my bookmark webpage list and will be checking back soon. Take a look at my web site too and tell me what you think.
A fascinating discussion is definitely worth comment. I do believe that you need to write more on this issue, it may not be a taboo matter but typically folks don’t discuss such issues. To the next! Kind regards.
Way cool! Some very valid points! I appreciate you writing this article and also the rest of the website is really good.
This blog was… how do you say it? Relevant!! Finally I have found something which helped me. Many thanks.
After looking into a few of the blog posts on your web site, I truly appreciate your technique of blogging. I book-marked it to my bookmark website list and will be checking back soon. Take a look at my web site as well and let me know what you think.
Saved as a favorite, I really like your site.
I used to be able to find good information from your blog articles.
An outstanding share! I’ve just forwarded this onto a friend who was doing a little research on this. And he in fact bought me dinner simply because I stumbled upon it for him… lol. So let me reword this…. Thanks for the meal!! But yeah, thanx for spending the time to talk about this matter here on your web site.
Very nice write-up. I definitely appreciate this website. Stick with it!
You should take part in a contest for one of the greatest sites on the net. I most certainly will highly recommend this blog!
Greetings! Very useful advice in this particular article! It’s the little changes that make the greatest changes. Many thanks for sharing!
I love it when individuals come together and share thoughts. Great website, keep it up.
I really like it when individuals come together and share opinions. Great site, stick with it!
Everything is very open with a very clear clarification of the issues. It was truly informative. Your website is extremely helpful. Thank you for sharing!
Oh my goodness! Awesome article dude! Thank you so much, However I am encountering issues with your RSS. I don’t understand why I am unable to join it. Is there anybody else getting identical RSS problems? Anybody who knows the answer can you kindly respond? Thanx!!
Aw, this was an incredibly nice post. Spending some time and actual effort to produce a good article… but what can I say… I hesitate a lot and don’t seem to get anything done.
This is the perfect blog for anybody who would like to find out about this topic. You know so much its almost tough to argue with you (not that I really would want to…HaHa). You certainly put a new spin on a topic that has been discussed for many years. Great stuff, just wonderful.
May I just say what a comfort to discover someone that truly understands what they’re talking about online. You actually realize how to bring a problem to light and make it important. More people really need to check this out and understand this side of your story. I was surprised that you’re not more popular since you surely have the gift.
You have made some really good points there. I checked on the net for more information about the issue and found most people will go along with your views on this web site.
Everyone loves it when individuals get together and share thoughts. Great blog, continue the good work!
I’d like to thank you for the efforts you’ve put in writing this blog. I’m hoping to view the same high-grade content by you later on as well. In truth, your creative writing abilities has motivated me to get my own site now 😉
I need to to thank you for this wonderful read!! I definitely loved every little bit of it. I’ve got you saved as a favorite to check out new things you post…
Nice post. I learn something new and challenging on websites I stumbleupon everyday. It’s always interesting to read content from other writers and practice a little something from their sites.
Oh my goodness! Incredible article dude! Thank you, However I am going through troubles with your RSS. I don’t understand the reason why I cannot subscribe to it. Is there anybody else getting identical RSS issues? Anyone that knows the solution can you kindly respond? Thanx!!
Aw, this was an incredibly nice post. Spending some time and actual effort to generate a really good article… but what can I say… I procrastinate a whole lot and don’t manage to get anything done.
An outstanding share! I’ve just forwarded this onto a coworker who has been conducting a little research on this. And he in fact ordered me breakfast due to the fact that I found it for him… lol. So let me reword this…. Thanks for the meal!! But yeah, thanks for spending some time to talk about this issue here on your website.
It’s hard to find knowledgeable people about this topic, but you sound like you know what you’re talking about! Thanks
After I originally left a comment I appear to have clicked the -Notify me when new comments are added- checkbox and now each time a comment is added I get 4 emails with the exact same comment. Perhaps there is a means you can remove me from that service? Kudos.
Wonderful post! We will be linking to this particularly great post on our website. Keep up the great writing.
Greetings! Very useful advice within this post! It is the little changes that produce the most significant changes. Thanks for sharing!
This is the right blog for anybody who wishes to find out about this topic. You realize a whole lot its almost hard to argue with you (not that I personally will need to…HaHa). You definitely put a fresh spin on a subject that’s been discussed for years. Great stuff, just great.
Right here is the perfect website for everyone who wishes to find out about this topic. You understand a whole lot its almost tough to argue with you (not that I really will need to…HaHa). You certainly put a brand new spin on a topic that’s been written about for decades. Great stuff, just great.
This blog was… how do I say it? Relevant!! Finally I’ve found something which helped me. Kudos!
Pretty! This was an incredibly wonderful article. Thank you for providing this info.
Hi there! This blog post could not be written much better! Looking through this post reminds me of my previous roommate! He always kept talking about this. I will forward this post to him. Pretty sure he’s going to have a very good read. Many thanks for sharing!
That is a very good tip especially to those fresh to the blogosphere. Brief but very precise information… Many thanks for sharing this one. A must read article!
This is a topic that’s close to my heart… Thank you! Exactly where can I find the contact details for questions?
Good web site you have here.. It’s difficult to find high quality writing like yours these days. I honestly appreciate people like you! Take care!!
This is the perfect website for anybody who would like to find out about this topic. You realize a whole lot its almost hard to argue with you (not that I personally would want to…HaHa). You certainly put a fresh spin on a topic which has been written about for many years. Great stuff, just excellent.
Good post. I’m going through many of these issues as well..
Pretty! This has been a really wonderful post. Many thanks for providing these details.
This is the perfect site for anybody who hopes to find out about this topic. You realize so much its almost tough to argue with you (not that I actually will need to…HaHa). You definitely put a new spin on a topic that’s been discussed for years. Excellent stuff, just wonderful.
Good day! I could have sworn I’ve visited your blog before but after browsing through many of the posts I realized it’s new to me. Nonetheless, I’m certainly pleased I came across it and I’ll be book-marking it and checking back often.
This page truly has all the information I needed concerning this subject and didn’t know who to ask.
Way cool! Some very valid points! I appreciate you penning this article and also the rest of the website is also very good.
Great web site you have here.. It’s difficult to find high quality writing like yours these days. I seriously appreciate individuals like you! Take care!!
I was able to find good information from your blog posts.
I love it when individuals come together and share opinions. Great blog, continue the good work!
Aw, this was an extremely good post. Taking the time and actual effort to generate a top notch article… but what can I say… I put things off a whole lot and don’t seem to get anything done.
I quite like reading through an article that can make men and women think. Also, thank you for permitting me to comment.
Hello there! I could have sworn I’ve visited this website before but after looking at a few of the posts I realized it’s new to me. Nonetheless, I’m certainly pleased I found it and I’ll be bookmarking it and checking back frequently!
I wanted to thank you for this very good read!! I certainly enjoyed every bit of it. I have got you bookmarked to look at new things you post…
I’m extremely pleased to find this website. I want to to thank you for ones time due to this wonderful read!! I definitely loved every little bit of it and I have you bookmarked to look at new things in your web site.
Pretty! This was an extremely wonderful post. Thanks for providing these details.
Hello! I simply wish to offer you a big thumbs up for your excellent information you have got here on this post. I am returning to your blog for more soon.
I was very happy to find this great site. I need to to thank you for ones time for this particularly wonderful read!! I definitely savored every bit of it and i also have you saved to fav to see new information on your site.
This is a topic that’s near to my heart… Thank you! Exactly where are your contact details though?
Right here is the right webpage for anybody who would like to understand this topic. You realize so much its almost tough to argue with you (not that I personally would want to…HaHa). You certainly put a brand new spin on a subject that has been discussed for ages. Excellent stuff, just wonderful.
Very nice article. I absolutely love this site. Continue the good work!
It’s hard to find experienced people in this particular topic, but you seem like you know what you’re talking about! Thanks
I blog frequently and I really thank you for your content. This great article has truly peaked my interest. I’m going to book mark your website and keep checking for new details about once a week. I opted in for your RSS feed as well.
I was pretty pleased to find this page. I need to to thank you for ones time due to this wonderful read!! I definitely really liked every bit of it and I have you book marked to look at new information on your website.
Your style is unique compared to other folks I’ve read stuff from. I appreciate you for posting when you’ve got the opportunity, Guess I’ll just bookmark this page.
Hello there, I believe your website could possibly be having internet browser compatibility problems. When I look at your website in Safari, it looks fine however when opening in IE, it has some overlapping issues. I merely wanted to give you a quick heads up! Other than that, great website.
Everything is very open with a really clear description of the challenges. It was truly informative. Your site is useful. Thank you for sharing!
bookmarked!!, I really like your web site!
An impressive share! I have just forwarded this onto a colleague who had been doing a little homework on this. And he actually bought me lunch due to the fact that I found it for him… lol. So allow me to reword this…. Thanks for the meal!! But yeah, thanx for spending some time to discuss this issue here on your website.
Having read this I thought it was really enlightening. I appreciate you finding the time and effort to put this information together. I once again find myself personally spending a significant amount of time both reading and commenting. But so what, it was still worth it.
Great info. Lucky me I recently found your blog by accident (stumbleupon). I’ve saved as a favorite for later.
I must thank you for the efforts you have put in penning this site. I’m hoping to check out the same high-grade blog posts from you in the future as well. In truth, your creative writing abilities has encouraged me to get my own site now 😉
Everyone loves it when folks come together and share thoughts. Great website, stick with it.
This is a very good tip particularly to those new to the blogosphere. Short but very accurate info… Thank you for sharing this one. A must read post.
Very good information. Lucky me I discovered your site by accident (stumbleupon). I’ve saved as a favorite for later!
The very next time I read a blog, Hopefully it does not disappoint me just as much as this one. I mean, Yes, it was my choice to read through, nonetheless I really believed you would have something helpful to talk about. All I hear is a bunch of crying about something that you could possibly fix if you weren’t too busy looking for attention.
I absolutely love your blog.. Very nice colors & theme. Did you create this amazing site yourself? Please reply back as I’m planning to create my own blog and would like to find out where you got this from or exactly what the theme is named. Thanks.
This is a topic which is near to my heart… Many thanks! Where can I find the contact details for questions?
I quite like reading through an article that can make people think. Also, many thanks for allowing me to comment.
You should be a part of a contest for one of the most useful sites on the net. I am going to highly recommend this web site!
I really like looking through an article that will make people think. Also, thank you for allowing me to comment.
I want to to thank you for this fantastic read!! I absolutely loved every bit of it. I have got you book marked to check out new things you post…
I used to be able to find good information from your articles.
Hello there! I just want to offer you a big thumbs up for the great info you have got here on this post. I am returning to your site for more soon.
I blog frequently and I really appreciate your content. This great article has really peaked my interest. I will book mark your site and keep checking for new details about once per week. I subscribed to your RSS feed as well.
Your style is very unique in comparison to other people I’ve read stuff from. Thank you for posting when you’ve got the opportunity, Guess I will just book mark this web site.
Right here is the perfect web site for anyone who hopes to find out about this topic. You understand a whole lot its almost tough to argue with you (not that I actually will need to…HaHa). You certainly put a new spin on a topic that’s been written about for many years. Excellent stuff, just wonderful.
After looking over a number of the blog posts on your website, I truly appreciate your technique of blogging. I saved as a favorite it to my bookmark webpage list and will be checking back soon. Please visit my website too and let me know your opinion.
You have made some good points there. I checked on the internet for additional information about the issue and found most individuals will go along with your views on this website.
I blog frequently and I seriously thank you for your information. This article has really peaked my interest. I am going to bookmark your site and keep checking for new details about once a week. I subscribed to your Feed too.
You have made some decent points there. I checked on the web to learn more about the issue and found most individuals will go along with your views on this site.
Aw, this was a really good post. Spending some time and actual effort to produce a top notch article… but what can I say… I hesitate a lot and don’t seem to get anything done.
Having read this I believed it was really informative. I appreciate you spending some time and energy to put this content together. I once again find myself personally spending way too much time both reading and posting comments. But so what, it was still worth it!
You need to take part in a contest for one of the most useful blogs on the internet. I will recommend this blog!
I blog quite often and I really appreciate your content. This great article has truly peaked my interest. I will take a note of your site and keep checking for new details about once a week. I opted in for your RSS feed too.
I could not refrain from commenting. Very well written.
There is definately a lot to know about this subject. I love all of the points you made.
Hello! I could have sworn I’ve been to this website before but after browsing through many of the articles I realized it’s new to me. Anyhow, I’m certainly delighted I discovered it and I’ll be book-marking it and checking back often.
Hi there! I could have sworn I’ve visited this site before but after browsing through a few of the articles I realized it’s new to me. Anyhow, I’m certainly delighted I came across it and I’ll be book-marking it and checking back regularly.
Very good post! We are linking to this particularly great content on our website. Keep up the great writing.
I love it when people get together and share views. Great blog, continue the good work.
Aw, this was an incredibly good post. Taking the time and actual effort to generate a top notch article… but what can I say… I procrastinate a whole lot and don’t manage to get nearly anything done.
Spot on with this write-up, I honestly feel this website needs much more attention. I’ll probably be back again to read more, thanks for the information!
Hello there! I simply would like to offer you a huge thumbs up for the great information you’ve got here on this post. I’ll be coming back to your website for more soon.
Hi, I think your site could possibly be having web browser compatibility issues. Whenever I take a look at your web site in Safari, it looks fine but when opening in IE, it’s got some overlapping issues. I just wanted to give you a quick heads up! Aside from that, fantastic website!
Hi, I do believe this is an excellent website. I stumbledupon it 😉 I may revisit once again since i have book marked it. Money and freedom is the best way to change, may you be rich and continue to help other people.
This site was… how do I say it? Relevant!! Finally I have found something that helped me. Many thanks!
May I simply just say what a comfort to uncover somebody who really understands what they’re discussing online. You actually realize how to bring a problem to light and make it important. More people have to read this and understand this side of your story. I was surprised that you aren’t more popular since you surely possess the gift.
It’s hard to come by experienced people in this particular topic, but you seem like you know what you’re talking about! Thanks
This excellent website really has all of the information I needed about this subject and didn’t know who to ask.
I could not resist commenting. Well written!
Good post! We are linking to this particularly great post on our website. Keep up the good writing.
Aw, this was an incredibly nice post. Taking the time and actual effort to produce a really good article… but what can I say… I procrastinate a whole lot and never seem to get anything done.
Good article. I will be going through many of these issues as well..
I couldn’t refrain from commenting. Well written!
Next time I read a blog, I hope that it won’t disappoint me just as much as this one. I mean, I know it was my choice to read, but I actually believed you would have something useful to talk about. All I hear is a bunch of whining about something you could fix if you weren’t too busy looking for attention.
Way cool! Some very valid points! I appreciate you penning this write-up and the rest of the site is also very good.
Way cool! Some extremely valid points! I appreciate you writing this write-up plus the rest of the website is really good.
Hello there, I do believe your site might be having browser compatibility issues. When I look at your site in Safari, it looks fine however, if opening in I.E., it’s got some overlapping issues. I merely wanted to give you a quick heads up! Apart from that, excellent site.
Greetings! Very useful advice within this post! It’s the little changes that make the most significant changes. Thanks a lot for sharing!
Good blog post. I absolutely love this website. Stick with it!
A motivating discussion is worth comment. I think that you ought to publish more about this subject matter, it might not be a taboo matter but usually people don’t discuss such subjects. To the next! Best wishes!
Good post! We are linking to this particularly great content on our website. Keep up the great writing.
When I originally commented I seem to have clicked on the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I receive four emails with the same comment. Is there an easy method you can remove me from that service? Thanks a lot.
I’m impressed, I must say. Seldom do I encounter a blog that’s equally educative and amusing, and without a doubt, you have hit the nail on the head. The issue is an issue that too few men and women are speaking intelligently about. I’m very happy I found this in my search for something concerning this.
I really love your website.. Great colors & theme. Did you develop this website yourself? Please reply back as I’m wanting to create my very own site and would love to learn where you got this from or just what the theme is named. Many thanks!
Greetings! Very useful advice within this post! It is the little changes that will make the most significant changes. Thanks a lot for sharing!
Everything is very open with a really clear clarification of the challenges. It was definitely informative. Your site is extremely helpful. Many thanks for sharing!
I really like reading through a post that will make people think. Also, thanks for allowing me to comment.
I could not refrain from commenting. Perfectly written.
I want to to thank you for this fantastic read!! I absolutely enjoyed every bit of it. I’ve got you bookmarked to check out new stuff you post…
Aw, this was an extremely good post. Spending some time and actual effort to make a great article… but what can I say… I procrastinate a lot and never manage to get nearly anything done.
That is a very good tip especially to those fresh to the blogosphere. Short but very precise info… Thank you for sharing this one. A must read post.
Howdy! This post couldn’t be written much better! Looking at this article reminds me of my previous roommate! He constantly kept talking about this. I am going to send this post to him. Pretty sure he’s going to have a great read. Many thanks for sharing!
Pretty! This was a really wonderful post. Thanks for providing these details.
You’re so awesome! I do not believe I’ve truly read through something like that before. So great to find another person with some original thoughts on this topic. Really.. thanks for starting this up. This website is one thing that’s needed on the internet, someone with a little originality.
Excellent article. I’m facing a few of these issues as well..
I blog frequently and I truly thank you for your information. The article has truly peaked my interest. I am going to book mark your site and keep checking for new details about once per week. I opted in for your RSS feed too.
Aw, this was an incredibly nice post. Taking a few minutes and actual effort to create a superb article… but what can I say… I hesitate a whole lot and never manage to get anything done.
Everything is very open with a really clear description of the challenges. It was truly informative. Your site is extremely helpful. Many thanks for sharing!
Your style is very unique compared to other folks I have read stuff from. Many thanks for posting when you’ve got the opportunity, Guess I will just bookmark this page.
The very next time I read a blog, Hopefully it doesn’t disappoint me as much as this one. After all, Yes, it was my choice to read through, nonetheless I really thought you would probably have something useful to talk about. All I hear is a bunch of complaining about something you could possibly fix if you weren’t too busy searching for attention.
An outstanding share! I’ve just forwarded this onto a coworker who was doing a little research on this. And he in fact ordered me dinner due to the fact that I found it for him… lol. So let me reword this…. Thank YOU for the meal!! But yeah, thanks for spending some time to discuss this issue here on your web site.
I must thank you for the efforts you have put in penning this website. I really hope to check out the same high-grade content by you later on as well. In truth, your creative writing abilities has motivated me to get my own blog now 😉
After looking over a handful of the articles on your web page, I seriously appreciate your way of blogging. I added it to my bookmark website list and will be checking back soon. Please visit my web site too and let me know your opinion.
Excellent post! We are linking to this great article on our site. Keep up the great writing.
Spot on with this write-up, I absolutely think this website needs a lot more attention. I’ll probably be returning to read more, thanks for the advice.
Your style is unique in comparison to other folks I have read stuff from. Many thanks for posting when you have the opportunity, Guess I will just book mark this page.
Your style is really unique compared to other folks I have read stuff from. I appreciate you for posting when you’ve got the opportunity, Guess I’ll just bookmark this page.
Right here is the perfect website for everyone who hopes to understand this topic. You realize a whole lot its almost tough to argue with you (not that I personally will need to…HaHa). You certainly put a new spin on a topic that’s been written about for decades. Great stuff, just great.
Your style is unique in comparison to other folks I have read stuff from. Thank you for posting when you have the opportunity, Guess I will just bookmark this page.
After exploring a number of the articles on your site, I truly appreciate your technique of writing a blog. I added it to my bookmark webpage list and will be checking back in the near future. Take a look at my web site as well and tell me what you think.
Pretty! This was a really wonderful post. Thank you for providing this info.
Oh my goodness! Awesome article dude! Thank you, However I am experiencing difficulties with your RSS. I don’t know the reason why I cannot join it. Is there anybody getting similar RSS issues? Anybody who knows the answer will you kindly respond? Thanx!
This is a topic that’s near to my heart… Many thanks! Exactly where are your contact details though?
Your style is so unique in comparison to other folks I have read stuff from. Thanks for posting when you have the opportunity, Guess I will just book mark this web site.
Everything is very open with a very clear explanation of the issues. It was really informative. Your site is useful. Many thanks for sharing.
Very good article. I am experiencing a few of these issues as well..
Hi, I do think this is an excellent blog. I stumbledupon it 😉 I’m going to revisit yet again since i have saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to help other people.
Pretty! This was an incredibly wonderful post. Thanks for providing this information.
This is a topic that is near to my heart… Best wishes! Where can I find the contact details for questions?
Saved as a favorite, I really like your site.
When I originally left a comment I seem to have clicked the -Notify me when new comments are added- checkbox and from now on each time a comment is added I get four emails with the same comment. There has to be a means you are able to remove me from that service? Thanks.
Everything is very open with a really clear clarification of the challenges. It was really informative. Your site is useful. Thanks for sharing!
May I simply say what a comfort to find someone that really understands what they are talking about online. You certainly understand how to bring an issue to light and make it important. More and more people need to look at this and understand this side of your story. I can’t believe you aren’t more popular given that you surely possess the gift.
Hello there! I simply would like to offer you a big thumbs up for your excellent info you’ve got here on this post. I will be coming back to your site for more soon.
Right here is the right webpage for anyone who really wants to find out about this topic. You know a whole lot its almost hard to argue with you (not that I personally would want to…HaHa). You definitely put a fresh spin on a subject that’s been discussed for decades. Wonderful stuff, just great.
I couldn’t refrain from commenting. Exceptionally well written.
Hi there! I just wish to give you a big thumbs up for your great info you’ve got right here on this post. I’ll be coming back to your web site for more soon.
Hello there! This article couldn’t be written much better! Reading through this article reminds me of my previous roommate! He continually kept talking about this. I most certainly will send this post to him. Pretty sure he’s going to have a very good read. Thank you for sharing!
Good web site you have here.. It’s hard to find quality writing like yours these days. I honestly appreciate individuals like you! Take care!!
May I simply say what a comfort to discover somebody who actually understands what they are talking about on the net. You actually understand how to bring an issue to light and make it important. More and more people have to read this and understand this side of the story. It’s surprising you are not more popular given that you most certainly have the gift.
You should take part in a contest for one of the most useful websites online. I most certainly will highly recommend this site!
It’s nearly impossible to find experienced people about this topic, but you sound like you know what you’re talking about! Thanks
An impressive share! I’ve just forwarded this onto a coworker who has been doing a little homework on this. And he in fact ordered me lunch simply because I stumbled upon it for him… lol. So allow me to reword this…. Thanks for the meal!! But yeah, thanks for spending time to talk about this matter here on your blog.
Good post. I learn something new and challenging on sites I stumbleupon every day. It’s always exciting to read content from other writers and use something from their web sites.
Good post! We will be linking to this particularly great content on our website. Keep up the good writing.
Greetings! Very useful advice within this post! It’s the little changes that produce the biggest changes. Many thanks for sharing!
Spot on with this write-up, I honestly believe that this site needs a lot more attention. I’ll probably be returning to see more, thanks for the info!
Oh my goodness! Awesome article dude! Thanks, However I am having issues with your RSS. I don’t know the reason why I am unable to subscribe to it. Is there anyone else having similar RSS problems? Anyone that knows the solution can you kindly respond? Thanx.
You made some good points there. I looked on the internet for additional information about the issue and found most individuals will go along with your views on this website.
There’s definately a great deal to find out about this topic. I like all of the points you have made.
I absolutely love your blog.. Great colors & theme. Did you create this amazing site yourself? Please reply back as I’m looking to create my own personal site and want to find out where you got this from or just what the theme is named. Thank you.
This blog was… how do I say it? Relevant!! Finally I’ve found something that helped me. Many thanks.
This is a very good tip especially to those new to the blogosphere. Simple but very precise info… Thanks for sharing this one. A must read article!
After I initially left a comment I seem to have clicked on the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I get four emails with the same comment. Is there an easy method you can remove me from that service? Thanks a lot.
It’s hard to come by educated people on this topic, but you seem like you know what you’re talking about! Thanks
Saved as a favorite, I like your web site!
Excellent blog you have got here.. It’s difficult to find high-quality writing like yours these days. I really appreciate individuals like you! Take care!!
Everything is very open with a precise explanation of the challenges. It was definitely informative. Your website is extremely helpful. Many thanks for sharing!
Greetings, I do think your blog may be having web browser compatibility issues. Whenever I look at your web site in Safari, it looks fine but when opening in IE, it has some overlapping issues. I merely wanted to give you a quick heads up! Aside from that, fantastic site!
bookmarked!!, I really like your website!
Right here is the perfect webpage for everyone who really wants to find out about this topic. You understand so much its almost tough to argue with you (not that I personally would want to…HaHa). You definitely put a fresh spin on a topic which has been discussed for a long time. Great stuff, just excellent.
You’ve made some really good points there. I looked on the net for more information about the issue and found most individuals will go along with your views on this site.
The next time I read a blog, Hopefully it doesn’t disappoint me just as much as this one. After all, Yes, it was my choice to read through, but I really believed you would have something helpful to say. All I hear is a bunch of moaning about something that you can fix if you were not too busy searching for attention.
Great post. I’m dealing with many of these issues as well..
This is the perfect blog for anyone who hopes to understand this topic. You realize a whole lot its almost hard to argue with you (not that I personally will need to…HaHa). You definitely put a brand new spin on a topic that’s been discussed for many years. Wonderful stuff, just excellent.
Hi, I believe your web site could possibly be having web browser compatibility problems. When I look at your site in Safari, it looks fine however, if opening in I.E., it has some overlapping issues. I simply wanted to provide you with a quick heads up! Apart from that, great website.
Pretty! This was an extremely wonderful post. Thank you for providing these details.
I blog frequently and I really appreciate your information. The article has truly peaked my interest. I will bookmark your website and keep checking for new details about once a week. I subscribed to your Feed as well.
Hi, I do believe this is a great website. I stumbledupon it 😉 I’m going to come back once again since I saved as a favorite it. Money and freedom is the best way to change, may you be rich and continue to guide others.
bookmarked!!, I like your web site.
After exploring a few of the blog posts on your website, I really like your technique of blogging. I bookmarked it to my bookmark webpage list and will be checking back soon. Take a look at my web site too and tell me how you feel.
I could not resist commenting. Exceptionally well written!
After looking into a few of the blog posts on your site, I honestly appreciate your technique of writing a blog. I bookmarked it to my bookmark site list and will be checking back in the near future. Take a look at my website too and let me know how you feel.
Oh my goodness! Awesome article dude! Thank you, However I am having problems with your RSS. I don’t know why I cannot subscribe to it. Is there anyone else getting similar RSS problems? Anyone that knows the solution will you kindly respond? Thanx.
I was extremely pleased to uncover this great site. I need to to thank you for ones time for this particularly wonderful read!! I definitely appreciated every little bit of it and i also have you saved as a favorite to look at new information in your blog.
Howdy! I could have sworn I’ve been to this site before but after looking at a few of the posts I realized it’s new to me. Anyhow, I’m definitely pleased I came across it and I’ll be book-marking it and checking back regularly.
Greetings! Very helpful advice within this article! It is the little changes which will make the biggest changes. Thanks a lot for sharing!
Right here is the right blog for anybody who would like to understand this topic. You understand a whole lot its almost hard to argue with you (not that I really will need to…HaHa). You certainly put a fresh spin on a topic which has been discussed for years. Excellent stuff, just great.
Howdy! I just wish to offer you a big thumbs up for your great information you have right here on this post. I am coming back to your site for more soon.
You’re so cool! I don’t believe I’ve read through a single thing like this before. So great to find another person with a few original thoughts on this topic. Seriously.. thank you for starting this up. This website is something that is needed on the web, someone with some originality.
Way cool! Some very valid points! I appreciate you penning this write-up plus the rest of the site is very good.
This blog was… how do you say it? Relevant!! Finally I have found something that helped me. Appreciate it!
Aw, this was a really nice post. Taking the time and actual effort to generate a top notch article… but what can I say… I hesitate a lot and never seem to get nearly anything done.
Hi there! I could have sworn I’ve visited this blog before but after looking at many of the articles I realized it’s new to me. Regardless, I’m certainly delighted I stumbled upon it and I’ll be bookmarking it and checking back regularly!
I would like to thank you for the efforts you have put in writing this website. I really hope to see the same high-grade content by you later on as well. In fact, your creative writing abilities has inspired me to get my own blog now 😉
Great post! We are linking to this particularly great post on our website. Keep up the good writing.
Hi, I do think this is an excellent web site. I stumbledupon it 😉 I’m going to revisit yet again since i have saved as a favorite it. Money and freedom is the best way to change, may you be rich and continue to help others.
I enjoy reading through a post that can make people think. Also, thank you for allowing for me to comment.
Very good article! We will be linking to this great content on our site. Keep up the great writing.
You made some really good points there. I looked on the web to find out more about the issue and found most people will go along with your views on this web site.
This is a topic that is close to my heart… Take care! Where are your contact details though?
Hi, I do think this is a great web site. I stumbledupon it 😉 I am going to return once again since I book-marked it. Money and freedom is the greatest way to change, may you be rich and continue to guide others.
Howdy! This post could not be written any better! Looking at this article reminds me of my previous roommate! He always kept talking about this. I most certainly will send this article to him. Fairly certain he will have a good read. Many thanks for sharing!
I’m pretty pleased to discover this website. I wanted to thank you for ones time for this fantastic read!! I definitely loved every little bit of it and i also have you saved as a favorite to see new information on your blog.
Spot on with this write-up, I truly believe that this amazing site needs a great deal more attention. I’ll probably be returning to see more, thanks for the information!
Having read this I believed it was really enlightening. I appreciate you taking the time and energy to put this short article together. I once again find myself personally spending a significant amount of time both reading and commenting. But so what, it was still worth it!
I couldn’t refrain from commenting. Very well written.
This site truly has all the information and facts I needed concerning this subject and didn’t know who to ask.
Hi, I do believe this is a great site. I stumbledupon it 😉 I am going to come back once again since I saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to help others.
This excellent website truly has all of the info I needed concerning this subject and didn’t know who to ask.
Having read this I believed it was rather informative. I appreciate you finding the time and effort to put this short article together. I once again find myself personally spending a lot of time both reading and commenting. But so what, it was still worthwhile!
You are so cool! I do not believe I’ve read through anything like this before. So nice to find someone with some unique thoughts on this subject matter. Really.. thank you for starting this up. This web site is something that is needed on the web, someone with a bit of originality.
When I initially left a comment I appear to have clicked the -Notify me when new comments are added- checkbox and now whenever a comment is added I recieve 4 emails with the same comment. Is there a way you are able to remove me from that service? Thank you.
Very good blog post. I certainly love this site. Keep writing!
bookmarked!!, I love your site.
I’m excited to discover this web site. I want to to thank you for your time due to this fantastic read!! I definitely savored every part of it and I have you saved as a favorite to look at new information on your web site.
Next time I read a blog, I hope that it won’t disappoint me as much as this one. After all, Yes, it was my choice to read, but I actually believed you’d have something interesting to talk about. All I hear is a bunch of moaning about something that you could possibly fix if you were not too busy looking for attention.
After checking out a number of the blog posts on your blog, I honestly like your way of writing a blog. I bookmarked it to my bookmark site list and will be checking back soon. Take a look at my website too and tell me your opinion.
I love it whenever people get together and share opinions. Great site, keep it up!
May I simply say what a comfort to find someone that truly knows what they are talking about on the web. You actually understand how to bring an issue to light and make it important. More and more people ought to read this and understand this side of your story. I was surprised you are not more popular given that you most certainly possess the gift.
Aw, this was an exceptionally good post. Taking the time and actual effort to generate a top notch article… but what can I say… I put things off a whole lot and never manage to get anything done.
May I just say what a comfort to find a person that truly knows what they’re discussing online. You certainly realize how to bring an issue to light and make it important. More people must check this out and understand this side of your story. It’s surprising you’re not more popular because you surely possess the gift.
Great info. Lucky me I recently found your blog by accident (stumbleupon). I’ve saved it for later.
Hi, I do believe this is an excellent site. I stumbledupon it 😉 I’m going to revisit yet again since I book-marked it. Money and freedom is the best way to change, may you be rich and continue to help others.
Great info. Lucky me I found your website by chance (stumbleupon). I have bookmarked it for later!
Good day! I could have sworn I’ve been to your blog before but after looking at some of the articles I realized it’s new to me. Anyhow, I’m certainly happy I discovered it and I’ll be book-marking it and checking back often.
There’s certainly a lot to find out about this topic. I really like all the points you have made.
Your style is very unique in comparison to other people I have read stuff from. Thank you for posting when you have the opportunity, Guess I will just bookmark this web site.
I could not refrain from commenting. Well written!
Way cool! Some extremely valid points! I appreciate you penning this write-up plus the rest of the website is really good.
Next time I read a blog, Hopefully it does not disappoint me just as much as this particular one. I mean, Yes, it was my choice to read, but I genuinely thought you’d have something useful to talk about. All I hear is a bunch of whining about something that you can fix if you weren’t too busy searching for attention.
I quite like reading a post that will make people think. Also, many thanks for allowing for me to comment.
Oh my goodness! Incredible article dude! Thank you, However I am having issues with your RSS. I don’t know the reason why I am unable to join it. Is there anyone else having the same RSS problems? Anyone that knows the answer can you kindly respond? Thanks!
Way cool! Some very valid points! I appreciate you writing this write-up and the rest of the website is extremely good.
Your style is so unique compared to other people I’ve read stuff from. Many thanks for posting when you’ve got the opportunity, Guess I’ll just book mark this page.
I couldn’t resist commenting. Very well written!
After exploring a few of the blog articles on your site, I really appreciate your technique of writing a blog. I book-marked it to my bookmark webpage list and will be checking back in the near future. Take a look at my web site too and tell me your opinion.
There is certainly a great deal to find out about this issue. I really like all of the points you’ve made.
I quite like reading through an article that will make people think. Also, thank you for permitting me to comment.
Your style is very unique in comparison to other people I have read stuff from. Many thanks for posting when you have the opportunity, Guess I will just bookmark this site.
An impressive share! I have just forwarded this onto a friend who had been doing a little research on this. And he in fact ordered me lunch simply because I stumbled upon it for him… lol. So let me reword this…. Thanks for the meal!! But yeah, thanx for spending time to discuss this matter here on your website.
An intriguing discussion is definitely worth comment. I think that you ought to write more on this subject, it might not be a taboo subject but generally people do not speak about such topics. To the next! Many thanks!
Having read this I thought it was really informative. I appreciate you finding the time and energy to put this article together. I once again find myself spending a significant amount of time both reading and commenting. But so what, it was still worthwhile.
This site was… how do you say it? Relevant!! Finally I have found something which helped me. Thank you.
I was excited to discover this great site. I need to to thank you for your time for this particularly fantastic read!! I definitely savored every little bit of it and i also have you bookmarked to check out new information in your site.
An outstanding share! I have just forwarded this onto a coworker who was conducting a little research on this. And he actually bought me breakfast because I found it for him… lol. So allow me to reword this…. Thanks for the meal!! But yeah, thanx for spending some time to discuss this topic here on your blog.
After I initially commented I seem to have clicked on the -Notify me when new comments are added- checkbox and now each time a comment is added I receive 4 emails with the exact same comment. Is there an easy method you can remove me from that service? Many thanks.
Way cool! Some very valid points! I appreciate you writing this article and the rest of the site is very good.
Aw, this was an extremely good post. Finding the time and actual effort to produce a really good article… but what can I say… I put things off a whole lot and don’t seem to get anything done.
This website was… how do you say it? Relevant!! Finally I have found something which helped me. Thank you!
I love it when folks come together and share ideas. Great website, keep it up!
After I initially left a comment I seem to have clicked on the -Notify me when new comments are added- checkbox and from now on whenever a comment is added I recieve four emails with the same comment. Is there a means you are able to remove me from that service? Thank you.
Great site you’ve got here.. It’s difficult to find high quality writing like yours these days. I truly appreciate people like you! Take care!!
Spot on with this write-up, I seriously feel this website needs a great deal more attention. I’ll probably be returning to see more, thanks for the advice.
Good information. Lucky me I came across your blog by chance (stumbleupon). I’ve saved as a favorite for later.
An impressive share! I have just forwarded this onto a co-worker who has been conducting a little homework on this. And he in fact bought me breakfast due to the fact that I discovered it for him… lol. So allow me to reword this…. Thank YOU for the meal!! But yeah, thanx for spending time to discuss this matter here on your website.
An outstanding share! I’ve just forwarded this onto a co-worker who has been conducting a little research on this. And he in fact bought me lunch due to the fact that I stumbled upon it for him… lol. So let me reword this…. Thank YOU for the meal!! But yeah, thanks for spending time to discuss this issue here on your internet site.
I have to thank you for the efforts you have put in penning this blog. I’m hoping to view the same high-grade content by you later on as well. In truth, your creative writing abilities has encouraged me to get my own blog now 😉
This excellent website truly has all the info I needed concerning this subject and didn’t know who to ask.
Greetings! Very helpful advice within this post! It is the little changes which will make the largest changes. Thanks a lot for sharing!
Your style is very unique compared to other folks I have read stuff from. Many thanks for posting when you’ve got the opportunity, Guess I will just book mark this page.
I love it when people come together and share opinions. Great site, keep it up!
I love looking through a post that can make men and women think. Also, many thanks for allowing for me to comment.
Your style is very unique in comparison to other people I’ve read stuff from. Thank you for posting when you have the opportunity, Guess I will just bookmark this site.
Good post. I learn something new and challenging on websites I stumbleupon every day. It will always be helpful to read articles from other authors and practice something from other sites.
Pretty! This was an extremely wonderful post. Thanks for supplying this info.
It’s nearly impossible to find educated people on this subject, but you sound like you know what you’re talking about! Thanks
Wonderful article! We will be linking to this great article on our website. Keep up the great writing.
The next time I read a blog, Hopefully it won’t fail me just as much as this one. After all, Yes, it was my choice to read, but I truly thought you would have something useful to say. All I hear is a bunch of complaining about something that you can fix if you were not too busy searching for attention.
Good post. I am going through a few of these issues as well..
Your style is very unique in comparison to other folks I have read stuff from. I appreciate you for posting when you have the opportunity, Guess I’ll just book mark this blog.
This is a good tip especially to those new to the blogosphere. Simple but very accurate information… Appreciate your sharing this one. A must read post.
Saved as a favorite, I really like your site.
Pretty! This has been a really wonderful article. Thanks for providing these details.
I’m extremely pleased to discover this great site. I wanted to thank you for ones time for this fantastic read!! I definitely really liked every bit of it and i also have you bookmarked to see new things in your web site.
Having read this I thought it was really enlightening. I appreciate you spending some time and effort to put this informative article together. I once again find myself spending a significant amount of time both reading and leaving comments. But so what, it was still worthwhile!
Good info. Lucky me I found your blog by chance (stumbleupon). I have book marked it for later!
Everything is very open with a really clear description of the challenges. It was really informative. Your site is very useful. Thank you for sharing!
Nice post. I learn something totally new and challenging on websites I stumbleupon on a daily basis. It will always be helpful to read through content from other authors and use a little something from other websites.
I love it whenever people get together and share opinions. Great site, stick with it!
Hi, I do think this is an excellent web site. I stumbledupon it 😉 I will revisit yet again since I book marked it. Money and freedom is the best way to change, may you be rich and continue to help other people.
After checking out a handful of the blog posts on your website, I truly appreciate your way of blogging. I book-marked it to my bookmark website list and will be checking back in the near future. Please check out my website as well and let me know what you think.
This is a topic that is close to my heart… Best wishes! Where can I find the contact details for questions?
There is definately a lot to know about this subject. I like all of the points you have made.
Way cool! Some very valid points! I appreciate you writing this write-up and also the rest of the site is very good.
Hello, I do think your website might be having internet browser compatibility issues. When I take a look at your blog in Safari, it looks fine however, if opening in Internet Explorer, it has some overlapping issues. I simply wanted to give you a quick heads up! Apart from that, fantastic blog!
I wanted to thank you for this great read!! I absolutely enjoyed every little bit of it. I have got you book-marked to check out new stuff you post…
I need to to thank you for this excellent read!! I absolutely loved every bit of it. I have you bookmarked to look at new stuff you post…
You are so interesting! I don’t believe I’ve read through a single thing like this before. So great to find another person with genuine thoughts on this subject matter. Really.. thanks for starting this up. This site is something that is required on the web, someone with a little originality.
Having read this I believed it was very enlightening. I appreciate you finding the time and energy to put this information together. I once again find myself personally spending a lot of time both reading and posting comments. But so what, it was still worth it.
This is a topic that’s close to my heart… Many thanks! Exactly where can I find the contact details for questions?
You should be a part of a contest for one of the best websites on the net. I will recommend this site!
This site certainly has all the info I wanted about this subject and didn’t know who to ask.
Howdy! This blog post could not be written much better! Reading through this article reminds me of my previous roommate! He constantly kept talking about this. I’ll send this post to him. Fairly certain he’ll have a good read. I appreciate you for sharing!
Hi, I do think this is an excellent blog. I stumbledupon it 😉 I will return yet again since i have saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to guide other people.
I blog frequently and I genuinely thank you for your content. This article has really peaked my interest. I will bookmark your website and keep checking for new details about once per week. I opted in for your Feed as well.
I’d like to thank you for the efforts you’ve put in penning this site. I’m hoping to see the same high-grade blog posts by you in the future as well. In fact, your creative writing abilities has inspired me to get my own site now 😉
I absolutely love your blog.. Very nice colors & theme. Did you develop this amazing site yourself? Please reply back as I’m looking to create my own blog and would like to find out where you got this from or what the theme is called. Thank you!
Right here is the right blog for everyone who wants to find out about this topic. You realize a whole lot its almost tough to argue with you (not that I personally would want to…HaHa). You certainly put a fresh spin on a subject which has been discussed for years. Excellent stuff, just great.
Hello there! This post couldn’t be written any better! Going through this post reminds me of my previous roommate! He always kept preaching about this. I most certainly will send this article to him. Pretty sure he will have a great read. Many thanks for sharing!
You should be a part of a contest for one of the best blogs on the internet. I will highly recommend this web site!
There is definately a lot to know about this topic. I really like all of the points you made.
Spot on with this write-up, I seriously believe that this amazing site needs much more attention. I’ll probably be returning to read more, thanks for the info.
bookmarked!!, I really like your site.
Next time I read a blog, I hope that it does not disappoint me as much as this particular one. After all, Yes, it was my choice to read through, nonetheless I actually thought you would have something helpful to say. All I hear is a bunch of crying about something that you can fix if you weren’t too busy searching for attention.
bookmarked!!, I really like your web site!
I’d like to thank you for the efforts you have put in writing this site. I’m hoping to view the same high-grade content from you later on as well. In fact, your creative writing abilities has encouraged me to get my very own blog now 😉
Having read this I thought it was really informative. I appreciate you spending some time and energy to put this information together. I once again find myself personally spending way too much time both reading and commenting. But so what, it was still worthwhile.
This is a great tip particularly to those new to the blogosphere. Brief but very accurate information… Many thanks for sharing this one. A must read article!
I need to to thank you for this very good read!! I absolutely enjoyed every bit of it. I have got you bookmarked to look at new things you post…
This site was… how do I say it? Relevant!! Finally I’ve found something that helped me. Appreciate it!
An outstanding share! I’ve just forwarded this onto a co-worker who was doing a little research on this. And he in fact bought me breakfast due to the fact that I discovered it for him… lol. So allow me to reword this…. Thanks for the meal!! But yeah, thanks for spending some time to discuss this issue here on your internet site.
A fascinating discussion is definitely worth comment. I think that you need to write more about this topic, it might not be a taboo subject but usually people do not discuss these subjects. To the next! All the best.
Oh my goodness! Incredible article dude! Thank you, However I am experiencing problems with your RSS. I don’t know the reason why I can’t join it. Is there anyone else having the same RSS problems? Anyone who knows the answer can you kindly respond? Thanks!
I need to to thank you for this wonderful read!! I definitely loved every little bit of it. I have you book marked to look at new things you post…
Aw, this was a really good post. Taking a few minutes and actual effort to generate a superb article… but what can I say… I put things off a whole lot and don’t seem to get nearly anything done.
Hi, There’s no doubt that your site could possibly be having web browser compatibility problems. When I take a look at your web site in Safari, it looks fine however when opening in Internet Explorer, it’s got some overlapping issues. I just wanted to give you a quick heads up! Apart from that, excellent site!
You have made some good points there. I looked on the web for more information about the issue and found most people will go along with your views on this web site.
Hello! I just want to give you a big thumbs up for your excellent info you’ve got right here on this post. I will be coming back to your site for more soon.
You ought to take part in a contest for one of the finest blogs on the net. I’m going to recommend this web site!
This is a topic that is close to my heart… Cheers! Exactly where are your contact details though?
Spot on with this write-up, I absolutely think this site needs a lot more attention. I’ll probably be returning to read more, thanks for the info.
There is certainly a great deal to know about this topic. I like all the points you have made.
Good post! We are linking to this great post on our website. Keep up the good writing.
Good post. I learn something new and challenging on websites I stumbleupon everyday. It’s always exciting to read content from other authors and practice a little something from other websites.
It’s hard to come by knowledgeable people in this particular subject, however, you sound like you know what you’re talking about! Thanks
I like it when people get together and share thoughts. Great site, continue the good work.
An impressive share! I’ve just forwarded this onto a coworker who has been conducting a little homework on this. And he in fact bought me lunch because I stumbled upon it for him… lol. So let me reword this…. Thanks for the meal!! But yeah, thanx for spending the time to discuss this matter here on your blog.
Hello there, There’s no doubt that your site may be having internet browser compatibility issues. Whenever I look at your website in Safari, it looks fine but when opening in IE, it has some overlapping issues. I merely wanted to give you a quick heads up! Apart from that, excellent blog!
Great post. I am facing a few of these issues as well..
Way cool! Some extremely valid points! I appreciate you penning this post plus the rest of the site is very good.
I seriously love your website.. Excellent colors & theme. Did you create this web site yourself? Please reply back as I’m trying to create my own personal site and would love to know where you got this from or what the theme is called. Thanks.
Hi! I simply wish to give you a big thumbs up for the excellent info you’ve got here on this post. I will be coming back to your website for more soon.
Pretty! This has been an extremely wonderful article. Thanks for providing these details.
I’m amazed, I have to admit. Seldom do I come across a blog that’s both equally educative and entertaining, and let me tell you, you have hit the nail on the head. The problem is something which not enough men and women are speaking intelligently about. Now i’m very happy I stumbled across this in my hunt for something relating to this.
I’m extremely pleased to uncover this web site. I need to to thank you for your time for this particularly wonderful read!! I definitely liked every part of it and i also have you saved as a favorite to look at new information in your blog.
I seriously love your site.. Pleasant colors & theme. Did you build this amazing site yourself? Please reply back as I’m wanting to create my own personal website and would love to know where you got this from or exactly what the theme is called. Appreciate it!
Next time I read a blog, Hopefully it won’t fail me as much as this one. After all, Yes, it was my choice to read through, nonetheless I really believed you’d have something useful to say. All I hear is a bunch of complaining about something that you could possibly fix if you weren’t too busy seeking attention.
This is a topic which is close to my heart… Thank you! Where can I find the contact details for questions?
This is a topic that is close to my heart… Take care! Exactly where can I find the contact details for questions?
Excellent blog you have got here.. It’s hard to find high quality writing like yours these days. I honestly appreciate individuals like you! Take care!!
That is a very good tip especially to those fresh to the blogosphere. Brief but very accurate info… Many thanks for sharing this one. A must read article.
The very next time I read a blog, I hope that it won’t disappoint me as much as this particular one. After all, I know it was my choice to read through, but I truly thought you would have something helpful to talk about. All I hear is a bunch of whining about something that you can fix if you were not too busy seeking attention.
Hi! I could have sworn I’ve visited this website before but after going through some of the posts I realized it’s new to me. Regardless, I’m definitely pleased I stumbled upon it and I’ll be bookmarking it and checking back regularly.
Having read this I believed it was very informative. I appreciate you finding the time and energy to put this article together. I once again find myself personally spending a lot of time both reading and commenting. But so what, it was still worthwhile.
I really love your website.. Pleasant colors & theme. Did you develop this web site yourself? Please reply back as I’m wanting to create my own personal site and want to learn where you got this from or just what the theme is called. Many thanks.
Having read this I believed it was really enlightening. I appreciate you spending some time and energy to put this article together. I once again find myself spending way too much time both reading and commenting. But so what, it was still worth it!
Way cool! Some extremely valid points! I appreciate you penning this write-up plus the rest of the website is also really good.
I absolutely love your site.. Very nice colors & theme. Did you make this amazing site yourself? Please reply back as I’m planning to create my very own blog and would love to find out where you got this from or exactly what the theme is named. Thanks.
Spot on with this write-up, I truly believe that this amazing site needs a great deal more attention. I’ll probably be returning to see more, thanks for the advice!
Having read this I believed it was really informative. I appreciate you finding the time and energy to put this short article together. I once again find myself spending way too much time both reading and posting comments. But so what, it was still worthwhile!
There is certainly a lot to learn about this subject. I really like all the points you made.
You’ve made some really good points there. I looked on the web to find out more about the issue and found most individuals will go along with your views on this site.
Greetings! Very useful advice in this particular post! It is the little changes that produce the largest changes. Thanks for sharing!
Oh my goodness! Impressive article dude! Thank you so much, However I am having difficulties with your RSS. I don’t know the reason why I can’t join it. Is there anybody else getting the same RSS problems? Anybody who knows the answer can you kindly respond? Thanks!
An impressive share! I have just forwarded this onto a coworker who had been doing a little research on this. And he actually ordered me breakfast simply because I found it for him… lol. So let me reword this…. Thanks for the meal!! But yeah, thanks for spending time to discuss this topic here on your web site.
Hi, I do think this is a great website. I stumbledupon it 😉 I am going to come back once again since I saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to help other people.
I have to thank you for the efforts you have put in penning this site. I am hoping to view the same high-grade content by you later on as well. In truth, your creative writing abilities has motivated me to get my own, personal site now 😉
I’m impressed, I must say. Rarely do I come across a blog that’s both equally educative and entertaining, and let me tell you, you have hit the nail on the head. The problem is something which not enough men and women are speaking intelligently about. I am very happy that I stumbled across this in my search for something regarding this.
This web site really has all of the info I wanted about this subject and didn’t know who to ask.
This is the perfect website for everyone who really wants to find out about this topic. You understand so much its almost tough to argue with you (not that I personally will need to…HaHa). You certainly put a fresh spin on a subject which has been discussed for a long time. Excellent stuff, just great.
After I initially commented I appear to have clicked the -Notify me when new comments are added- checkbox and from now on each time a comment is added I recieve 4 emails with the same comment. Is there a way you can remove me from that service? Thanks a lot.
Way cool! Some extremely valid points! I appreciate you penning this write-up plus the rest of the website is extremely good.
Greetings! Very helpful advice within this article! It is the little changes that make the most significant changes. Many thanks for sharing!
I must thank you for the efforts you’ve put in writing this website. I really hope to check out the same high-grade blog posts by you later on as well. In fact, your creative writing abilities has inspired me to get my very own blog now 😉
I enjoy reading through a post that will make men and women think. Also, thank you for allowing for me to comment.
Oh my goodness! Impressive article dude! Thank you so much, However I am experiencing troubles with your RSS. I don’t understand why I am unable to subscribe to it. Is there anybody else getting similar RSS issues? Anyone that knows the answer can you kindly respond? Thanx!!
You’re so awesome! I don’t think I have read anything like that before. So great to find another person with some original thoughts on this subject. Really.. many thanks for starting this up. This web site is one thing that is required on the internet, someone with a bit of originality.
May I simply say what a comfort to uncover somebody that really knows what they’re discussing on the internet. You definitely realize how to bring a problem to light and make it important. More people have to check this out and understand this side of the story. It’s surprising you are not more popular given that you definitely have the gift.
Good post. I learn something new and challenging on sites I stumbleupon every day. It’s always exciting to read content from other writers and practice a little something from other sites.
Oh my goodness! Impressive article dude! Many thanks, However I am having issues with your RSS. I don’t know the reason why I can’t join it. Is there anybody else having identical RSS problems? Anybody who knows the solution will you kindly respond? Thanks!!
This is a great tip especially to those fresh to the blogosphere. Short but very precise info… Appreciate your sharing this one. A must read article.
Spot on with this write-up, I really feel this site needs much more attention. I’ll probably be back again to see more, thanks for the information!
Great blog you have here.. It’s hard to find excellent writing like yours these days. I honestly appreciate people like you! Take care!!
Right here is the right webpage for everyone who wishes to understand this topic. You understand a whole lot its almost tough to argue with you (not that I really will need to…HaHa). You certainly put a brand new spin on a subject that has been discussed for many years. Excellent stuff, just excellent.
An outstanding share! I have just forwarded this onto a friend who was conducting a little research on this. And he in fact bought me breakfast due to the fact that I stumbled upon it for him… lol. So allow me to reword this…. Thank YOU for the meal!! But yeah, thanks for spending some time to discuss this subject here on your website.
Spot on with this write-up, I truly believe this site needs a great deal more attention. I’ll probably be back again to see more, thanks for the advice.
Right here is the perfect blog for everyone who really wants to find out about this topic. You realize so much its almost hard to argue with you (not that I actually would want to…HaHa). You certainly put a brand new spin on a topic that has been discussed for decades. Excellent stuff, just excellent.
After going over a few of the blog articles on your blog, I really like your technique of writing a blog. I saved as a favorite it to my bookmark webpage list and will be checking back soon. Please visit my web site as well and tell me how you feel.
This web site definitely has all the information I needed about this subject and didn’t know who to ask.
Can I simply say what a comfort to find somebody that actually understands what they are talking about over the internet. You definitely know how to bring a problem to light and make it important. More and more people have to check this out and understand this side of the story. I can’t believe you are not more popular given that you surely possess the gift.
Having read this I thought it was extremely enlightening. I appreciate you taking the time and effort to put this informative article together. I once again find myself personally spending way too much time both reading and leaving comments. But so what, it was still worthwhile.
An outstanding share! I’ve just forwarded this onto a colleague who was doing a little homework on this. And he in fact ordered me breakfast because I found it for him… lol. So allow me to reword this…. Thank YOU for the meal!! But yeah, thanx for spending some time to discuss this matter here on your web page.
Greetings! Very helpful advice within this post! It’s the little changes that make the biggest changes. Many thanks for sharing!
This site definitely has all the information I needed about this subject and didn’t know who to ask.
There’s certainly a great deal to know about this topic. I like all of the points you’ve made.
I really love your site.. Pleasant colors & theme. Did you make this site yourself? Please reply back as I’m hoping to create my own personal site and would love to know where you got this from or just what the theme is named. Thank you!
I blog frequently and I genuinely appreciate your content. Your article has truly peaked my interest. I am going to take a note of your site and keep checking for new details about once per week. I subscribed to your RSS feed too.
Excellent blog you have got here.. It’s hard to find quality writing like yours these days. I honestly appreciate individuals like you! Take care!!
Howdy! I simply wish to give you a big thumbs up for the great information you’ve got here on this post. I’ll be returning to your blog for more soon.
I love it when folks come together and share thoughts. Great site, keep it up!
The next time I read a blog, I hope that it won’t disappoint me just as much as this one. I mean, I know it was my choice to read, but I actually thought you would probably have something helpful to say. All I hear is a bunch of whining about something that you can fix if you were not too busy seeking attention.
I was able to find good info from your articles.
There’s definately a great deal to learn about this subject. I really like all of the points you have made.
I’m amazed, I have to admit. Seldom do I encounter a blog that’s both educative and interesting, and let me tell you, you’ve hit the nail on the head. The issue is something that too few folks are speaking intelligently about. Now i’m very happy that I came across this in my hunt for something regarding this.
I’m amazed, I have to admit. Seldom do I come across a blog that’s both equally educative and engaging, and without a doubt, you have hit the nail on the head. The problem is an issue that not enough folks are speaking intelligently about. Now i’m very happy I stumbled across this in my search for something concerning this.
An impressive share! I’ve just forwarded this onto a friend who had been conducting a little research on this. And he in fact ordered me lunch because I stumbled upon it for him… lol. So let me reword this…. Thank YOU for the meal!! But yeah, thanx for spending some time to discuss this topic here on your website.
Hi there, I do believe your web site may be having browser compatibility problems. When I take a look at your blog in Safari, it looks fine however, when opening in Internet Explorer, it has some overlapping issues. I just wanted to provide you with a quick heads up! Apart from that, fantastic site!
After looking over a handful of the blog posts on your web site, I honestly like your way of blogging. I book-marked it to my bookmark site list and will be checking back soon. Take a look at my website too and let me know your opinion.
After looking into a number of the blog posts on your website, I really appreciate your way of writing a blog. I bookmarked it to my bookmark site list and will be checking back in the near future. Take a look at my web site too and let me know what you think.
Your style is really unique in comparison to other people I’ve read stuff from. Thank you for posting when you’ve got the opportunity, Guess I will just book mark this page.
Nice post. I learn something totally new and challenging on sites I stumbleupon every day. It will always be useful to read through content from other authors and practice a little something from their web sites.
Everyone loves it when people come together and share ideas. Great blog, keep it up!
I love it when individuals come together and share views. Great website, keep it up!
I was pretty pleased to discover this web site. I want to to thank you for ones time for this particularly wonderful read!! I definitely appreciated every part of it and I have you book marked to check out new information on your blog.
Wonderful article! We are linking to this great article on our site. Keep up the good writing.
Hi, I do think this is a great website. I stumbledupon it 😉 I will return once again since i have saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to guide others.
Howdy! This blog post could not be written any better! Looking at this article reminds me of my previous roommate! He constantly kept preaching about this. I’ll send this article to him. Pretty sure he will have a great read. Many thanks for sharing!
I really like it whenever people come together and share opinions. Great blog, continue the good work!
Can I simply just say what a comfort to find an individual who genuinely understands what they are discussing on the internet. You certainly understand how to bring a problem to light and make it important. More people really need to read this and understand this side of the story. I was surprised that you aren’t more popular given that you certainly possess the gift.
Hi there! This post could not be written much better! Looking at this post reminds me of my previous roommate! He continually kept preaching about this. I most certainly will send this post to him. Fairly certain he’s going to have a good read. Thanks for sharing!
Hello, I think your blog might be having internet browser compatibility issues. Whenever I take a look at your web site in Safari, it looks fine but when opening in IE, it has some overlapping issues. I just wanted to provide you with a quick heads up! Other than that, excellent website!
I like reading a post that will make people think. Also, thank you for allowing for me to comment.
Having read this I thought it was extremely enlightening. I appreciate you spending some time and effort to put this content together. I once again find myself spending a significant amount of time both reading and posting comments. But so what, it was still worthwhile.
Way cool! Some extremely valid points! I appreciate you writing this article and the rest of the site is very good.
Great information. Lucky me I found your site by chance (stumbleupon). I have saved it for later!
Oh my goodness! Impressive article dude! Thank you, However I am encountering problems with your RSS. I don’t understand the reason why I can’t join it. Is there anyone else having the same RSS problems? Anybody who knows the answer will you kindly respond? Thanx!!
I blog often and I genuinely appreciate your content. This great article has truly peaked my interest. I will take a note of your blog and keep checking for new information about once a week. I subscribed to your Feed too.
Hi, I do think this is an excellent site. I stumbledupon it 😉 I am going to come back yet again since I book-marked it. Money and freedom is the greatest way to change, may you be rich and continue to help others.
I’d like to thank you for the efforts you’ve put in writing this blog. I’m hoping to view the same high-grade blog posts by you in the future as well. In fact, your creative writing abilities has inspired me to get my own website now 😉
Your style is unique in comparison to other people I have read stuff from. Thanks for posting when you have the opportunity, Guess I will just bookmark this blog.
I must thank you for the efforts you have put in writing this website. I’m hoping to view the same high-grade content from you in the future as well. In truth, your creative writing abilities has encouraged me to get my own website now 😉
Greetings! Very helpful advice within this post! It’s the little changes that make the biggest changes. Thanks a lot for sharing!
I love it whenever people come together and share opinions. Great site, stick with it.
Having read this I thought it was extremely enlightening. I appreciate you spending some time and energy to put this article together. I once again find myself spending a lot of time both reading and leaving comments. But so what, it was still worth it!
I love it when folks come together and share opinions. Great blog, keep it up.
You have made some really good points there. I checked on the net for more information about the issue and found most people will go along with your views on this website.
I enjoy reading an article that will make men and women think. Also, thanks for allowing for me to comment.
Very good write-up. I certainly love this website. Keep it up!
That is a very good tip particularly to those new to the blogosphere. Short but very accurate info… Many thanks for sharing this one. A must read article!
Way cool! Some very valid points! I appreciate you penning this article and also the rest of the website is really good.
Hi, I do think this is an excellent site. I stumbledupon it 😉 I may revisit yet again since i have saved as a favorite it. Money and freedom is the best way to change, may you be rich and continue to help others.
Your style is very unique compared to other people I have read stuff from. I appreciate you for posting when you have the opportunity, Guess I’ll just book mark this page.
I love it when folks get together and share views. Great website, keep it up.
Good info. Lucky me I came across your site by chance (stumbleupon). I’ve book-marked it for later!
After I originally commented I seem to have clicked on the -Notify me when new comments are added- checkbox and now every time a comment is added I recieve 4 emails with the exact same comment. Perhaps there is an easy method you can remove me from that service? Many thanks.
Excellent article. I definitely appreciate this site. Keep it up!
There is certainly a great deal to find out about this subject. I like all of the points you have made.
I’m extremely pleased to discover this great site. I want to to thank you for ones time just for this fantastic read!! I definitely appreciated every little bit of it and I have you bookmarked to check out new things in your site.
Hi, I do believe this is a great site. I stumbledupon it 😉 I’m going to come back once again since i have bookmarked it. Money and freedom is the greatest way to change, may you be rich and continue to guide other people.
Nice post. I learn something new and challenging on websites I stumbleupon everyday. It’s always useful to read through articles from other authors and use a little something from their websites.
This is a good tip particularly to those fresh to the blogosphere. Brief but very accurate information… Many thanks for sharing this one. A must read post!
Good day! I could have sworn I’ve visited this website before but after browsing through a few of the posts I realized it’s new to me. Anyways, I’m definitely delighted I discovered it and I’ll be book-marking it and checking back regularly!
Excellent web site you have got here.. It’s hard to find high-quality writing like yours nowadays. I seriously appreciate individuals like you! Take care!!
Right here is the perfect site for everyone who really wants to understand this topic. You realize a whole lot its almost tough to argue with you (not that I personally would want to…HaHa). You certainly put a new spin on a subject which has been written about for decades. Excellent stuff, just great.
Good information. Lucky me I came across your site by chance (stumbleupon). I’ve saved it for later.
Oh my goodness! Awesome article dude! Thank you, However I am having issues with your RSS. I don’t understand why I am unable to subscribe to it. Is there anyone else getting identical RSS issues? Anyone that knows the answer can you kindly respond? Thanx.
A fascinating discussion is worth comment. I think that you should publish more about this subject, it may not be a taboo subject but typically folks don’t talk about such subjects. To the next! Kind regards!
There’s definately a great deal to learn about this subject. I love all of the points you have made.
I couldn’t resist commenting. Well written.
I couldn’t refrain from commenting. Perfectly written.
Hi, I do believe this is a great website. I stumbledupon it 😉 I am going to return yet again since I saved as a favorite it. Money and freedom is the greatest way to change, may you be rich and continue to help other people.
Your style is really unique compared to other people I have read stuff from. Many thanks for posting when you have the opportunity, Guess I’ll just bookmark this page.
It’s difficult to find educated people in this particular subject, however, you sound like you know what you’re talking about! Thanks
Excellent article! We will be linking to this great post on our site. Keep up the good writing.
Very good article. I’m facing a few of these issues as well..
This is the perfect site for anybody who wishes to understand this topic. You know a whole lot its almost tough to argue with you (not that I actually would want to…HaHa). You definitely put a new spin on a subject which has been written about for years. Wonderful stuff, just excellent.
I was able to find good information from your blog posts.
Way cool! Some very valid points! I appreciate you writing this article and also the rest of the site is also really good.
After looking at a number of the blog articles on your web page, I seriously like your way of writing a blog. I saved it to my bookmark site list and will be checking back soon. Take a look at my web site as well and let me know your opinion.
I’m amazed, I must say. Rarely do I come across a blog that’s equally educative and amusing, and let me tell you, you’ve hit the nail on the head. The issue is something too few people are speaking intelligently about. I am very happy that I came across this during my search for something relating to this.
Good article! We will be linking to this great article on our site. Keep up the good writing.
Hi, I do think this is an excellent website. I stumbledupon it 😉 I’m going to revisit yet again since I book marked it. Money and freedom is the greatest way to change, may you be rich and continue to help others.
Way cool! Some very valid points! I appreciate you penning this write-up and also the rest of the site is also very good.
Very good info. Lucky me I came across your site by chance (stumbleupon). I’ve book marked it for later!
I couldn’t refrain from commenting. Very well written!
I’m more than happy to find this site. I want to to thank you for your time just for this wonderful read!! I definitely appreciated every part of it and I have you book-marked to see new information in your web site.
Aw, this was an incredibly nice post. Taking a few minutes and actual effort to make a superb article… but what can I say… I put things off a whole lot and never manage to get nearly anything done.
You ought to take part in a contest for one of the greatest sites on the net. I will recommend this website!
Can I simply just say what a relief to uncover someone who genuinely knows what they are discussing online. You definitely realize how to bring an issue to light and make it important. More people ought to read this and understand this side of your story. It’s surprising you are not more popular since you definitely have the gift.
Oh my goodness! Amazing article dude! Thank you so much, However I am experiencing issues with your RSS. I don’t understand the reason why I can’t subscribe to it. Is there anyone else getting similar RSS problems? Anyone who knows the solution can you kindly respond? Thanks!!
It’s nearly impossible to find educated people on this topic, however, you seem like you know what you’re talking about! Thanks
There’s definately a great deal to learn about this topic. I really like all of the points you’ve made.
Your style is really unique compared to other folks I’ve read stuff from. Thanks for posting when you have the opportunity, Guess I will just bookmark this web site.
Hi! I could have sworn I’ve visited your blog before but after browsing through many of the posts I realized it’s new to me. Regardless, I’m definitely delighted I stumbled upon it and I’ll be book-marking it and checking back regularly!
You’re so cool! I do not suppose I’ve read through something like this before. So wonderful to discover someone with some genuine thoughts on this issue. Seriously.. thank you for starting this up. This web site is one thing that is required on the internet, someone with some originality.
Spot on with this write-up, I honestly believe this web site needs far more attention. I’ll probably be returning to read more, thanks for the advice.
Your style is very unique compared to other folks I have read stuff from. Thanks for posting when you have the opportunity, Guess I’ll just bookmark this web site.
I used to be able to find good info from your content.
This site was… how do you say it? Relevant!! Finally I have found something that helped me. Cheers!
Pretty! This has been a really wonderful article. Thank you for providing this info.
Greetings! Very helpful advice in this particular post! It is the little changes that will make the greatest changes. Thanks a lot for sharing!
Having read this I thought it was extremely enlightening. I appreciate you finding the time and effort to put this information together. I once again find myself personally spending a lot of time both reading and posting comments. But so what, it was still worthwhile!
I would like to thank you for the efforts you’ve put in penning this blog. I really hope to view the same high-grade content by you later on as well. In fact, your creative writing abilities has inspired me to get my own, personal blog now 😉
Everything is very open with a really clear explanation of the challenges. It was truly informative. Your website is very helpful. Thank you for sharing.
I blog quite often and I really thank you for your information. Your article has truly peaked my interest. I will book mark your site and keep checking for new information about once a week. I opted in for your RSS feed too.
Spot on with this write-up, I really think this website needs much more attention. I’ll probably be returning to see more, thanks for the advice.
Right here is the right site for anyone who would like to understand this topic. You realize so much its almost hard to argue with you (not that I really would want to…HaHa). You definitely put a fresh spin on a subject which has been written about for decades. Wonderful stuff, just great.
I blog often and I really appreciate your content. The article has really peaked my interest. I am going to take a note of your blog and keep checking for new details about once per week. I opted in for your RSS feed too.
After checking out a handful of the articles on your web page, I honestly like your technique of blogging. I bookmarked it to my bookmark webpage list and will be checking back soon. Please visit my web site too and tell me your opinion.
Having read this I believed it was really informative. I appreciate you taking the time and energy to put this article together. I once again find myself spending way too much time both reading and posting comments. But so what, it was still worthwhile!
Everything is very open with a very clear description of the challenges. It was really informative. Your site is extremely helpful. Thank you for sharing.
Having read this I believed it was rather enlightening. I appreciate you taking the time and effort to put this information together. I once again find myself personally spending way too much time both reading and commenting. But so what, it was still worthwhile!
I’m amazed, I must say. Rarely do I come across a blog that’s equally educative and amusing, and let me tell you, you have hit the nail on the head. The problem is something that too few folks are speaking intelligently about. I am very happy that I came across this in my hunt for something concerning this.
I really like it when individuals get together and share opinions. Great website, keep it up.
I wanted to thank you for this excellent read!! I definitely enjoyed every bit of it. I have got you book-marked to look at new stuff you post…
You’re so interesting! I don’t suppose I’ve truly read anything like that before. So wonderful to find somebody with genuine thoughts on this subject matter. Really.. thank you for starting this up. This website is something that’s needed on the internet, someone with a bit of originality.
Pretty! This has been an extremely wonderful post. Thanks for supplying this information.
Very nice article. I definitely love this site. Keep writing!
Pretty! This was an incredibly wonderful post. Many thanks for supplying this info.
Good article! We are linking to this particularly great content on our site. Keep up the great writing.
bookmarked!!, I like your site!
Your style is so unique in comparison to other people I have read stuff from. Many thanks for posting when you’ve got the opportunity, Guess I will just book mark this web site.
Everyone loves it when folks come together and share ideas. Great site, keep it up.
bookmarked!!, I like your web site!
Greetings! Very useful advice in this particular article! It’s the little changes that make the largest changes. Many thanks for sharing!
I truly love your website.. Pleasant colors & theme. Did you create this website yourself? Please reply back as I’m planning to create my own site and want to know where you got this from or what the theme is named. Many thanks!
Great info. Lucky me I came across your blog by accident (stumbleupon). I’ve saved it for later.
An impressive share! I have just forwarded this onto a coworker who has been doing a little homework on this. And he actually bought me breakfast simply because I stumbled upon it for him… lol. So allow me to reword this…. Thanks for the meal!! But yeah, thanx for spending some time to talk about this matter here on your web page.
Good post. I learn something totally new and challenging on websites I stumbleupon on a daily basis. It’s always helpful to read through articles from other authors and use a little something from other sites.
Good post. I’m dealing with some of these issues as well..
Good post. I learn something totally new and challenging on blogs I stumbleupon everyday. It will always be interesting to read through articles from other writers and use something from their web sites.
Good post. I learn something new and challenging on sites I stumbleupon everyday. It will always be interesting to read through articles from other writers and use a little something from their web sites.
Saved as a favorite, I like your website!
I absolutely love your blog.. Great colors & theme. Did you make this site yourself? Please reply back as I’m wanting to create my very own blog and want to find out where you got this from or exactly what the theme is called. Many thanks.
Hi there! This blog post couldn’t be written any better! Going through this post reminds me of my previous roommate! He always kept talking about this. I will forward this information to him. Fairly certain he’s going to have a very good read. Thanks for sharing!
I blog quite often and I truly appreciate your content. This article has truly peaked my interest. I’m going to bookmark your website and keep checking for new information about once per week. I opted in for your RSS feed too.
This site was… how do I say it? Relevant!! Finally I have found something which helped me. Kudos.
I’m extremely pleased to uncover this page. I wanted to thank you for your time due to this fantastic read!! I definitely loved every part of it and I have you saved as a favorite to look at new information in your blog.
I was more than happy to find this site. I need to to thank you for your time just for this fantastic read!! I definitely loved every part of it and I have you saved as a favorite to see new information in your website.
There is certainly a lot to know about this issue. I like all the points you made.
This is a topic which is close to my heart… Many thanks! Exactly where can I find the contact details for questions?
I like it whenever people get together and share ideas. Great site, keep it up.
I was able to find good information from your articles.
I couldn’t refrain from commenting. Very well written!
Spot on with this write-up, I actually believe that this amazing site needs a lot more attention. I’ll probably be returning to read more, thanks for the info.
bookmarked!!, I really like your blog!
Way cool! Some extremely valid points! I appreciate you penning this article and the rest of the website is really good.
Oh my goodness! Impressive article dude! Thank you so much, However I am encountering difficulties with your RSS. I don’t know the reason why I can’t join it. Is there anyone else having the same RSS problems? Anybody who knows the solution can you kindly respond? Thanx!!
Oh my goodness! Impressive article dude! Thank you, However I am experiencing difficulties with your RSS. I don’t know why I cannot join it. Is there anybody else having the same RSS issues? Anyone that knows the answer can you kindly respond? Thanks.
Hi, I do believe this is a great web site. I stumbledupon it 😉 I am going to revisit once again since I book-marked it. Money and freedom is the best way to change, may you be rich and continue to help others.
I could not refrain from commenting. Very well written!
Good article. I will be dealing with some of these issues as well..
Hi there! I simply want to offer you a huge thumbs up for the excellent information you have got here on this post. I am returning to your blog for more soon.
Greetings! Very useful advice within this post! It is the little changes that produce the most significant changes. Thanks a lot for sharing!
You are so cool! I do not suppose I’ve truly read something like this before. So good to find another person with genuine thoughts on this issue. Seriously.. thank you for starting this up. This web site is something that’s needed on the internet, someone with a bit of originality.
Very good blog post. I absolutely appreciate this website. Stick with it!
Good post. I learn something totally new and challenging on sites I stumbleupon everyday. It’s always helpful to read content from other authors and practice something from their sites.
I like it when individuals come together and share ideas. Great website, keep it up!
I truly love your site.. Pleasant colors & theme. Did you create this amazing site yourself? Please reply back as I’m wanting to create my own blog and want to know where you got this from or exactly what the theme is called. Thank you.
It’s hard to come by knowledgeable people in this particular topic, however, you seem like you know what you’re talking about! Thanks
That is a good tip especially to those new to the blogosphere. Brief but very precise info… Thank you for sharing this one. A must read post!
Hi! I could have sworn I’ve been to this web site before but after looking at a few of the articles I realized it’s new to me. Regardless, I’m definitely delighted I found it and I’ll be bookmarking it and checking back frequently.
You’ve made some really good points there. I looked on the web for more information about the issue and found most people will go along with your views on this web site.
Can I simply just say what a comfort to uncover someone that really understands what they’re talking about on the net. You actually realize how to bring a problem to light and make it important. More people ought to check this out and understand this side of the story. It’s surprising you are not more popular because you definitely possess the gift.
After looking into a handful of the articles on your site, I honestly appreciate your technique of blogging. I saved it to my bookmark site list and will be checking back in the near future. Take a look at my website as well and let me know what you think.
Howdy! I simply wish to offer you a huge thumbs up for your great information you have here on this post. I’ll be returning to your site for more soon.
Wonderful post! We are linking to this great content on our website. Keep up the great writing.
Hi, I do think this is a great site. I stumbledupon it 😉 I may return once again since i have book-marked it. Money and freedom is the greatest way to change, may you be rich and continue to guide other people.
Hello, There’s no doubt that your website could be having browser compatibility problems. Whenever I take a look at your site in Safari, it looks fine however, when opening in Internet Explorer, it has some overlapping issues. I simply wanted to give you a quick heads up! Besides that, excellent site!
Good post. I learn something totally new and challenging on blogs I stumbleupon on a daily basis. It’s always helpful to read articles from other writers and use a little something from their sites.
I love looking through an article that will make men and women think. Also, many thanks for allowing me to comment.
I blog quite often and I truly appreciate your content. This article has truly peaked my interest. I am going to take a note of your website and keep checking for new information about once per week. I opted in for your RSS feed too.
After I initially commented I appear to have clicked the -Notify me when new comments are added- checkbox and now whenever a comment is added I recieve 4 emails with the same comment. There has to be a means you can remove me from that service? Thanks.
This is a topic which is near to my heart… Many thanks! Exactly where can I find the contact details for questions?
After I originally commented I seem to have clicked on the -Notify me when new comments are added- checkbox and now every time a comment is added I receive four emails with the exact same comment. There has to be a way you can remove me from that service? Cheers.
Having read this I thought it was extremely informative. I appreciate you spending some time and effort to put this content together. I once again find myself personally spending a lot of time both reading and posting comments. But so what, it was still worthwhile.
Your style is so unique in comparison to other folks I have read stuff from. Thank you for posting when you have the opportunity, Guess I’ll just book mark this site.
Spot on with this write-up, I seriously believe this website needs far more attention. I’ll probably be returning to read more, thanks for the info.
Can I just say what a comfort to discover someone that genuinely knows what they are discussing on the web. You certainly realize how to bring an issue to light and make it important. More and more people really need to read this and understand this side of your story. I was surprised you’re not more popular given that you surely possess the gift.
Oh my goodness! Incredible article dude! Many thanks, However I am encountering troubles with your RSS. I don’t know why I am unable to join it. Is there anybody else having similar RSS problems? Anyone who knows the solution will you kindly respond? Thanx!
I like it whenever people get together and share ideas. Great website, keep it up!
Very nice write-up. I absolutely love this website. Continue the good work!
This is a very good tip particularly to those new to the blogosphere. Brief but very accurate info… Appreciate your sharing this one. A must read article!
Good post. I learn something totally new and challenging on websites I stumbleupon every day. It will always be helpful to read content from other writers and practice something from other sites.
I must thank you for the efforts you have put in penning this blog. I’m hoping to check out the same high-grade blog posts from you in the future as well. In truth, your creative writing abilities has encouraged me to get my own, personal blog now 😉
Having read this I believed it was extremely informative. I appreciate you spending some time and energy to put this information together. I once again find myself personally spending way too much time both reading and leaving comments. But so what, it was still worth it.
This blog was… how do you say it? Relevant!! Finally I’ve found something that helped me. Cheers!
Your style is so unique compared to other folks I have read stuff from. Thank you for posting when you’ve got the opportunity, Guess I’ll just book mark this web site.
Great blog you have got here.. It’s hard to find high quality writing like yours nowadays. I seriously appreciate individuals like you! Take care!!
A motivating discussion is worth comment. I do think that you need to publish more on this subject, it may not be a taboo subject but generally people don’t talk about such topics. To the next! Many thanks!
Good info. Lucky me I came across your website by chance (stumbleupon). I’ve bookmarked it for later.
You made some good points there. I checked on the web for additional information about the issue and found most people will go along with your views on this web site.
Aw, this was an exceptionally nice post. Finding the time and actual effort to generate a superb article… but what can I say… I procrastinate a lot and don’t manage to get nearly anything done.
I have to thank you for the efforts you have put in writing this site. I am hoping to see the same high-grade content by you in the future as well. In fact, your creative writing abilities has inspired me to get my own website now 😉
Discover how On-chain Mining Projects is evolving across modern ecosystems and why chain-native design matters. Learn what makes on-chain participation loops more sustainable than short-term emissions.
After looking at a few of the blog articles on your site, I seriously like your technique of writing a blog. I bookmarked it to my bookmark website list and will be checking back soon. Take a look at my web site too and let me know how you feel.
I could not refrain from commenting. Exceptionally well written!
Explore Gamified Mining to understand how mine-to-earn systems work without specialized hardware. See how accessible on-chain participation is changing the way users accumulate scarce assets.
I think this is a real great post.Thanks Again. Want more.
Great, thanks for sharing this post.Really looking forward to read more. Will read on…
This is one awesome article post. Fantastic.
Thanks-a-mundo for the article post. Awesome.